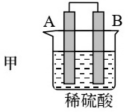
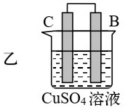
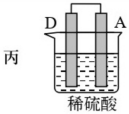
1 . 由A、B、C、D四种金属按表中装置图进行实验。
根据实验现象回答下列问题:
(1)装置甲中作正极的是_______ (填“A”或“B”)。
(2)装置乙溶液中C电极反应:_______ ;外电路中电子由_______ (填“C极向B极移动”或“B极向C极移动”)。
(3)装置丙中金属A上电极反应属于_______ (填“氧化反应”或“还原反应”)。
(4)四种金属活动性由强到弱的顺序是_______ 。
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中作正极的是
(2)装置乙溶液中C电极反应:
(3)装置丙中金属A上电极反应属于
(4)四种金属活动性由强到弱的顺序是
您最近一年使用:0次
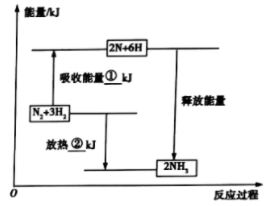
2 . (1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1mol氮气中的化学键需要吸收946kJ能量;破坏0.5mol氢气中的 键需要吸收218kJ能量;形成氨分子中1mol
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
①______ kJ,②_____ kJ。
(2)由A、B、C、D四种金属按如表所示装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为_______________ 。
②装置乙中正极的电极反应式为_______________ 。
③装置丙中溶液的pH_________ (填“变大”“变小”或“不变”)
④四种金属的活动性由强到弱的顺序是____________ 。
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: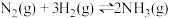 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
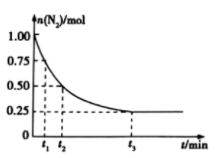
从开始反应到 min,氮气的平均反应速率为
min,氮气的平均反应速率为_________ 。
 键需要吸收218kJ能量;形成氨分子中1mol
键需要吸收218kJ能量;形成氨分子中1mol 键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。
键能够释放391kJ能量。图表示合成氨工业过程中能量的变化,请将图中①、②的能量变化的数值填在下边的横线上。①

(2)由A、B、C、D四种金属按如表所示装置进行实验。
| 装置 | 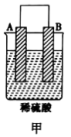 | 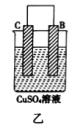 | 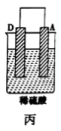 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为2L的恒容密闭容器中充入1mol
 和3mol
和3mol ,一定条件下发生反应:
,一定条件下发生反应: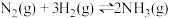 ,测得其中
,测得其中 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
 min,氮气的平均反应速率为
min,氮气的平均反应速率为
您最近一年使用:0次
解题方法
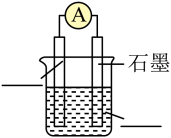
3 . 已知可逆反应: 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
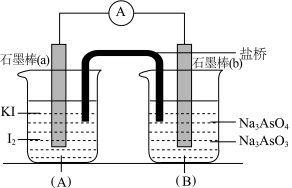
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:____________________________________ 。
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为____________________________________ 。
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为____________________________________ 。
 。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
。设计如图所示装置(盐桥中的阴、阳离子可以自由移动,盐桥在原电池中不参与反应,只起导电作用)。
进行如下操作:
(Ⅰ)向(B)烧杯中逐滴加入浓盐酸,发现电流表指针偏转;
(Ⅱ)若改往(B)烧杯中滴加质量分数为40%的NaOH溶液,发现电流表指针向相反方向偏转。
(1)两次操作过程中电流表指针偏转方向为什么会相反?
试用电极反应和化学平衡移动的原理解释此现象:
(2)(Ⅰ)操作过程中石墨棒(a)上发生的电极反应为
(3)(Ⅱ)操作过程中石墨棒(b)上发生的电极反应为
您最近一年使用:0次
4 . (1)合成氨工业是煤化工产业链中非常重要的一步。已知有一组数据:破坏1molN2中的 键需要吸收
键需要吸收 能量;破坏
能量;破坏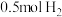 中的
中的 键需要吸收
键需要吸收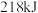 能量;形成
能量;形成 中的
中的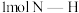 键能释放
键能释放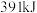 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
①________________  ,②
,②____________________  。
。

(2)用A、B、C、D四种金属按如表所示的装置进行实验。
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为__________________ 。
②装置乙中正极的电极反应式为________________ 。
③装置丙中溶液的pH________ (填“变大”“变小”或“不变”)。
④四种金属的活动性由强到弱的顺序是________ 。
(3)一定温度下,在体积为 的恒容密闭容器中充入
的恒容密闭容器中充入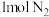 和
和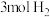 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
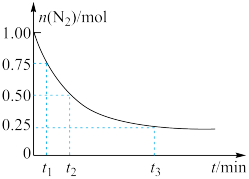
从开始反应到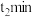 ,用
,用 表示的化学反应速率为
表示的化学反应速率为_________ 。
 键需要吸收
键需要吸收 能量;破坏
能量;破坏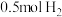 中的
中的 键需要吸收
键需要吸收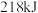 能量;形成
能量;形成 中的
中的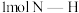 键能释放
键能释放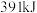 能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。
能量。图表示合成氨工业过程中能量的变化,请将图中①②的能量变化的数值填在横线上。①
 ,②
,② 。
。
(2)用A、B、C、D四种金属按如表所示的装置进行实验。
| 装置 |  甲 |  乙 |  丙 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
①装置甲中负极的电极反应式为
②装置乙中正极的电极反应式为
③装置丙中溶液的pH
④四种金属的活动性由强到弱的顺序是
(3)一定温度下,在体积为
 的恒容密闭容器中充入
的恒容密闭容器中充入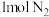 和
和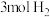 ,发生反应
,发生反应 ,测得
,测得 的物质的量随时间的变化如图所示。
的物质的量随时间的变化如图所示。
从开始反应到
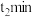 ,用
,用 表示的化学反应速率为
表示的化学反应速率为
您最近一年使用:0次
2020-09-24更新
|
651次组卷
|
3卷引用:鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 章末综合检测卷
解题方法
5 . 某同学设计实验探究构成原电池的条件,装置如图所示:
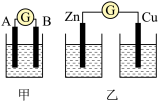
实验一:探究电极的构成。图甲中,①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
(1)结论一:________________________ ;
实验二:探究溶液的构成。图甲中,A极用锌片,B极用铜片,①液体采用无水乙醇,发现电流计指针不偏转;②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生。
(2)结论二:________________________ ;
实验三:探究图乙装置能否构成原电池。将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转。
(3)结论三:________________________ ;
思考:对该同学的实验,有同学提出了如下疑问,请你帮助解决。
(4)在图甲装置中,若A为镁片,B为铝片,电解质溶液为 溶液;负极为
溶液;负极为________ (填“A”或“B”);电流计的指针应向________ (填“右”或“左”)偏转。

实验一:探究电极的构成。图甲中,①A、B两极均选用石墨作电极,发现电流计指针不偏转;②A、B两极均选用铜片作电极,发现电流计指针不偏转;③A极用锌片,B极用铜片,发现电流计指针向左偏转;④A极用锌片,B极用石墨,发现电流计指针向左偏转。
(1)结论一:
实验二:探究溶液的构成。图甲中,A极用锌片,B极用铜片,①液体采用无水乙醇,发现电流计指针不偏转;②改用硫酸溶液,发现电流计指针偏转,B极上有气体产生。
(2)结论二:
实验三:探究图乙装置能否构成原电池。将锌、铜两电极分别放入稀硫酸中,发现锌片上有气泡产生,铜片上无明显现象,电流计指针不发生偏转。
(3)结论三:
思考:对该同学的实验,有同学提出了如下疑问,请你帮助解决。
(4)在图甲装置中,若A为镁片,B为铝片,电解质溶液为
 溶液;负极为
溶液;负极为
您最近一年使用:0次
2020-04-07更新
|
454次组卷
|
3卷引用:课时1 化学能与电能的相互转化——A学习区 夯实基础(人教版必修2)
6 . (1)下列装置属于原电池的是___________ ;
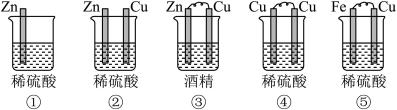
(2)在选出的原电池中,______ 是负极,发生______ (氧化、还原) 反应 ,______ 是正极 ,该极的现象___________________________ ;
(3)在该原电池的内电路中,硫酸根离子移向_________ (正、负)极。
(4)此原电池反应的化学方程式为___________________________ 。

(2)在选出的原电池中,
(3)在该原电池的内电路中,硫酸根离子移向
(4)此原电池反应的化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 人们应用原电池原理制作了多种电池,以满足不同的需要。请回答下列问题。
(1)请你利用下列反应 设计一个化学电池,该电池的负极材料是
设计一个化学电池,该电池的负极材料是_______ ,电解质溶液是_______ 。
(2)“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。在紧急状况下,应急电池会自动启动,工作原理为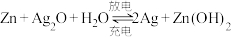 ,其正极的电极反应式为
,其正极的电极反应式为_______ 。
(3)目前正在研发的高能量密度燃料电池车,是以肼( )燃料电池作为动力来源,电池结构如图所示。
)燃料电池作为动力来源,电池结构如图所示。 溶液浓度相同,工作一段时间后,
溶液浓度相同,工作一段时间后, 浓度较大的是
浓度较大的是_______ (填“正”或“负”)极区。
②该电池负极的电极反应式为_______ 。
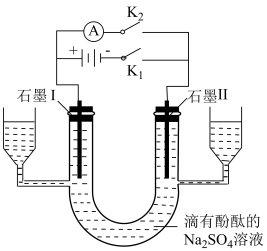
(4)利用如图所示装置探究氢氧燃料电池的工作原理。 、
、 :打开
:打开 ,闭合
,闭合 ,连接电池负极的石墨Ⅱ为
,连接电池负极的石墨Ⅱ为_______ (填“阳极”或“阴极”),阳极的电极反应式为_______ ;_______ (填“石墨Ⅰ”或“石墨Ⅱ”)附近的溶液变红。
②探究燃料电池的工作原理:在上述实验①结束后,立即打开 ,闭合
,闭合 ,可以观察到电流表指针偏转,则外电路中电子的流动方向是
,可以观察到电流表指针偏转,则外电路中电子的流动方向是_______ (填“石墨Ⅱ流向石墨Ⅰ”或“石墨Ⅰ流向石墨Ⅱ”);负极的电极反应式是_______ 。
(1)请你利用下列反应
 设计一个化学电池,该电池的负极材料是
设计一个化学电池,该电池的负极材料是(2)“神舟九号”飞船的电源系统共有3种,分别是太阳能电池帆板、镉镍蓄电池和应急电池。在紧急状况下,应急电池会自动启动,工作原理为
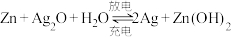 ,其正极的电极反应式为
,其正极的电极反应式为(3)目前正在研发的高能量密度燃料电池车,是以肼(
 )燃料电池作为动力来源,电池结构如图所示。
)燃料电池作为动力来源,电池结构如图所示。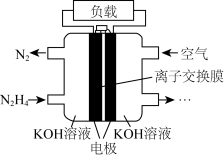
 溶液浓度相同,工作一段时间后,
溶液浓度相同,工作一段时间后, 浓度较大的是
浓度较大的是②该电池负极的电极反应式为
(4)利用如图所示装置探究氢氧燃料电池的工作原理。
 、
、 :打开
:打开 ,闭合
,闭合 ,连接电池负极的石墨Ⅱ为
,连接电池负极的石墨Ⅱ为②探究燃料电池的工作原理:在上述实验①结束后,立即打开
 ,闭合
,闭合 ,可以观察到电流表指针偏转,则外电路中电子的流动方向是
,可以观察到电流表指针偏转,则外电路中电子的流动方向是
您最近一年使用:0次
名校
解题方法
8 . 如下图设计的串联电池装置,R为变阻器,以调节电路电流。
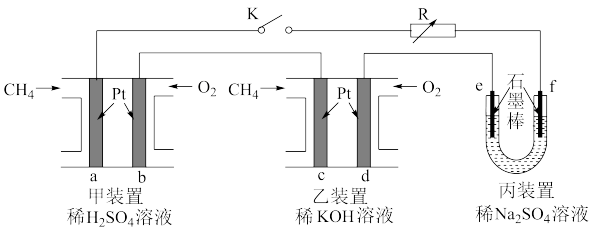
(1)写出b、c电极的电极反应式:b______________ ,c_______________ ;
(2)写出f电极的电极反应式____________________ ,向此电极区域滴入酚酞的现象为:_____________ ;该电极区域水的电离平衡被____________ (填“促进”、“抑制”或“无影响”)。
(3)闭合K一段时间后,丙装置的电解质溶液pH__________ (填“变大”、“变小”或“不变”),原因是______________ 。
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入______ g H2O就可以将析出的沉淀溶解并恢复到原有浓度。

(1)写出b、c电极的电极反应式:b
(2)写出f电极的电极反应式
(3)闭合K一段时间后,丙装置的电解质溶液pH
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入
您最近一年使用:0次
2018-10-19更新
|
487次组卷
|
5卷引用:【全国百强校】黑龙江省哈尔滨师范大学附属中学2018-2019学年高二上学期第一次月考化学试题
名校
9 . 氮及其化合物在化肥、医药、材料和国防工业中具有广泛应用。回答下列问题:
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类温饱问题做出了极大贡献。写出实验室制备氨气的方程式_______________ 。
(2)有人设想寻求合适的催化剂和电极材料,以 、
、 为电极反应物,以HCl、
为电极反应物,以HCl、 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。________ (选填“正极”、“负极”);该电池正极的电极反应式是________________ 。
(3)盐酸羟胺( )主要用作还原剂和定影剂,是一种易溶于水的盐。以
)主要用作还原剂和定影剂,是一种易溶于水的盐。以 、
、 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。_____________________ 。
②该电池在工作过程中 的浓度变化为
的浓度变化为_______ (选填“增大”、“减小”、“不变”),假设放电过程中电解质溶液的体积不变,当右室溶液质量增加5.1g时,消耗 的物质的量为
的物质的量为_________ 。
(4) 电化学传感器是将环境中
电化学传感器是将环境中 浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融
浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融 和YSZ之间的界面X会生成固体
和YSZ之间的界面X会生成固体 。
。 向
向___________ (填正极或负极)。
②写出金属电极b发生的电极反应式:_______________________ 。
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类温饱问题做出了极大贡献。写出实验室制备氨气的方程式
(2)有人设想寻求合适的催化剂和电极材料,以
 、
、 为电极反应物,以HCl、
为电极反应物,以HCl、 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型电池,如图所示。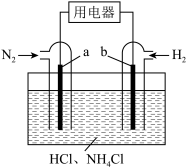
(3)盐酸羟胺(
 )主要用作还原剂和定影剂,是一种易溶于水的盐。以
)主要用作还原剂和定影剂,是一种易溶于水的盐。以 、
、 、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。
、盐酸为原料通过电化学方法一步制备盐酸羟胺的装置示意图如下。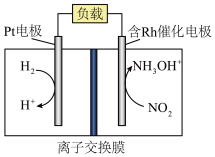
②该电池在工作过程中
 的浓度变化为
的浓度变化为 的物质的量为
的物质的量为(4)
 电化学传感器是将环境中
电化学传感器是将环境中 浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融
浓度转变为电信号的装置,工作原理如图所示,其中YSZ是固体电解质,当传感器在一定温度下工作时,在熔融 和YSZ之间的界面X会生成固体
和YSZ之间的界面X会生成固体 。
。
 向
向②写出金属电极b发生的电极反应式:
您最近一年使用:0次
名校
10 . 化学反应同时伴随着能量变化,是人类获取能量的重要途径。以下是常见的化学反应,回答(1)和(2)。 晶体与
晶体与 晶体反应
晶体反应
c.氢氧化钠与盐酸反应 d.盐酸与碳酸氢钠反应
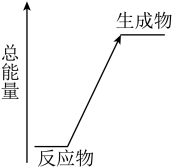
(1)以上化学反应中能用上图表示其能量变化的是______ (填字母),此类反应中有能量变化的原因是:断开反应物的化学键吸收的总能量______ (填“>”或“<”)形成生成物的化学键释放的总能量。
(2)从以上反应中选择一个反应设计原电池。
①将如图原电池装置补充完整______ 。
②证实化学能转化为电能的实验现象是______ .
③正极的电极反应式是______ .______ .
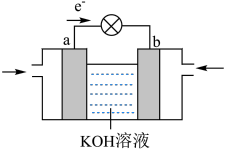
(4) 还原
还原 电化学法制备
电化学法制备 (甲醇)的工作原理如图所示。通入
(甲醇)的工作原理如图所示。通入 的一端是电池的
的一端是电池的______ 极(填“正”或“负”),通入 的一端发生的电极反应式为
的一端发生的电极反应式为______ 。生成 甲醇时,转移
甲醇时,转移______  电子。
电子。
 晶体与
晶体与 晶体反应
晶体反应c.氢氧化钠与盐酸反应 d.盐酸与碳酸氢钠反应
(1)以上化学反应中能用上图表示其能量变化的是
(2)从以上反应中选择一个反应设计原电池。
①将如图原电池装置补充完整
②证实化学能转化为电能的实验现象是
③正极的电极反应式是
(4)
 还原
还原 电化学法制备
电化学法制备 (甲醇)的工作原理如图所示。通入
(甲醇)的工作原理如图所示。通入 的一端是电池的
的一端是电池的 的一端发生的电极反应式为
的一端发生的电极反应式为 甲醇时,转移
甲醇时,转移 电子。
电子。
您最近一年使用:0次