1 . 氧化还原反应可拆分为氧化和还原两个“半反应”,某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是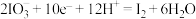 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验【硫酸与浓盐酸中 接近】。
接近】。
②甲实验的目的是___________ 。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:___________ 。
(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧 电极表面有
电极表面有 析出。
析出。
①该装置中左侧  电极作
电极作___________ (填“正”或“负”)极。
②写出该装置右侧 烧杯中的电极反应式___________ 。
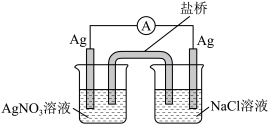
对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池__________ 。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
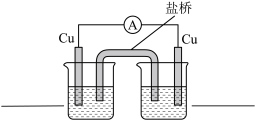
a.若能,在右装置图中填写烧杯中的试剂,并标出电子的移动方向 。
b.若不能,说明原因。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
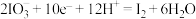 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验【硫酸与浓盐酸中
 接近】。
接近】。| 装置 | 序号 | 试管内药品 | 现象 |
 | 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧
 电极表面有
电极表面有 析出。
析出。①该装置中
 电极作
电极作②写出该装置

对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若能,在右装置图中填写烧杯中的试剂,
b.若不能,说明原因。
您最近一年使用:0次
解题方法
2 . 如图是牺牲阳极法保护金属的实验装置图,烧杯内为经过酸化的 溶液。
溶液。
下列关于该装置的叙述错误的是
 溶液。
溶液。
下列关于该装置的叙述错误的是
| A.铁作正极被保护 |
B.将 换成 换成 ,也可以保护铁不被腐蚀 ,也可以保护铁不被腐蚀 |
C.向试管中加入 溶液,无明显现象 溶液,无明显现象 |
D.正极反应式为 |
您最近一年使用:0次
解题方法
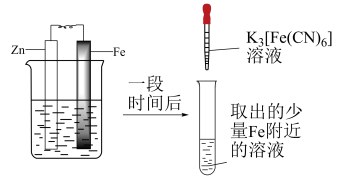
3 . 将1 g琼脂加入250 mL烧杯中,再向其中加入50 mL饱和食盐水和150 mL水。搅拌、加热、煮沸,使琼脂溶解。稍冷后,趁热把琼脂溶液分别倒入两个培养皿中,各滴入5~6滴酚酞溶液和铁氰化钾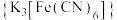 溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
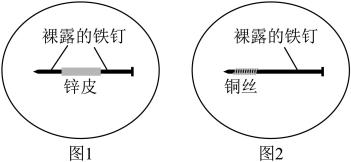
(1)图1中裸露的铁钉作___________ 极,该电极的电极反应式为___________ ,其附近可观察到的颜色变化为___________ 。
(2)图2中,在裸露的铁钉附近看到的颜色变化为___________ ,分析出现该颜色的原因:___________ ,靠近铜丝一端可观察到的颜色变化为___________ 。
(3)另一个同学也进行了上述实验操作,在图1装置中没有看到上述实验现象,其原因可能是___________ (填一条)。
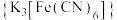 溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
溶液,混合均匀。取两个2~3cm长的铁钉,用砂纸擦光,除去表面氧化物。将裹有锌皮的铁钉放入上述培养皿中,如图1;将缠有铜丝的铁钉放入上述另一个培养皿中,如图2。
(1)图1中裸露的铁钉作
(2)图2中,在裸露的铁钉附近看到的颜色变化为
(3)另一个同学也进行了上述实验操作,在图1装置中没有看到上述实验现象,其原因可能是
您最近一年使用:0次
名校
解题方法
4 . 实验小组探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
【实验1】
(1)实验1中,电解质溶液为盐酸,镁条做原电池的___________ 极。
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为___________ 。
实验2实际获得的现象如下:
(3)ⅰ中铝条表面放电的物质是溶解在溶液中的O2,则该电极反应式为___________ 。
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是___________ 。
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
(5)根据实验3和实验4可获得的正确推论是___________(填字母序号)。
(6)由实验1~实验4可推知,铝片做电极材料时的原电池反应与___________ 等因素有关。
【实验1】
| 装置 | 实验现象 |
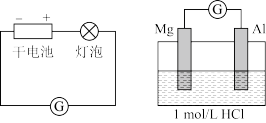 | 左侧装置电流计指针向右偏转,灯泡亮 右侧装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为
 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为实验2实际获得的现象如下:
| 装置 | 实验现象 |
 | ⅰ.电流计指针迅速向右偏转,镁条表面无气泡,铝条表面有气泡 ⅱ.电流计指针逐渐向零刻度恢复,经零刻度后继续向左偏转。镁条表面开始时无明显现象,一段时间后有少量气泡逸出,铝条表面持续有气泡逸出 |
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
| 编号 | 装置 | 实验现象 |
| 实验3 | 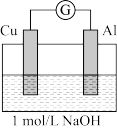 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| 实验4 | 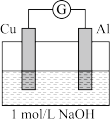 煮沸冷却后的溶液 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象:约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| A.上述两装置中,开始时铜片表面得电子的物质是O2 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
| C.铜片表面产生的气泡为H2 |
| D.由“铝条表面气泡略有减少”能推测H+在铜片表面得电子 |
您最近一年使用:0次
2023-10-24更新
|
221次组卷
|
3卷引用:北京市清华大学附属中学2023-2024学年高二上学期(G22级)统练二化学试题
名校
解题方法
5 . 有X、Y、Z、M四种金属,按如下装置进行实验,实验现象如表中。
下列说法不正确的是
| 装置 | 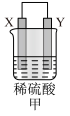 |  | 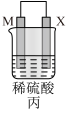 |
| 现象 | 金属X不断溶解 | Z的质量增加 | X上有气体产生 |
| A.装置甲中电子从X极流出,经外电路流入Y极 |
B.装置乙的正极反应式为: |
| C.装置丙溶液中阳离子往M极移动 |
| D.四种金属活动性由强到弱的顺序是:M>X>Y>Z |
您最近一年使用:0次
2023-07-05更新
|
166次组卷
|
2卷引用:四川省宜宾市兴文第二中学校2023-2024学年高二上学期开学考试化学试题
解题方法
6 . 利用所学电化学反应原理,解决以下问题:
Ⅰ.如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。
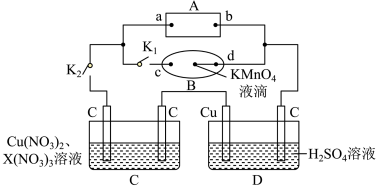
(1)闭合K1,断开K2,通电后,d端显红色,则电源b端为___________ 极,若c、d为惰性电极,检验c端产物的方法为___________ 。滤纸中央KMnO4溶液处发生的现象为___________ 。
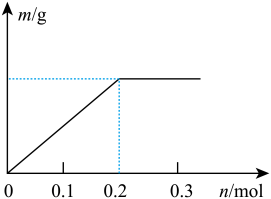
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2, 通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是___________ 。
(3)D装置中溶液是H2SO4溶液,则电极C端从开始至一段时间后的实验现象是___________ 。
Ⅱ.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :
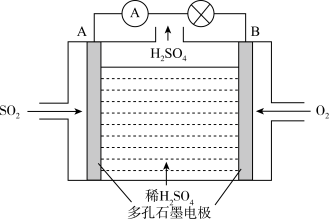
(4)电解质溶液中 离子向
离子向___________ (填“A极”或“B极” )移动。
(5)请写出负极电极反应式___________ 。
(6)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为___________ 。
Ⅰ.如图所示,A为电源,B为浸透饱和食盐水和酚酞溶液的滤纸,滤纸中央滴有一滴KMnO4溶液,C、D为电解槽,其电极材料及电解质溶液如图所示。

(1)闭合K1,断开K2,通电后,d端显红色,则电源b端为
(2)已知C装置中溶液的溶质为Cu(NO3)2和X(NO3)3,且均为0.1mol,打开K1,关闭K2, 通电一段时间后,阴极析出固体质量m(g)与通过电子的物质的量n(mol)关系如图所示,则Cu2+、X3+、H+氧化能力由大到小的顺序是

(3)D装置中溶液是H2SO4溶液,则电极C端从开始至一段时间后的实验现象是
Ⅱ.电化学技术是有效解决 CO、SO2、NOx 等大气污染的重要方法,某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下 :

(4)电解质溶液中
 离子向
离子向(5)请写出负极电极反应式
(6)用该原电池做电源,石墨做电极电解2L AgNO3和KNO3混合溶液,通电一段时间,两极均产生2.24 L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
您最近一年使用:0次
2023-07-25更新
|
89次组卷
|
2卷引用:甘肃省天水市清水县2022-2023学年高二上学期12月期中考试化学试题
名校
解题方法
7 . 某小组同学实验验证“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(1)实验验证
实验I:将0.0100mol/LAg2SO4溶液与0.0400mo/LFeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入0.0100mol/LFe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:_______ 。
②Ⅱ中溶液选用Fe2(SO4)3,不选用Fe(NO3)3的原因为_______ 。
综合上述实验,证实“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
(2)采用电化学装置进行验证。
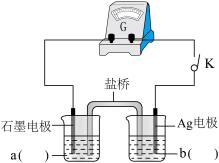
小组同学设计如上图电化学装置进行实验:
i.按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为_______ 溶液;b为_______ 溶液;(写a、b化学式)
ii.再向左侧烧杯中滴加较浓的_______ 溶液,产生的现象为_______ 。表明“Ag++Fe2+ Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(1)实验验证
实验I:将0.0100mol/LAg2SO4溶液与0.0400mo/LFeSO4溶液(pH=1)等体积混合,产生灰黑色沉淀,溶液呈黄色。
实验Ⅱ:向少量Ag粉中加入0.0100mol/LFe2(SO4)3溶液(pH=1),固体完全溶解。
①取I中沉淀,加入浓硝酸,证实灰黑色沉淀为Ag。请写出该反应的离子方程式:
②Ⅱ中溶液选用Fe2(SO4)3,不选用Fe(NO3)3的原因为
综合上述实验,证实“Ag++Fe2+
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。(2)采用电化学装置进行验证。

小组同学设计如上图电化学装置进行实验:
i.按照上图的装置图,组装好仪器后,分别在两烧杯中加入一定浓度的a、b两电解质溶液,闭合开关K,观察到的现象为:Ag电极上有灰黑色固体析出,指针向右偏转,一段时间后指针归零,说明此时反应达到平衡。则a为
ii.再向左侧烧杯中滴加较浓的
 Fe3++Ag↓”为可逆反应。
Fe3++Ag↓”为可逆反应。
您最近一年使用:0次
2023-08-20更新
|
205次组卷
|
2卷引用:福建省福州市八县(市)一中2022-2023学年高二上学期11月期中联考化学试题
22-23高一上·全国·课时练习
名校
8 . 用选项中的电极、溶液和如图所示装置可组成原电池。下列现象或结论的叙述正确的是
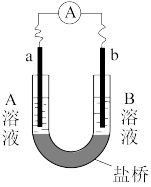

| 选项 | 电极a | 电极b | A溶液 | B溶液 | 现象或结论 |
| A | Cu | Zn | CuSO4 | ZnSO4 | 一段时间后,a增加的质量与b减少的质量相等 |
| B | Cu | Zn | 稀H2SO4 | ZnSO4 | 盐桥中阳离子向b极移动 |
| C | Fe | C | NaCl | FeCl3 | 外电路电子转移方向:b→a |
| D | C | C | FeCl3 | KI、淀粉混合液 | 若开始时只增大FeCl3溶液浓度,b极附近溶液变蓝的速度加快 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-12-27更新
|
448次组卷
|
3卷引用:北京市第一○一中学2023-2024学年高二上学期12月统练四化学试题
2023高二上·全国·专题练习
9 . 锌铜原电池的工作原理
(1)ZnZnSO4半电池:在ZnSO4溶液中,锌片逐渐溶解,即Zn被_______ ,锌原子失去电子,形成Zn2+进入溶液,即Zn-2e-=Zn2+;从锌片上释放出的_______ ,经过导线流向铜片。
(2)CuCuSO4半电池:CuSO4溶液中的Cu2+从铜片上得到_______ ,_______ 为铜单质并沉积在铜片上,即Cu2++2e-=Cu。
(3)盐桥的作用:电池工作时,盐桥中的_______ 会移向ZnSO4溶液,_______ 移向CuSO4溶液,使两溶液均保持电中性。当取出盐桥后,形成断路,反应停止。
| 装置示意图 | 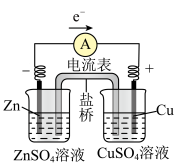 注:盐桥中装有含KCl饱和溶液的琼胶 |
| 现象 | 锌片 |
| 能量转换 | |
| 微观探析 | 在硫酸锌溶液中,负极一端的 在硫酸铜溶液中,正极一端的 |
| 电子或离子移动方向 | 电子: 盐桥: |
| 工作原理,电极反应式 | 负极:Zn-2e-=Zn2+( 正极:Cu2++2e-=Cu( |
| 总反应:Zn+Cu2+=Zn2++Cu |
(2)CuCuSO4半电池:CuSO4溶液中的Cu2+从铜片上得到
(3)盐桥的作用:电池工作时,盐桥中的
您最近一年使用:0次
名校
解题方法
10 . 由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是
| 实验装置 | 甲 | 乙 | 丙 |
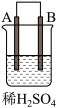 | 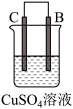 | 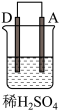 | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A.装置甲中的B金属是原电池的负极 | B.装置乙中电流的流向为B→C |
C.装置丙中溶液里的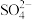 移向A 移向A | D.四种金属的活泼性顺序是D>A>B>C |
您最近一年使用:0次



