解题方法
1 . 由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题(用符号A、B、C、D回答下列问题)
(1)装置甲中负极 为___ 。装置丙中负极 为__ 。
(2)装置乙中正极 的电极反应式是___ 。
(3)四种金属活泼性由强到弱 的顺序是___ 。
| 装置 |  甲 甲 |  乙 乙 |  丙 丙 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题(用符号A、B、C、D回答下列问题)
(1)装置甲中
(2)装置乙中
(3)四种金属活泼性
您最近一年使用:0次
名校
解题方法
2 . 如图设计的串联电池装置,R为变阻器,以调节电路电流。
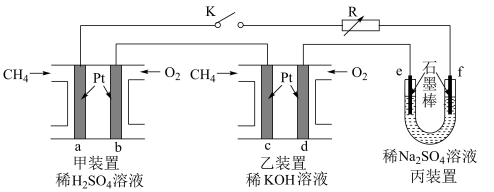
(1)写出b、c电极的电极反应式:b___ ,c___ ;
(2)写出f电极的电极反应式___ ,向此电极区域滴入酚酞的现象为:___ ;该电极区域水的电离平衡被___ (填“促进”、“抑制”或“无影响”)。
(3)闭合K一段时间后,丙装置的电解质溶液pH___ (填“变大”、“变小”或“不变”),原因是___ 。
(4)电解一段时间后丙装置析出芒硝(Na2SO4•10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入___ gH2O就可以将析出的沉淀溶解并恢复到原有浓度。
(5)有一硝酸盐晶体,其化学式为M(NO3)x•yH2O,相对分子质量为242。取1.21g该晶体溶于水,配成100mL溶液,将此溶液用石墨作电极进行电解,当有0.0100mol电子发生转移时,溶液中金属全部析出。经称量阴极增重0.320g。则
①金属M的相对原子质量为___ ;
②电解后,生成气体体积=___ (标准状况下)溶液的pH=___ (电解过程中溶液体积变化忽略不计)。要求写出计算过程。

(1)写出b、c电极的电极反应式:b
(2)写出f电极的电极反应式
(3)闭合K一段时间后,丙装置的电解质溶液pH
(4)电解一段时间后丙装置析出芒硝(Na2SO4•10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入
(5)有一硝酸盐晶体,其化学式为M(NO3)x•yH2O,相对分子质量为242。取1.21g该晶体溶于水,配成100mL溶液,将此溶液用石墨作电极进行电解,当有0.0100mol电子发生转移时,溶液中金属全部析出。经称量阴极增重0.320g。则
①金属M的相对原子质量为
②电解后,生成气体体积=
您最近一年使用:0次
3 . 由W、X、Y、Z四种金属按下列装置进行实验。下列说法不正确的是
| 装置 |  | 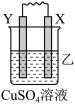 | 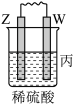 |
| 现象 | 金属W不断溶解 | Y的质量增加 | W上有气体产生 |
| A.装置甲中X作原电池正极 |
| B.装置乙中Y电极上的反应式为Cu2++2e−=Cu |
| C.装置丙中溶液的c(H+)不变 |
| D.四种金属的活动性强弱顺序为Z>W>X>Y |
您最近一年使用:0次
2020-04-30更新
|
189次组卷
|
2卷引用:江西省赣州中学2023-2024学年高二上学期月考化学试题
名校
解题方法
4 . 在下图所示的装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹,夹在被Na2SO4溶液浸湿的滤纸条上,滤纸条的中部滴有一滴KMnO4;电源有a、b两极。若在A、B中充满0.01 mol/L 的KOH溶液后倒立于同浓度的KOH溶液的水槽中,断开K1,闭合K2、K3,通直流电,实验现象如下图所示,则:
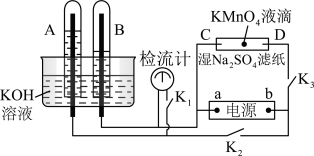
(1)断开K1,闭合K2、K3,通直流电,试管B中产生的气体为_________ (填化学式)。
(2)在Na2SO4溶液浸湿的滤纸条中部的KMnO4处现象为_____________ 。
(3)断开K1,闭合K2、K3,通直流电较长一段时间后,KOH溶液pH变__________ (填“变大”“变小”或“不变”)。
(4)电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,检流计有指数,此时该装置A试管中电极上发生的反应为_____________

(1)断开K1,闭合K2、K3,通直流电,试管B中产生的气体为
(2)在Na2SO4溶液浸湿的滤纸条中部的KMnO4处现象为
(3)断开K1,闭合K2、K3,通直流电较长一段时间后,KOH溶液pH变
(4)电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,检流计有指数,此时该装置A试管中电极上发生的反应为
您最近一年使用:0次
2019-11-20更新
|
157次组卷
|
2卷引用:山东省师范大学附属中学2019-2020学年高二上学期第五次学分认定考试化学试题
5 . 电化学技术的发展是近年来科技的热点。请结合电化学知识回答下列问题:
(1)如图甲所示的电化学装置。盐桥为浸泡了饱和氯化钾溶液的琼脂。反应一段时间,向两烧杯中分别滴加几滴酚酞,___________ (填“m”或“ 烧杯中溶液变红,盐桥中的K+向
烧杯中溶液变红,盐桥中的K+向___________ (填“m”或“n”)烧杯移动。 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 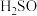 4和NaOH。
4和NaOH。___________ 。
②电解池中同时制备 和NaOH的总反应为
和NaOH的总反应为___________ 。
③d膜为___________ (填“阳”或“阴”)离子交换膜。
④当电解池中产生标准状况下22.4L H2时,理论上正极区CuSO4浓度变为___________ mol/L。
⑤从电池开始工作到停止放电,制备NaOH的质量为204g。若该电化学装置的工作效率= 。则该过程的工作效率为
。则该过程的工作效率为___________ 。
(1)如图甲所示的电化学装置。盐桥为浸泡了饱和氯化钾溶液的琼脂。反应一段时间,向两烧杯中分别滴加几滴酚酞,
 烧杯中溶液变红,盐桥中的K+向
烧杯中溶液变红,盐桥中的K+向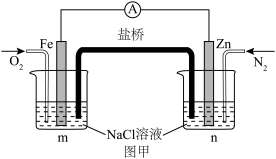
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 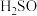 4和NaOH。
4和NaOH。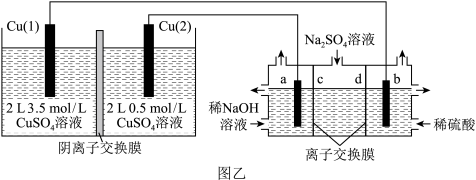
②电解池中同时制备
 和NaOH的总反应为
和NaOH的总反应为③d膜为
④当电解池中产生标准状况下22.4L H2时,理论上正极区CuSO4浓度变为
⑤从电池开始工作到停止放电,制备NaOH的质量为204g。若该电化学装置的工作效率=
 。则该过程的工作效率为
。则该过程的工作效率为
您最近一年使用:0次
名校
6 . 某同学做了如下实验:
下列说法中不正确的是
| 装置 | 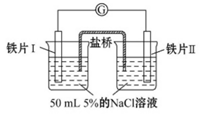 |  |
| 现象 | 电流计指针未发生偏转 | 电流计指针发生偏转 |
| A.往铁片Ⅰ所在烧杯加入蒸馏水,电流表指针会发生偏转 |
| B.用K3[Fe(CN)3]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极 |
| C.铁片Ⅰ、Ⅲ的腐蚀速率不相等 |
| D.“电流计指针未发生偏转”,铁片Ⅰ、铁片Ⅱ均未被腐蚀 |
您最近一年使用:0次
7 . 无水氯化铝是有机化工中常用的催化剂,178℃时升华,极易潮解。某化学兴趣小组设计了下列实验。根据所学知识,回答下列问题:
【实验1】利用置换反应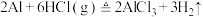 制备少量无水氯化铝,实验装置如图。
制备少量无水氯化铝,实验装置如图。
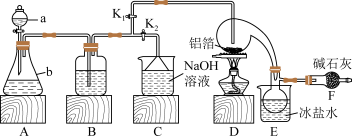
(1)a中盛放浓硫酸,b中盛放浓盐酸。将a中液体逐滴加入b中。B装置中的试剂为_______ 。
(2)实验时,检验装置气密性后,向D装置的曲颈瓶中加入铝箔,连接好装置,接下来对 、
、 进行的操作是
进行的操作是_______ ,然后加热D装置。
(3)F中干燥管内碱石灰的作用是_______ 。
【实验2】利用原电池反应检测金属的活动性顺序,甲、乙两组均使用镁片和铝片作电极,但甲组将电极放入 的硫酸中,乙组将电极放入
的硫酸中,乙组将电极放入 的氢氧化钠溶液中,装置如图所示。
的氢氧化钠溶液中,装置如图所示。
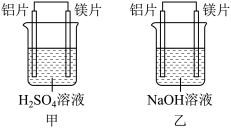
(4)写出甲电池中正极的电极反应式:_______ 。在标准状况下,正极产生 气体,得
气体,得_______ mol电子。
(5)乙电池中负极为_______ ,总反应的离子方程式为_______ 。
(6)由此实验,可得到的正确结论有_______(填标号)。
【实验1】利用置换反应
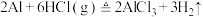 制备少量无水氯化铝,实验装置如图。
制备少量无水氯化铝,实验装置如图。
(1)a中盛放浓硫酸,b中盛放浓盐酸。将a中液体逐滴加入b中。B装置中的试剂为
(2)实验时,检验装置气密性后,向D装置的曲颈瓶中加入铝箔,连接好装置,接下来对
 、
、 进行的操作是
进行的操作是(3)F中干燥管内碱石灰的作用是
【实验2】利用原电池反应检测金属的活动性顺序,甲、乙两组均使用镁片和铝片作电极,但甲组将电极放入
 的硫酸中,乙组将电极放入
的硫酸中,乙组将电极放入 的氢氧化钠溶液中,装置如图所示。
的氢氧化钠溶液中,装置如图所示。
(4)写出甲电池中正极的电极反应式:
 气体,得
气体,得(5)乙电池中负极为
(6)由此实验,可得到的正确结论有_______(填标号)。
| A.利用原电池反应判断金属活动性顺序时应注意选择合适的介质 |
| B.镁的金属活动性不一定比铝的强 |
| C.该实验说明金属活动性顺序表已过时,已没有利用价值 |
| D.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析 |
您最近一年使用:0次
名校
8 . 铁是人类最早使用的金属,它在日常生活中的应用十分广泛。
I.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如下图所示:

①作负极的物质是______________ 。
②正极的电极反应式是_________________________________ 。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
pH=4.5时,NO3-的去除率低。其原因是_____________________________ 。

II.铁生锈是比较常见的现象,某实验小组为研究铁生锈的条件,设计了以下快速、易行的方法:首先检查制氧气装置的气密性,然后按上图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到实验现象为:①硬质玻璃管中干燥的团状细铁丝表面依然光亮,没有发生锈蚀;②硬质玻璃管中潮湿的团状细铁丝表面颜色变得灰暗,发生锈蚀;③烧杯中潮湿的团状细铁丝依然光亮。
试回答以下问题:
(1)由于与金属接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于_______ 。能表示其原理的正极反应式为________________________ 。
(2)大试管中发生的反应方程式为______________________________________ 。
(3)仪器A的名称为_______________ ,其中装的药品可以是_______________ 。
(4)有实验可知,决定铁生锈快慢的一个重要因素是___________________ 。
I.用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如下图所示:

①作负极的物质是
②正极的电极反应式是
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 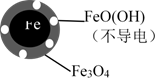 |  |
pH=4.5时,NO3-的去除率低。其原因是

II.铁生锈是比较常见的现象,某实验小组为研究铁生锈的条件,设计了以下快速、易行的方法:首先检查制氧气装置的气密性,然后按上图连接好装置,点燃酒精灯给药品加热,持续3分钟左右,观察到实验现象为:①硬质玻璃管中干燥的团状细铁丝表面依然光亮,没有发生锈蚀;②硬质玻璃管中潮湿的团状细铁丝表面颜色变得灰暗,发生锈蚀;③烧杯中潮湿的团状细铁丝依然光亮。
试回答以下问题:
(1)由于与金属接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于
(2)大试管中发生的反应方程式为
(3)仪器A的名称为
(4)有实验可知,决定铁生锈快慢的一个重要因素是
您最近一年使用:0次
名校
解题方法
9 . 如下图设计的串联电池装置,R为变阻器,以调节电路电流。
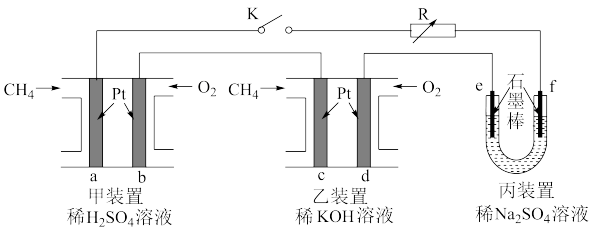
(1)写出b、c电极的电极反应式:b______________ ,c_______________ ;
(2)写出f电极的电极反应式____________________ ,向此电极区域滴入酚酞的现象为:_____________ ;该电极区域水的电离平衡被____________ (填“促进”、“抑制”或“无影响”)。
(3)闭合K一段时间后,丙装置的电解质溶液pH__________ (填“变大”、“变小”或“不变”),原因是______________ 。
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入______ g H2O就可以将析出的沉淀溶解并恢复到原有浓度。

(1)写出b、c电极的电极反应式:b
(2)写出f电极的电极反应式
(3)闭合K一段时间后,丙装置的电解质溶液pH
(4)电解一段时间后丙装置析出芒硝(Na2SO4·10H2O),若此时通入CH4的体积为22.4L(标准状况下),则向丙装置中加入
您最近一年使用:0次
2018-10-19更新
|
487次组卷
|
5卷引用:【全国百强校】黑龙江省哈尔滨师范大学附属中学2018-2019学年高二上学期第一次月考化学试题
名校
解题方法
10 . 根据下列要求回答问题。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
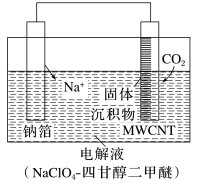
①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是___________ 。
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。
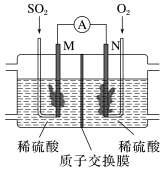
①M极发生的电极反应式为___________ 。
②质子交换膜右侧的溶液在反应后pH___________ (填“增大”“减小”或“不变”)。
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量___________ (填“增大”或“减小”)___________ g。
(1)我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示。
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28 g时,转移电子的物质的量为
③可选用高氯酸钠-四甘醇二甲醚作电解液的理由是
(2)用电化学法模拟工业处理SO2。将硫酸工业尾气中的SO2通入如图装置(电极均为惰性材料)进行实验,可用于制备硫酸,同时获得电能。

①M极发生的电极反应式为
②质子交换膜右侧的溶液在反应后pH
③当外电路通过0.2 mol e-时,质子交换膜左侧的溶液质量
您最近一年使用:0次



