名校
1 . 盐酸羟胺( )是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-,
)是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-, 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
 )是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-,
)是一种常见的还原剂,工业上采用如图1所示方法利用NO制备盐酸羟胺,图2是用图1的电池处理含Cl-, 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
| A.图2电解池工作时a电极应与Pt电极相连 |
B.处理1mol ,电路中转移5mole- ,电路中转移5mole- |
| C.电池工作时,每消耗2.24 L(标准状况下)NO,左室溶液质量增加3.3g |
| D.电池工作一段时间后,正负极区溶液的pH均下降 |
您最近一年使用:0次
2024-02-01更新
|
335次组卷
|
2卷引用:江西省宜春市第一中学2023-2024学年高三上学期1月质量检测化学试题
2 . CO2的资源化利用和转化已成为当今科学研究的热点。回答下列问题:
(1)325℃时,水在锰粉表面产生的H2可将CO2转化成甲酸,同时生成MnO。
①由H2O、Mn、CO2制备甲酸的化学方程式为___________ 。
②直接将H2和CO2混合,在325℃条件下难以生成甲酸,而在锰粉表面可以较快生成甲酸的原因是___________ 。
(2)由CO2和H2制备甲醇(CH3OH)的反应原理如下:
反应I.
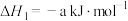 (a>0)
(a>0)
反应I.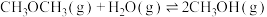
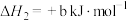 (b>0)
(b>0)
反应Ⅲ. △H3
△H3
恒压下将CO2和H2按体积比1∶3混合,在不同催化剂作用下发生反应I和反应Ⅲ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图所示。其中:CH3OH的选择性=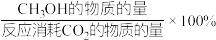 。
。
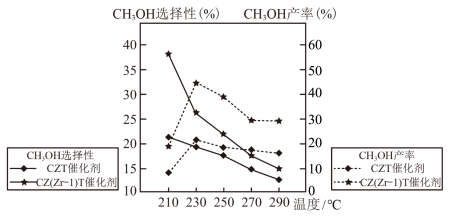
①△H3=_________ kJ∙mol-1,据此判断反应Ⅲ在_________ (填“低温”“高温”或“任意温度”)条件下有利于自发进行。
②在上述条件下,结合图像分析,合成甲醇的最佳温度是________ ,最佳催化剂是________ 。
③温度高于230℃,使用CZT催化剂时CH3OH产率随温度升高而下降的原因是___________ 。
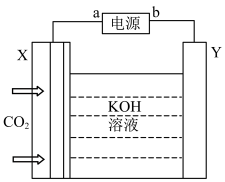
(3)模拟在碱性环境中电催化还原CO2制乙烯(X、Y均为新型电极材料,可减少CO2和碱发生副反应)装置如图所示,装置中b电极为___________ (填“正”或“负”)极,X极上发生反应的电极反应式为___________ 。
(1)325℃时,水在锰粉表面产生的H2可将CO2转化成甲酸,同时生成MnO。
①由H2O、Mn、CO2制备甲酸的化学方程式为
②直接将H2和CO2混合,在325℃条件下难以生成甲酸,而在锰粉表面可以较快生成甲酸的原因是
(2)由CO2和H2制备甲醇(CH3OH)的反应原理如下:
反应I.

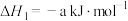 (a>0)
(a>0)反应I.
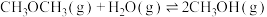
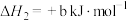 (b>0)
(b>0)反应Ⅲ.
 △H3
△H3恒压下将CO2和H2按体积比1∶3混合,在不同催化剂作用下发生反应I和反应Ⅲ,在相同的时间段内CH3OH的选择性和产率随温度的变化如图所示。其中:CH3OH的选择性=
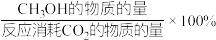 。
。
①△H3=
②在上述条件下,结合图像分析,合成甲醇的最佳温度是
③温度高于230℃,使用CZT催化剂时CH3OH产率随温度升高而下降的原因是
(3)模拟在碱性环境中电催化还原CO2制乙烯(X、Y均为新型电极材料,可减少CO2和碱发生副反应)装置如图所示,装置中b电极为

您最近一年使用:0次
解题方法
3 . 盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用向两侧电极分别通入NO和H2,以盐酸为电解质来进行制备,其电池装置(图1)和含Fe的催化电极反应机理(图2)如图。不考虑溶液体积的变化,下列说法正确的是
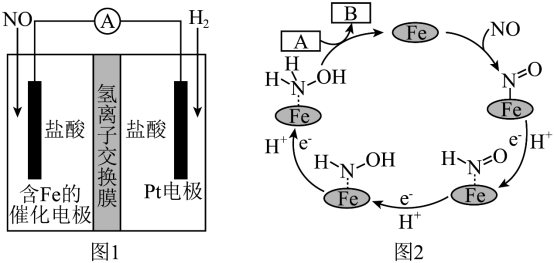

| A.电池工作时,含Fe的催化电极为正极,发生还原反应 |
B.图2中,A为H+和e-,B为 |
| C.电池工作时,每消耗标况下2.24LNO,左室溶液质量增加3.0g |
| D.电池工作一段时间后,正、负极区溶液的pH均下降 |
您最近一年使用:0次
4 . 化学性质类似 的盐酸羟胺(
的盐酸羟胺( )是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是

 的盐酸羟胺(
的盐酸羟胺( )是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
| A.图1电池工作时,Pt电极是正极 |
B.图2中,A为 和 和 ,B为 ,B为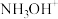 |
C.电极b接电源负极,处理 ,酸性废水中 ,酸性废水中 减少 减少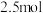 |
D.电池工作时,每消耗 (标准状况下),左室溶液质量增加 (标准状况下),左室溶液质量增加 |
您最近一年使用:0次
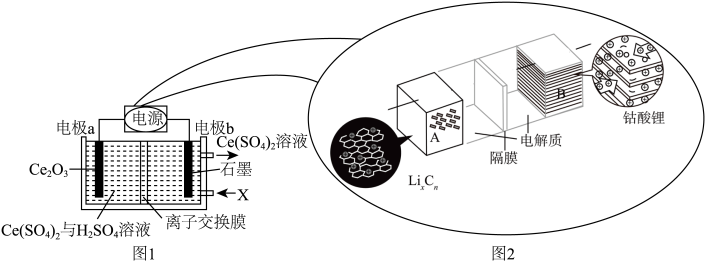
5 . 用废料Ce2O3制备Ce(SO4)2的工作原理示意图如图1所示[电源为可充电锂离子电池,该电池放电时的反应为 ]。下列说法错误的是
]。下列说法错误的是
 ]。下列说法错误的是
]。下列说法错误的是
| A.图1中的离子交换膜为阳离子交换膜 |
B.图2装置充电时,电极B的电极反应式为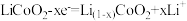 |
| C.图1装置工作一段时间后,电极a区溶液的质量减小 |
| D.锂离子电池电动汽车可有效减少光化学烟雾污染 |
您最近一年使用:0次
2023-05-18更新
|
291次组卷
|
2卷引用:湖南省部分学校2023届高三下学期5月联考化学试题
名校
解题方法
6 . 图1为浓差电池,图2为电渗析法制备磷酸二氢钠,用浓差电池为电源完成电渗析法制备磷酸二氢钠。下列说法错误 的是


| A.电极a应与Ag(II)相连 |
| B.电渗析装置中膜b为阳离子交换膜 |
| C.电渗析过程中左、右室中H2SO4和NaOH的浓度均增大 |
| D.电池从开始到停止放电,理论上可制备2.4gNaH2PO4 |
您最近一年使用:0次
2023-11-23更新
|
320次组卷
|
2卷引用:河南省郑州市实验中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
7 . 2021年6月24日,《一种硫酸铜废液制备高纯氧化铜》获得第22届中国专利优秀奖,其工艺流程如图:
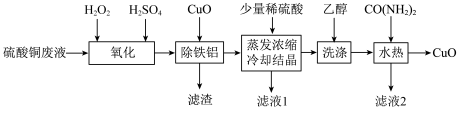
已知:①硫酸铜废液中的杂质离子仅含Na+、Fe2+、Fe3+、Al3+等。
②25℃时的溶度积:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.25×10-33。
回答下列问题:
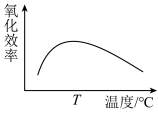
(1)双氧水能把Fe2+氧化为Fe3+,写出反应的离子方程式________ ;如图是双氧水的氧化效率随温度变化的曲线,请解释氧化效率变化的原因________ 。
(2)“除铁铝”时,为使Fe3+和Al3+沉淀完全(溶液中剩余离子的浓度小于1×10-5mol•L-1),需加入CuO调节溶液pH至______ (lg2=0.3)。
(3)“洗涤”目的是为了除去硫酸铜晶体表面沾附的少量杂质,杂质的化学式为______ ,洗涤所需要的玻璃仪器有______ ,判断晶体洗涤干净的实验操作是________ 。
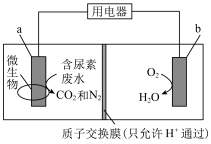
(4)如图装置可在净化含尿素[CO(NH2)2]废水的同时提供电能,以下说法正确的是________ 。

已知:①硫酸铜废液中的杂质离子仅含Na+、Fe2+、Fe3+、Al3+等。
②25℃时的溶度积:Ksp[Fe(OH)3]=2.8×10-39,Ksp[Al(OH)3]=1.25×10-33。
回答下列问题:
(1)双氧水能把Fe2+氧化为Fe3+,写出反应的离子方程式

(2)“除铁铝”时,为使Fe3+和Al3+沉淀完全(溶液中剩余离子的浓度小于1×10-5mol•L-1),需加入CuO调节溶液pH至
(3)“洗涤”目的是为了除去硫酸铜晶体表面沾附的少量杂质,杂质的化学式为
(4)如图装置可在净化含尿素[CO(NH2)2]废水的同时提供电能,以下说法正确的是

| A.温度越高,反应速率越快,装置的转化率越高 |
| B.该装置工作时,b为正极,发生还原反应 |
C.装置内溶液电流的方向由 到 到 ,电子的流向与之相反 ,电子的流向与之相反 |
| D.工作一段时间后,正极区域pH会显著升高 |
您最近一年使用:0次
名校
解题方法
8 . 化学性质类似NH4Cl的盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有Cl-、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
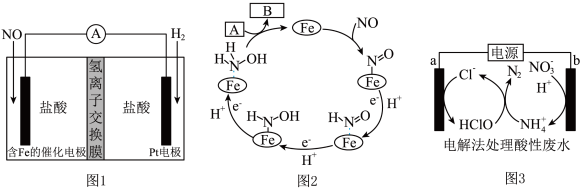
 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
| A.图1为原电池,含Fe的催化电极为负极 |
| B.图1电池工作时,每消耗3.36LH2(标准状况下),左室溶液质量增加3.3g |
| C.图2中A为H+和e-,B为NH3OH+ |
D.图3中处理 ,酸性废水中Cl-减少5mol ,酸性废水中Cl-减少5mol |
您最近一年使用:0次
2023-10-11更新
|
307次组卷
|
4卷引用:安徽省六安第一中学2023-2024学年高三上学期12月月考化学试题
名校
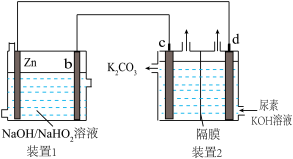
9 . 目前研究较多的Zn-H2O2电池,其电池总反应为Zn+OH-+HO =ZnO
=ZnO +H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
+H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
 =ZnO
=ZnO +H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
+H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
| A.装置1中OH-移向Zn电极 |
| B.反应过程中,d极附近的pH增大 |
C.电极c的主要反应式为CO(NH2)2-6e-+8OH-=CO +N2+6H2O +N2+6H2O |
| D.通电一段时间后,若Zn电极的质量减轻19.5g,则c电极产生N22.24L(标准状况) |
您最近一年使用:0次
名校
解题方法
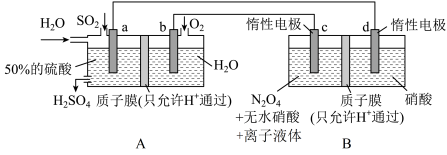
10 . 硝化剂可在化学反应中向有机化合物中引入硝基、硝酸酯基 是一种绿色硝化剂。有人设想利用工业废气
是一种绿色硝化剂。有人设想利用工业废气 ,依据电化学原理制备
,依据电化学原理制备 和
和 。装置图如下,下列说法
。装置图如下,下列说法不正确 的是
 是一种绿色硝化剂。有人设想利用工业废气
是一种绿色硝化剂。有人设想利用工业废气 ,依据电化学原理制备
,依据电化学原理制备 和
和 。装置图如下,下列说法
。装置图如下,下列说法
A.装置 可将电能转化为化学能 可将电能转化为化学能 |
B.装置 中H从a极区迁移到b极区 中H从a极区迁移到b极区 |
C.c电极表面生成 ,电极反应式为: ,电极反应式为: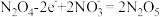 |
D.反应过程中 装置d区 装置d区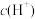 保持不变 保持不变 |
您最近一年使用:0次
2023-10-13更新
|
410次组卷
|
2卷引用:湖北省重点高中智学联盟2023-2024学年高三上学期10月联考化学试题



