1 . 下列装置及操作能达到实验目的的是
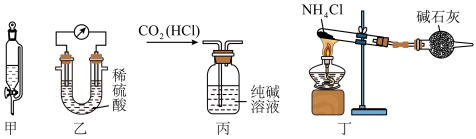
| A.利用甲装置用四氯化碳萃取碘水中的碘 | B.利用乙装置验证金属镁、铝的活泼性 |
C.利用丙装置除去 气体中混有的少量HCl 气体中混有的少量HCl | D.利用丁装置制备少量 |
您最近一年使用:0次
名校
解题方法
2 . 二氯化钒(VCl2)有强还原性和吸湿性,熔点为425°C、沸点为900°C,是制备多种医药、催化剂、含钒化合物的中间体。学习小组在实验室制备VCl2并进行相关探究。回答下列问题:
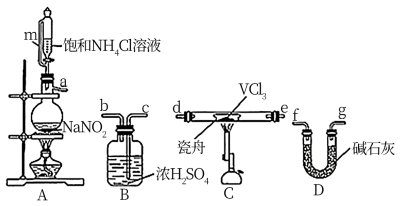
(1)小组同学通过VCl3分解制备VCl2。
①按气流方向,图中装置合理的连接顺序为_______ (用小写字母填空)。
②A中盛放NaNO2的仪器名称为_______ , 其中发生反应的离子方程式为_______ 。
③实验前需通入N2,其作用为_______ 。
(2)测定产品纯度:实验后产品中混有少量VCl3杂质。称量2.795g样品,溶于水充分水解,调pH后滴加Na2CrO4作指示剂,用0.5000mol/LAgNO3标准溶液滴定Cl-,达到滴定终点时消耗标准液体积为100.00mL(Ag2CrO4为砖红色沉淀,杂质不参加反应)。
①滴定终点的现象为_______ 。
②产品中VCl3与VCl2的物质的量之比为_______ 。
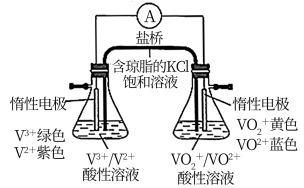
(3)小组同学进一步用如图所示装置比较含钒离子的还原性。接通电路后,观察到右侧锥形瓶中溶液蓝色逐渐变深,发生的电极反应式为_______ ,则VO2+、V2+的还原性较强的是_______ 。

(1)小组同学通过VCl3分解制备VCl2。
①按气流方向,图中装置合理的连接顺序为
②A中盛放NaNO2的仪器名称为
③实验前需通入N2,其作用为
(2)测定产品纯度:实验后产品中混有少量VCl3杂质。称量2.795g样品,溶于水充分水解,调pH后滴加Na2CrO4作指示剂,用0.5000mol/LAgNO3标准溶液滴定Cl-,达到滴定终点时消耗标准液体积为100.00mL(Ag2CrO4为砖红色沉淀,杂质不参加反应)。
①滴定终点的现象为
②产品中VCl3与VCl2的物质的量之比为
(3)小组同学进一步用如图所示装置比较含钒离子的还原性。接通电路后,观察到右侧锥形瓶中溶液蓝色逐渐变深,发生的电极反应式为

您最近一年使用:0次
2021-05-02更新
|
820次组卷
|
2卷引用:黑龙江省哈尔滨市第六中学2021届高三下学期第二次模拟考试理科综合化学试题
3 . 用如图所示装置进行相应实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 | 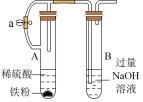 |  | 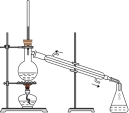 | 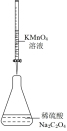 |
| 目的 | 制取 沉淀 沉淀 | 将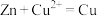 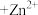 设计成原电池装置 设计成原电池装置 | 分离苯和硝基苯 | 测定 溶液的物质的量浓度 溶液的物质的量浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-18更新
|
1279次组卷
|
4卷引用:湖北省2022届高三5月联考化学试题
湖北省2022届高三5月联考化学试题(已下线)专题11 化学实验基础-三年(2020-2022)高考真题分项汇编青海省西宁市城西区青海师范大学附属实验中学2022-2023学年高二上学期12月月考化学试题 吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题
解题方法
4 . 为探究 与
与 溶液能否发生氧化还原反应,设计了如下装置:闭合K一段时间后,观察到Y电极表面有银白色物质析出。下列说法正确的是
溶液能否发生氧化还原反应,设计了如下装置:闭合K一段时间后,观察到Y电极表面有银白色物质析出。下列说法正确的是
 与
与 溶液能否发生氧化还原反应,设计了如下装置:闭合K一段时间后,观察到Y电极表面有银白色物质析出。下列说法正确的是
溶液能否发生氧化还原反应,设计了如下装置:闭合K一段时间后,观察到Y电极表面有银白色物质析出。下列说法正确的是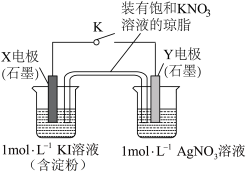
| A.Y电极为阴极 | B.右侧烧杯中 经盐桥移向左侧烧杯 经盐桥移向左侧烧杯 |
C.闭合K后右侧烧杯中溶液 不断升高 不断升高 | D.若将X电极换成 ,实验现象不变 ,实验现象不变 |
您最近一年使用:0次
5 . 下列有关实验操作、现象和所得结论均正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向2mL0.1mol/LNaCl溶液中加入过量的 溶液后,再加1mL0.1mol/LNaI,出现黄色沉淀。 溶液后,再加1mL0.1mol/LNaI,出现黄色沉淀。 | Ksp(AgCl)>Ksp(AgI) |
| B | 将镁片和铝片用导线连接后插入NaOH溶液中,镁片表面产生气泡 | 该装置构成了原电池,铝片做负极。 |
| C | 向某溶液中加入稀NaOH溶液,用湿润的红色石蕊试纸检验,无明显现象 | 溶液中一定无 |
| D | 向 溶液中通入 溶液中通入 和X气体,产生白色沉淀 和X气体,产生白色沉淀 | 气体X一定具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是
| 实验装置与现象 | |||
| 装置 | 甲 | 乙 | 丙 |
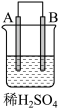 | 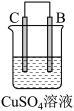 | 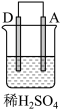 | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A.装置甲中的B金属是原电池的负极 | B.装置乙中的C金属是原电池的阳极 |
| C.装置丙中的D金属是原电池的正极 | D.四种金属的活泼性顺序是D>A>B>C |
您最近一年使用:0次
2022-09-16更新
|
99次组卷
|
5卷引用:浙江省2018版考前特训(2017年10月):选考仿真测试卷(一)
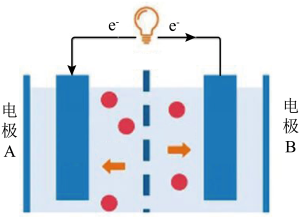
7 . 钠电池具有价格优势,且综合性能也明显优于铅酸蓄电池,电池装置如图所示,负极的电极反应为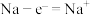 ,目前常以单晶
,目前常以单晶 纳米线、橄榄石型
纳米线、橄榄石型 等材料为正极。下列有关说法错误的是
等材料为正极。下列有关说法错误的是
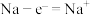 ,目前常以单晶
,目前常以单晶 纳米线、橄榄石型
纳米线、橄榄石型 等材料为正极。下列有关说法错误的是
等材料为正极。下列有关说法错误的是
| A.放电时,电极A为电池的负极 |
B.充电时, 向电极A移动 向电极A移动 |
C.单晶 纳米线作电极材料的优点在于比表面积大 纳米线作电极材料的优点在于比表面积大 |
D.橄榄石型 可利用金属钠与 可利用金属钠与 的水溶液发生置换反应制备 的水溶液发生置换反应制备 |
您最近一年使用:0次
8 . 化学性质类似 的盐酸羟胺(
的盐酸羟胺( )是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是

 的盐酸羟胺(
的盐酸羟胺( )是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有
)是一种常见的还原剂和显像剂。工业上主要采用图1所示的方法制备,其电池装置中含Fe的催化电极反应机理如图2所示。图3是用图1的电池电解处理含有 、
、 的酸性废水的装置。下列说法正确的是
的酸性废水的装置。下列说法正确的是
| A.图1电池工作时,Pt电极是正极 |
B.图2中,A为 和 和 ,B为 ,B为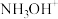 |
C.电极b接电源负极,处理 ,酸性废水中 ,酸性废水中 减少 减少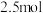 |
D.电池工作时,每消耗 (标准状况下),左室溶液质量增加 (标准状况下),左室溶液质量增加 |
您最近一年使用:0次
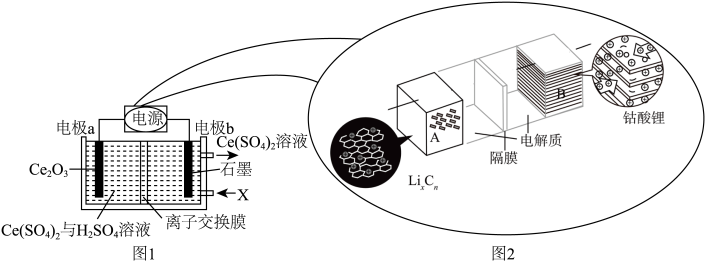
9 . 用废料Ce2O3制备Ce(SO4)2的工作原理示意图如图1所示[电源为可充电锂离子电池,该电池放电时的反应为 ]。下列说法错误的是
]。下列说法错误的是
 ]。下列说法错误的是
]。下列说法错误的是
| A.图1中的离子交换膜为阳离子交换膜 |
B.图2装置充电时,电极B的电极反应式为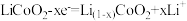 |
| C.图1装置工作一段时间后,电极a区溶液的质量减小 |
| D.锂离子电池电动汽车可有效减少光化学烟雾污染 |
您最近一年使用:0次
2023-05-18更新
|
287次组卷
|
2卷引用:广东省部分学校2023届高三5月联合考试化学试题
名校
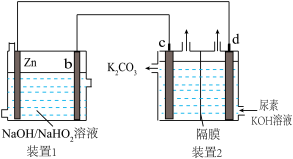
10 . 目前研究较多的Zn-H2O2电池,其电池总反应为Zn+OH-+HO =ZnO
=ZnO +H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
+H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
 =ZnO
=ZnO +H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
+H2O。现以Zn-H2O2电池电解尿素[CO(NH2)2]碱性溶液制备氢气,同时获得N2及极少量O2(装置2中隔膜仅阻止气体通过,b、c、d均为惰性电极)。下列说法错误的是
| A.装置1中OH-移向Zn电极 |
| B.反应过程中,d极附近的pH增大 |
C.电极c的主要反应式为CO(NH2)2-6e-+8OH-=CO +N2+6H2O +N2+6H2O |
| D.通电一段时间后,若Zn电极的质量减轻19.5g,则c电极产生N22.24L(标准状况) |
您最近一年使用:0次



