1 . 利用下列装置和试剂进行实验,能达到实验目的的是
A.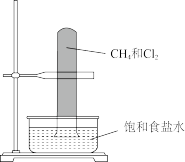 甲烷与氯气暗处发生取代反应 甲烷与氯气暗处发生取代反应 |
B. 比较Zn与Cu的金属性 比较Zn与Cu的金属性 |
C. 蒸干FeCl3溶液,制备无水FeCl3固体 蒸干FeCl3溶液,制备无水FeCl3固体 |
D.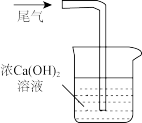 实验室处理尾气SO2 实验室处理尾气SO2 |
您最近一年使用:0次
2022-08-16更新
|
204次组卷
|
2卷引用:重庆市巴蜀中学2023届高三第一次高考适应性月考化学试题
2 . 用如图所示装置进行相应实验,能达到实验目的的是
| 选项 | A | B | C | D |
| 装置 | 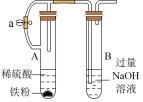 |  | 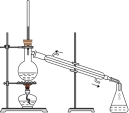 | 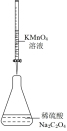 |
| 目的 | 制取 沉淀 沉淀 | 将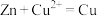 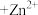 设计成原电池装置 设计成原电池装置 | 分离苯和硝基苯 | 测定 溶液的物质的量浓度 溶液的物质的量浓度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-05-18更新
|
1279次组卷
|
4卷引用:青海省西宁市城西区青海师范大学附属实验中学2022-2023学年高二上学期12月月考化学试题
青海省西宁市城西区青海师范大学附属实验中学2022-2023学年高二上学期12月月考化学试题 湖北省2022届高三5月联考化学试题(已下线)专题11 化学实验基础-三年(2020-2022)高考真题分项汇编吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题
3 . 利用如图装置可以测定铜锌原电池工作时转移电子的物质的量,假设量筒的量程足够大,锌片和铜片中无杂质,气体积已转换为标准状况。下列说法正确的是
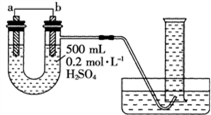

| A.a电极的电极材料是铜 |
| B.如果将稀硫酸换为CuSO4溶液,则不能达到实验目的 |
| C.锌与稀硫酸反应时放出的热量对实验测定不产生影响 |
| D.若量筒中收集到aLH2,则电解质溶液中通过了a/11.2mol电子 |
您最近一年使用:0次
2017-06-13更新
|
305次组卷
|
3卷引用:甘肃省天水市第一中学2016-2017学年高一下学期第二次月考(B卷)化学试题
名校
4 . I.为了探究原电池的工作原理,某研究性学习小组进行了如下实验。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。_______ (填字母)。
A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极_______ (填实验现象),其对应的电极反应式为_______ 。
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
Ⅱ.化学反应 的能量变化如图所示。
的能量变化如图所示。_______ (填“能”或“不能”)将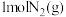 和
和 全部转化为
全部转化为 。
。
(4)该反应属于_______ (填“吸热”或“放热”)反应。
(5)一定量的 和
和 充分反应生成
充分反应生成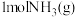 时,释放
时,释放_______  能量。
能量。
(1)按下图中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。

A.甲中锌片是原电池的负极,乙中铜片是原电池的正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向

D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(2)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______。
A.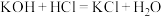 |
B. |
C. |
D.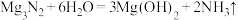 |
Ⅱ.化学反应
 的能量变化如图所示。
的能量变化如图所示。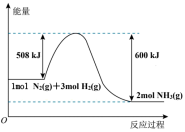
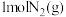 和
和 全部转化为
全部转化为 。
。(4)该反应属于
(5)一定量的
 和
和 充分反应生成
充分反应生成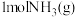 时,释放
时,释放 能量。
能量。
您最近一年使用:0次
名校
解题方法
5 . 人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。请根据题中提供的信息,回答下列问题:
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_______(填字母,下同)。
(2)为了探究原电池的工作原理,某研究性学习小组进行了如下实验。分别按图1中甲、乙所示装置进行实验,甲中两个烧杯中的溶液为同浓度的稀硫酸。_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是_______ 。
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极_______ (填实验现象),其对应的电极反应式为_______ 。
(3)某氢氧燃料电池装置如图所示,a、b均为惰性电极。_______ (填“A”或“B”)口通入。
②负极上的电极反应式为_______ ,当电路中转移 电子时,理论上负极通入的气体在标准状况下的体积为
电子时,理论上负极通入的气体在标准状况下的体积为_______ L。
(1)直接提供电能的反应一般是放热反应,下列反应能设计成原电池的是_______(填字母,下同)。
A. 与 与 反应 反应 | B.氢氧化钠与稀盐酸反应 |
C.灼热的炭与 反应 反应 | D. 与 与 燃烧反应 燃烧反应 |
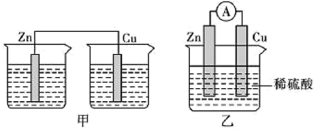
A.甲中锌片是负极,乙中铜片是正极
B.两装置中铜片表面均有气泡产生
C.乙的外电路中电流方向Cu→Zn
D.如果将装置乙中锌片换成铁片,则电路中的电流方向不变
②在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是
③在乙实验中,如果把硫酸换成硫酸铜溶液,可观察到正极
(3)某氢氧燃料电池装置如图所示,a、b均为惰性电极。
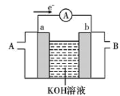
②负极上的电极反应式为
 电子时,理论上负极通入的气体在标准状况下的体积为
电子时,理论上负极通入的气体在标准状况下的体积为
您最近一年使用:0次
名校
解题方法
6 . 下列各实验的方案设计、现象及结论都正确的是
| 选项 | 实验 | 现象 | 结论 |
| A | 将少量Fe(NO3)2加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成红色 | Fe(NO3)2不一定变质 |
| B | 镁、铝为电极,氢氧化钠为电解质的原电池装置 | 铝表面有气泡 | 金属活动性:Mg>Al |
| C | 向待测液中滴加浓氢氧化钠溶液并加热 | 产生使湿润蓝色石蕊试纸变红的气体 | 待测液中含有 |
| D | 将灼热的木炭加入到浓硝酸中 | 有红棕色气体产生 | 木炭在加热时能与浓硝酸发生反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中正极的电极反应式是__________________ 。
(2)装置乙中正极的电极反应式是__________________ 。
(3)装置丙中负极的电极反应是__________________ 。
(4)四种金属活泼性的强弱顺序是__________________ 。
(5)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。下列说法正确的是____ (填序号)。
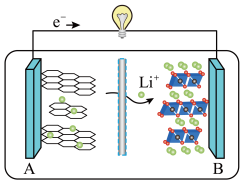
①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
(6) 是一种大气污染物。工业尾气中含有
是一种大气污染物。工业尾气中含有 ,会造成严重的环境污染;未脱除
,会造成严重的环境污染;未脱除 的煤气,运输过程中还会腐蚀管道。干法氧化铁脱硫是目前除去煤气中
的煤气,运输过程中还会腐蚀管道。干法氧化铁脱硫是目前除去煤气中 的常用方法,其原理如图所示。
的常用方法,其原理如图所示。
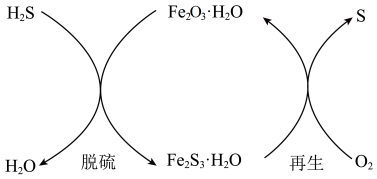
脱硫反应___________ 。再生过程中反应___________________ 。
| 装置 | 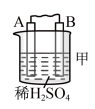 |  |  |
| 现象 | A上有气体产生 | B的质量增加 | 二价金属A不断溶解 |
(1)装置甲中正极的电极反应式是
(2)装置乙中正极的电极反应式是
(3)装置丙中负极的电极反应是
(4)四种金属活泼性的强弱顺序是
(5)2019年诺贝尔化学奖授予对锂离子电池研究做出突出贡献的科学家。某锂离子电池的工作原理如下。下列说法正确的是

①A为电池的正极
②该装置实现了化学能转化为电能
③电池工作时,电池内部的锂离子定向移动
(6)
 是一种大气污染物。工业尾气中含有
是一种大气污染物。工业尾气中含有 ,会造成严重的环境污染;未脱除
,会造成严重的环境污染;未脱除 的煤气,运输过程中还会腐蚀管道。干法氧化铁脱硫是目前除去煤气中
的煤气,运输过程中还会腐蚀管道。干法氧化铁脱硫是目前除去煤气中 的常用方法,其原理如图所示。
的常用方法,其原理如图所示。
脱硫反应
您最近一年使用:0次
8 . 应用电化学原理,回答下列问题:
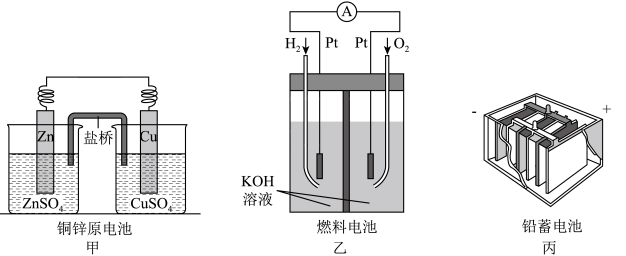
(1)上述三个装置中,负极反应的共同特点是_____________________ 。
(2)甲电池工作时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是________________ 。
(3)乙中正极反应式为____________________ ;若将H2换成CH4,则负极反应式为______________________ 。
(4)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池______ 极相连接。
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按右图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
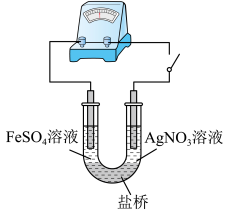
a.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
b.随后向U型管左侧逐渐加入浓Fe2(SO4)3溶液,发现电流计指针的变化依次为:偏移减小→回到零点→逆向偏移。
① 实验a中银作_________ 极。
② 综合实验a和b的现象,得出Ag+和Fe2+反应的离子方程式是_____________________ 。

(1)上述三个装置中,负极反应的共同特点是
(2)甲电池工作时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是
(3)乙中正极反应式为
(4)丙中铅蓄电池放电一段时间后,进行充电时,要将外接电源的负极与铅蓄电池
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按右图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:

a.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
b.随后向U型管左侧逐渐加入浓Fe2(SO4)3溶液,发现电流计指针的变化依次为:偏移减小→回到零点→逆向偏移。
① 实验a中银作
② 综合实验a和b的现象,得出Ag+和Fe2+反应的离子方程式是
您最近一年使用:0次
名校
9 . 完成下列问题。
(1)下列反应中,属于放热反应的是___________ (填字母,下同),属于吸热反应的是___________ 。
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
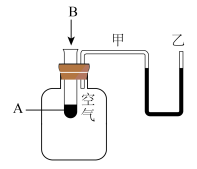
试回答下列问题:
①该反应为___________ 反应(填“放热”或“吸热”)。
②该反应的反应物化学键断裂吸收的能量________ (填“高”或“低”)于生成物化学键形成放出的能量。
(3) A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
①装置甲溶液中的阴离子移向________ (填“A”或“B”)极。
②装置乙中正极的电极反应式为________ 。
③四种金属活动性由强到弱的顺序是________ 。
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:
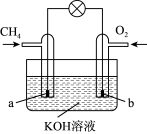
①外电路电子移动方向:___________ (填“a极到b极”或“b极到a极”)。
②a电极的电极方程式为___________ 。
(1)下列反应中,属于放热反应的是
a.盐酸与烧碱溶液反应 b.Ba(OH)2·8H2O+2NH4Cl=BaCl2+10H2O+2NH3↑
c.氢气在氧气中燃烧生成水 d.高温煅烧石灰石使其分解
e.铝和盐酸反应 f.葡萄糖在人体内氧化分解
(2)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。

试回答下列问题:
①该反应为
②该反应的反应物化学键断裂吸收的能量
(3) A、B、C、D四种金属按下表中装置进行实验。
| 装置 | 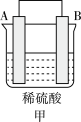 |  |  |
| 现象 | 金属A不断溶解 | C的质量增加 | A上有气体产生 |
①装置甲溶液中的阴离子移向
②装置乙中正极的电极反应式为
③四种金属活动性由强到弱的顺序是
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如下图所示:

①外电路电子移动方向:
②a电极的电极方程式为
您最近一年使用:0次
名校
解题方法
10 . 实验小组探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
【实验1】
(1)实验1中,电解质溶液为盐酸,镁条做原电池的___________ 极。
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为___________ 。
实验2实际获得的现象如下:
(3)ⅰ中铝条表面放电的物质是溶解在溶液中的O2,则该电极反应式为___________ 。
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是___________ 。
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
(5)根据实验3和实验4可获得的正确推论是___________(填字母序号)。
(6)由实验1~实验4可推知,铝片做电极材料时的原电池反应与___________ 等因素有关。
【实验1】
| 装置 | 实验现象 |
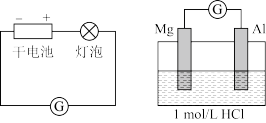 | 左侧装置电流计指针向右偏转,灯泡亮 右侧装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验2】将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为
 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为实验2实际获得的现象如下:
| 装置 | 实验现象 |
 | ⅰ.电流计指针迅速向右偏转,镁条表面无气泡,铝条表面有气泡 ⅱ.电流计指针逐渐向零刻度恢复,经零刻度后继续向左偏转。镁条表面开始时无明显现象,一段时间后有少量气泡逸出,铝条表面持续有气泡逸出 |
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
| 编号 | 装置 | 实验现象 |
| 实验3 | 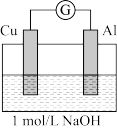 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| 实验4 | 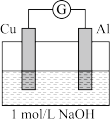 煮沸冷却后的溶液 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象:约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| A.上述两装置中,开始时铜片表面得电子的物质是O2 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
| C.铜片表面产生的气泡为H2 |
| D.由“铝条表面气泡略有减少”能推测H+在铜片表面得电子 |
您最近一年使用:0次
2023-10-24更新
|
217次组卷
|
3卷引用:北京市清华大学附属中学2023-2024学年高二上学期(G22级)统练二化学试题



