名校
1 . 回答下列问题
(1)已知完全燃烧ag乙炔(C2H2)气体时生成1molCO2和H2O(l),同时放出热量bkJ,则表示乙炔燃烧热的热化学方程式:_____ 。
(2)某课外科学兴趣小组的同学用如图所示装置研究有关电化学的问题。图中是两个串联的甲烷燃料电池做电源对乙池丙池进行电解实验(各溶液溶质均足量),当闭合该装置的电键时,观察到电流表的指针发生了偏转。

①A电极上发生的电极反应式为:____ 。
②电解过程中丙池中发生的总反应方程式为:____ 。
③当两个燃料电池共消耗甲烷2240mL(标况),乙池中某极上析出Ag的质量为_____ g。
(3)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

若以此新型电池为电源,用惰性电极电解制备硼酸[H3BO3或B(OH)3],其工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。

①新型电池放电时,负极电极反应式为:____ 。
②两池工作时,电池的电极M应与电解池的____ (填a或b)极相连接;1、2、3膜为阳膜的是:____ 。
③产品室中发生的离子反应为:____ 。
(1)已知完全燃烧ag乙炔(C2H2)气体时生成1molCO2和H2O(l),同时放出热量bkJ,则表示乙炔燃烧热的热化学方程式:
(2)某课外科学兴趣小组的同学用如图所示装置研究有关电化学的问题。图中是两个串联的甲烷燃料电池做电源对乙池丙池进行电解实验(各溶液溶质均足量),当闭合该装置的电键时,观察到电流表的指针发生了偏转。

①A电极上发生的电极反应式为:
②电解过程中丙池中发生的总反应方程式为:
③当两个燃料电池共消耗甲烷2240mL(标况),乙池中某极上析出Ag的质量为
(3)如图所示是一种可实现氢气循环利用的新型电池的放电工作原理。

若以此新型电池为电源,用惰性电极电解制备硼酸[H3BO3或B(OH)3],其工作原理如图所示(阳膜和阴膜分别只允许阳离子和阴离子通过)。

①新型电池放电时,负极电极反应式为:
②两池工作时,电池的电极M应与电解池的
③产品室中发生的离子反应为:
您最近一年使用:0次
2022-10-08更新
|
475次组卷
|
2卷引用:河北省邢台市六校2022-2023学年高三上学期第一次月考化学试题
名校
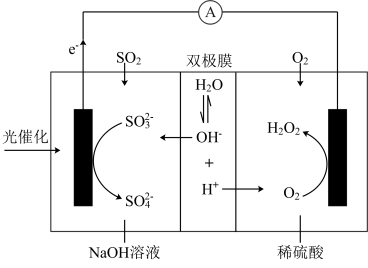
2 . 我国科研人员将单独脱除SO2的反应与H2O2的制备反应相结合,实现协同转化。
①单独制备H2O2:2H2O+O2=2H2O2,不能自发进行
②单独脱除SO2:4OH-+2SO2+O2=2SO +2H2O,能自发进行协同转化装置如图所示,在电场作用下,双极膜中间层的H2O解离为OH-和H+,并向两极迁移。下列叙述错误的是
+2H2O,能自发进行协同转化装置如图所示,在电场作用下,双极膜中间层的H2O解离为OH-和H+,并向两极迁移。下列叙述错误的是
①单独制备H2O2:2H2O+O2=2H2O2,不能自发进行
②单独脱除SO2:4OH-+2SO2+O2=2SO
 +2H2O,能自发进行协同转化装置如图所示,在电场作用下,双极膜中间层的H2O解离为OH-和H+,并向两极迁移。下列叙述错误的是
+2H2O,能自发进行协同转化装置如图所示,在电场作用下,双极膜中间层的H2O解离为OH-和H+,并向两极迁移。下列叙述错误的是
A.负极区域存在反应为SO2+2OH-= +H2O +H2O |
| B.双极膜中间层的H2O的解离可不断提供OH-和H+,故不需要补加H2SO4 |
| C.协同转化总反应为SO2+O2+2NaOH=H2O2+Na2SO4 |
| D.当正极生成1molH2O2时,负极区域的溶液质量增重64g |
您最近一年使用:0次
2022-09-30更新
|
332次组卷
|
3卷引用:湖南省湖湘名校教育联合体2023届高三上学期9月大联考化学试题
名校
解题方法
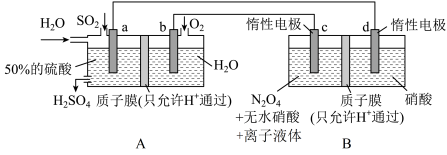
3 . 硝化剂可在化学反应中向有机化合物中引入硝基、硝酸酯基 是一种绿色硝化剂。有人设想利用工业废气
是一种绿色硝化剂。有人设想利用工业废气 ,依据电化学原理制备
,依据电化学原理制备 和
和 。装置图如下,下列说法
。装置图如下,下列说法不正确 的是
 是一种绿色硝化剂。有人设想利用工业废气
是一种绿色硝化剂。有人设想利用工业废气 ,依据电化学原理制备
,依据电化学原理制备 和
和 。装置图如下,下列说法
。装置图如下,下列说法
A.装置 可将电能转化为化学能 可将电能转化为化学能 |
B.装置 中H从a极区迁移到b极区 中H从a极区迁移到b极区 |
C.c电极表面生成 ,电极反应式为: ,电极反应式为: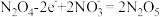 |
D.反应过程中 装置d区 装置d区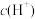 保持不变 保持不变 |
您最近一年使用:0次
2023-10-13更新
|
410次组卷
|
2卷引用:湖北省重点高中智学联盟2023-2024学年高三上学期10月联考化学试题
名校
解题方法
4 . 电化学原理在能量转化,物质制备及环境保护等领域均有广泛应用,请按要求回答下列问题:
一种以液态肼(N2H4)为燃料的电池装置如图甲所示,该电池用KOH溶液作为电解质溶液。以该燃料电池作为电源电解足量的饱和CuSO4溶液以实现向铁棒上镀铜,装置如图乙所示。
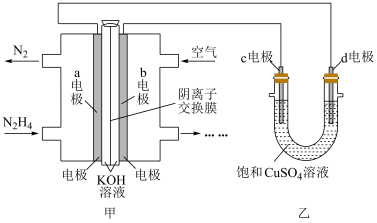
(1)b电极为燃料电池的_______ 极(填“ 正”或“负”)。a电极反应式为_______________ ,c电极应选用的电极材料为_____ (填“铁”或“铜” ) 。若c、d电极均为惰性电极,则c电极反应式应为_____________________________ ,装置乙总反应为___________________
氰化物有剧毒,在含氰工业废水排放前,需要对其进行治理。在碱性条件下利用电解法除去废水中的氯化物(以CN- 代表),装置如图丙,已知石墨电极上依次发生的部分反应有:
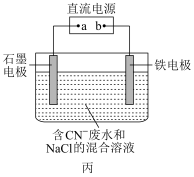
a.CN-+ 2OH--2e -=CNO- + H2O
b.2Cl--2e- = Cl2↑
c.3Cl2+ 2CNO -+ 8OH-=N2↑+6C1-+ 2CO + 4H2O
+ 4H2O
(2)铁电极上发生的电极反应为__________________
(3)忽略铁电极上的其他反应,电解一段时间后,相同条件下在石墨电极处测得产生N2 a mL,同时在铁电极处产生气体b mL,则氰去除率为_______ (氰去除率= 100%)
100%)
一种以液态肼(N2H4)为燃料的电池装置如图甲所示,该电池用KOH溶液作为电解质溶液。以该燃料电池作为电源电解足量的饱和CuSO4溶液以实现向铁棒上镀铜,装置如图乙所示。

(1)b电极为燃料电池的
氰化物有剧毒,在含氰工业废水排放前,需要对其进行治理。在碱性条件下利用电解法除去废水中的氯化物(以CN- 代表),装置如图丙,已知石墨电极上依次发生的部分反应有:

a.CN-+ 2OH--2e -=CNO- + H2O
b.2Cl--2e- = Cl2↑
c.3Cl2+ 2CNO -+ 8OH-=N2↑+6C1-+ 2CO
 + 4H2O
+ 4H2O(2)铁电极上发生的电极反应为
(3)忽略铁电极上的其他反应,电解一段时间后,相同条件下在石墨电极处测得产生N2 a mL,同时在铁电极处产生气体b mL,则氰去除率为
 100%)
100%)
您最近一年使用:0次
名校
解题方法
5 . 盐酸羟胺(NH2OH⋅HCl)在水中完全电离为NH3OH+和Cl−,可利用如下装置来制备盐酸羟胺。以盐酸为离子导体,向两电极分别通入NO和H2。下列说法正确的是
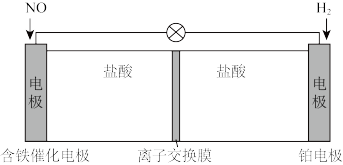

| A.铂电极为正极 |
| B.离子交换膜为阴离子交换膜,Cl−从左室移向右室 |
| C.含铁催化电极上的反应为:NO+3e−+4H+=NH3OH+ |
| D.每生成1mol盐酸羟胺电路中转移4mol e− |
您最近一年使用:0次
2022-11-28更新
|
212次组卷
|
3卷引用:重庆2023届拔尖强基联合11月定时检测化学试题
2014高三·全国·专题练习
名校
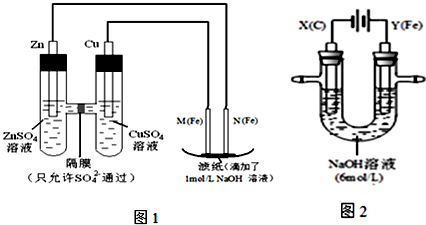
6 . 某课外小组分别用下图所示装置对原电池和电解原理进行实验探究.
请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是______ (填字母序号).
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为_____________ .
(3)实验过程中,SO42-______ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有______________ .
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH______ (填“增大”、“减小”或“不变”).
(5)电解过程中,Y极发生的电极反应为_____________ 和4OH- - 4e-= 2H2O + O2↑
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______ g.
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为__________ .

请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为
(3)实验过程中,SO42-
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为
您最近一年使用:0次
2017-06-17更新
|
606次组卷
|
7卷引用:河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题
河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题(已下线)2014届高考化学二轮专题复习 电化学练习卷(已下线)2014高考名师推荐化学电解规律及电化学计算北京市2017届高三高考押题卷化学试题2020届高考化学二轮复习大题精准训练 ——原电池、电解池填空题辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题
解题方法
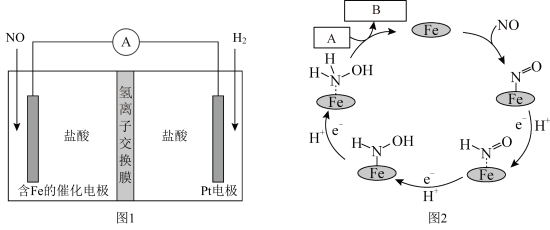
7 . 盐酸羟胺(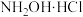 )是一种无机物,可用作合成抗癌药,其化学性质类似
)是一种无机物,可用作合成抗癌药,其化学性质类似 。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
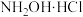 )是一种无机物,可用作合成抗癌药,其化学性质类似
)是一种无机物,可用作合成抗癌药,其化学性质类似 。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
| A.该装置能将电能转化为化学能,Pt电极为阳极 |
B.图2中,A为 ,B为 ,B为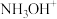 |
C.每制取0.1mol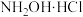 ,有3.36L(标准状况) ,有3.36L(标准状况) 参与反应 参与反应 |
| D.电池工作一段时间后,正极区溶液的pH下降 |
您最近一年使用:0次
8 . 回答下列问题
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是_______ 。(填“A”或“B”)

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
则生成1mol水可以放出热量 _______ kJ
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:_______ (填序号)。
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中 向铜片方向移动
向铜片方向移动
②乙中能量转化的主要形式为_______ 。
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是_______ ,当电路中转移0.25 mol电子时,消耗负极材料的质量为_______ g。
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
| 化学键 | H-H | O=O | H-O |
| 键能kJ/mol | 436 | 496 | 463 |
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中
 向铜片方向移动
向铜片方向移动②乙中能量转化的主要形式为
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是
您最近一年使用:0次
名校
解题方法
9 . Ⅰ.回答下列问题
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:
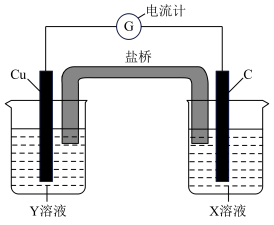
①写出电极反应式。正极:_______ ;负极:_______ 。
②图中X溶液的溶质是_______ (填化学式,下同),Y溶液的溶质是_______ 。
③原电池工作时,盐桥中的_______ (填“阳”或“阴”)离子向X溶液方向移动。
(2)控制合适的条件将反应2Fe3++2I-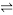 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:

①反应开始时,乙中石墨电极上发生_______ (填“氧化”或“还原”,下同)反应,电极反应式为_______ 。甲中石墨电极上发生_______ 反应,电极反应式为_______ 。
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作_______ (填“正”或“负”)极,该电极的电极反应式为_______ 。
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为_______ 。
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式_______ 。实验结果未见到蓝色。
(5)乙同学认为甲同学的实验方案有问题,理由是_______ 。请设计原电池证明Ag+也能氧化 Iˉ,画出装置图,并标明电极材料及电解质溶液。______
(1)利用反应Cu+2FeCl3=CuCl2+2FeCl2,设计成如图所示的原电池,回答下列问题:

①写出电极反应式。正极:
②图中X溶液的溶质是
③原电池工作时,盐桥中的
(2)控制合适的条件将反应2Fe3++2I-
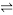 2Fe2++I2设计成如图所示的原电池。请回答下列问题:
2Fe2++I2设计成如图所示的原电池。请回答下列问题:
①反应开始时,乙中石墨电极上发生
②电流计读数为0时,反应达到平衡状态,此时在甲中加入FeCl2固体,则乙中的石墨作
(3)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,其正极电极反应式为
Ⅱ.已知:①将 0.1 mol·Lˉ1KI 溶液加入到 0.1 mol·L-1 FeCl3溶液中时,可以看到溶液颜色加深,滴加淀粉后溶液变为蓝色;
②当离子浓度相同时,氧化性:Ag+>Fe3+;
③ 若浓度减小时,离子的氧化性也会随之减弱。
(4)甲同学猜测,0.1 mol·Lˉ1 KI 溶液(加入几滴淀粉溶液)加入0.1mol·Lˉ1AgNO3 溶液中时,溶液应变蓝色。请写出该猜测对应的离子方程式
(5)乙同学认为甲同学的实验方案有问题,理由是
您最近一年使用:0次
解题方法
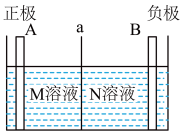
10 . 某实验小组用铜和 溶液来制备
溶液来制备 溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
 溶液来制备
溶液来制备 溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
| A.电极A为铜 |
B.a为阴离子交换膜,电解质N为 |
| C.理论上每生成1molN时会消耗1molM |
| D.当B电极质量减少6.4克,则N溶液质量增加6.4克 |
您最近一年使用:0次
2022-08-18更新
|
167次组卷
|
2卷引用:贵州省思南县梵净山中学2022-2023学年高三上学期11月月考化学试题



