1 . Ⅰ.由A、B、C、D四种金属按下表中装置进行实验。
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是_______ 。
(2)装置乙中正极的电极反应式是_______ 。
(3)装置丙中溶液的pH变化是_______ 。
(4)四种金属活动性由强到弱的顺序是_______ 。
Ⅱ.今有下列物质:
①甲烷 ②乙烷 ③乙烯 ④苯 ⑤苯乙烯 ⑥分馏汽油
(5)常温下呈气态的是_______ 。
(6)属于芳香烃的是_______ 。
(7)能与溴水反应而使溴水褪色的是_______ ,由于萃取作用而使溴水褪色的是_______ 。
(8)能使酸性高锰酸钾溶液褪色的是_______ 。
| 装置 | 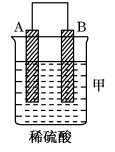 | 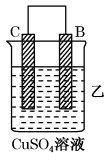 | 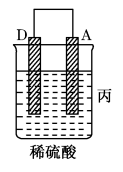 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是
(2)装置乙中正极的电极反应式是
(3)装置丙中溶液的pH变化是
(4)四种金属活动性由强到弱的顺序是
Ⅱ.今有下列物质:
①甲烷 ②乙烷 ③乙烯 ④苯 ⑤苯乙烯 ⑥分馏汽油
(5)常温下呈气态的是
(6)属于芳香烃的是
(7)能与溴水反应而使溴水褪色的是
(8)能使酸性高锰酸钾溶液褪色的是
您最近一年使用:0次
解题方法
2 . 将锌片和铜片用导线连接后插入稀硫酸中,并在中间串联一个电流表,装置如图所示。
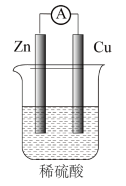
(1)该装置可以将_______ 能转化为_______ 能。
(2)装置中的负极材料是_______ 。
(3)铜片上的电极反应式是_______ ,该电极上发生了_______ (填“氧化”或“还原”)反应。
(4)稀硫酸中的SO 向
向_______ 片移动。导线中电子流向_______ 片。
(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为_______ 。

(1)该装置可以将
(2)装置中的负极材料是
(3)铜片上的电极反应式是
(4)稀硫酸中的SO
 向
向(5)若将电解质溶液换成CuSO4溶液,则正极上的实验现象为
您最近一年使用:0次
名校
解题方法
3 . 由A、B、C、D四种金属按表中装置进行实验,下列叙述中正确的是
| 实验装置 | 甲 | 乙 | 丙 |
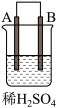 | 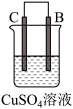 | 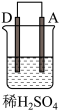 | |
| 现象 | A不断溶解 | C的质量增加 | A上有气体产生 |
| A.装置甲中的B金属是原电池的负极 | B.装置乙中电流的流向为B→C |
C.装置丙中溶液里的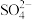 移向A 移向A | D.四种金属的活泼性顺序是D>A>B>C |
您最近一年使用:0次
4 . 应用电化学原理,回答下列问题:

(1)上述三个装置中,负极反应物化学性质上的共同特点是___________ 。
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是___________ 。
(3)乙中正极反应式为___________ ;若将 换成
换成 ,则负极反应式为
,则负极反应式为___________ 。
(4)丙中正极的电极反应式为___________ 。
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U型管左侧逐渐加入浓 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
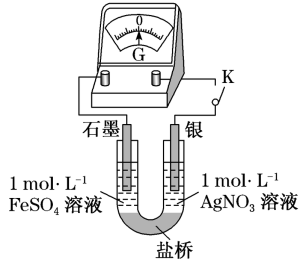
①实验ⅰ中银作___________ 极。
②综合实验ⅰ、ⅱ的现象,得出 和
和 反应的离子方程式是
反应的离子方程式是___________

(1)上述三个装置中,负极反应物化学性质上的共同特点是
(2)甲中电流计指针偏移时,盐桥(装有含琼胶的KCl饱和溶液)中离子移动的方向是
(3)乙中正极反应式为
 换成
换成 ,则负极反应式为
,则负极反应式为(4)丙中正极的电极反应式为
(5)应用原电池反应可以探究氧化还原反应进行的方向和程度。按下图连接装置并加入药品(盐桥中的物质不参与反应),进行实验:
ⅰ.K闭合时,指针偏移。放置一段时间后,指针偏移减小。
ⅱ.随后向U型管左侧逐渐加入浓
 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
①实验ⅰ中银作
②综合实验ⅰ、ⅱ的现象,得出
 和
和 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
2022-12-02更新
|
326次组卷
|
2卷引用:北京市第二中学2022-2023学年高二上学期11月月考化学试题
名校
解题方法
5 . 某小组同学为探究 和
和 反应的程度,进行以下实验。已知:相关物质的
反应的程度,进行以下实验。已知:相关物质的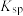 (25℃) AgCl:
(25℃) AgCl:
 :
:
(1)甲同学的实验如下:
注:经检验黑色固体为Ag。
①白色沉淀的化学式是___________ 。
②甲同学得出 氧化了
氧化了 的依据是
的依据是___________ 。
(2)乙同学为探究 和
和 反应的程度,进行实验Ⅱ。
反应的程度,进行实验Ⅱ。
a.按下图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。
偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
b.随后向甲烧杯中逐渐加入浓 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
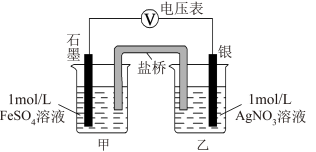
①a中甲烧杯里的电极反应式是___________ 。
②b中电压表指逆向偏移后,银为极___________ (填“正”或“负”)。
③由实验得出 和
和 反应的离子方程式是
反应的离子方程式是___________ 。
 和
和 反应的程度,进行以下实验。已知:相关物质的
反应的程度,进行以下实验。已知:相关物质的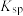 (25℃) AgCl:
(25℃) AgCl:
 :
:
(1)甲同学的实验如下:
序号 | 操作 | 现象 |
实验1 | 将2mL | 产生白色沉淀,随后有黑色固体产生 |
取上层清液,滴加KSCN溶液 | 溶液变红 |
①白色沉淀的化学式是
②甲同学得出
 氧化了
氧化了 的依据是
的依据是(2)乙同学为探究
 和
和 反应的程度,进行实验Ⅱ。
反应的程度,进行实验Ⅱ。a.按下图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。
偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
b.随后向甲烧杯中逐渐加入浓
 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
①a中甲烧杯里的电极反应式是
②b中电压表指逆向偏移后,银为极
③由实验得出
 和
和 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
2022-12-04更新
|
130次组卷
|
2卷引用:广东省江门市第一中学2022-2023学年高二上学期第二次月考化学试题
名校
6 . I.如图所示,某同学设计了一个燃料电池并进行电解实验,请回答下列问题:

(1)甲池中通____ (填“氧气”或“甲烷”)的是负极,其电极反应式为____ 。
(2)标准状况下,若有2.24L氧气参加反应,则乙装置中铁电极上生成气体的物质的量为____ mol。
(3)丙池中铜片上可观察到的现象为____ 。
II.据报道,我国已研制出“可充室温钠-二氧化碳电池”,如图所示,该电池的工作原理为4Na+3CO2 Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。

(4)放电时,钠箔为该电池的____ 极(填“正”或“负”):电解质溶液中ClO 流向
流向____ (填“钠箔”或“多壁碳纳米管”)电极。
(5)充电时,多糖碳纳米管连接直流电源的____ (填“正”或“负”)极,其电极反应式为____ 。

(1)甲池中通
(2)标准状况下,若有2.24L氧气参加反应,则乙装置中铁电极上生成气体的物质的量为
(3)丙池中铜片上可观察到的现象为
II.据报道,我国已研制出“可充室温钠-二氧化碳电池”,如图所示,该电池的工作原理为4Na+3CO2
 Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
Na2CO3+C(放电时产生的Na2CO3固体贮存于多壁碳纳米管中)。
(4)放电时,钠箔为该电池的
 流向
流向(5)充电时,多糖碳纳米管连接直流电源的
您最近一年使用:0次
7 . 某科学探究小组为探究电化学原理, 设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述错误的是
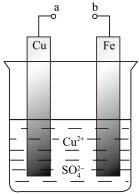

| A.a和b不连接时,铁片上有红色的铜析出 |
| B.a和b用导线连接时, 铜片为负极 |
| C.无论a和b是否连接,反应的本质相同,铁片均会被氧化,溶液中均有Fe2+生成 |
| D.a和b用导线连接时,溶液中的Cu2+应向铜电极移动且能更快地在铜电极上析出铜 |
您最近一年使用:0次
8 . 化学电源广泛地应用于现代社会的生产和生活。请回答下列问题:
(1)原电池是一种化学能转变为电能的装置,所以原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
(2)化学反应均涉及相应的能量变化,为探究这些能量变化,某同学设计了如图两个实验,已知两个实验除了是否有导线连接两个金属棒外,其余均相同。

①该同学设计这两个实验的目的是___________ 。
②有关反应一段时间后的实验现象,下列说法正确的是___________ ( 填字母)。
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温。
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(3)若将用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为___________ ,工作时间内装置所产生氢气的体积为 ___________ L(标准状况)。
(1)原电池是一种化学能转变为电能的装置,所以原电池的设计原理与某类化学反应有关。你认为下列化学反应,可以设计成原电池的是___________(填字母)。
| A.CaO+H2O=Ca(OH)2 |
B.C+CO2 2CO 2CO |
| C.NaOH+HCl=NaCl+H2O |
| D.2FeCl3+Cu=2FeCl2+CuCl2 |

①该同学设计这两个实验的目的是
②有关反应一段时间后的实验现象,下列说法正确的是
A.图1中温度计的示数高于图2的示数
B.图1和图2中温度计的示数相等,且均高于室温。
C.图1和图2的气泡均产生于锌棒表面
D.图2中产生气体的速率比1慢
(3)若将用导线相连在一起,总质量为80.00 g的锌片和银片同时浸入稀硫酸中,工作一段时间后,取出金属片,进行洗涤、干燥、称量,得金属片的总质量为63.75 g,则装置工作时锌片上的电极反应式为
您最近一年使用:0次
2022-05-28更新
|
1060次组卷
|
5卷引用:山西省运城市2021-2022学年高一下学期5月联考化学试题
山西省运城市2021-2022学年高一下学期5月联考化学试题山东省济宁市曲阜孔子高级中学2022-2023学年高一下学期4月月考化学试题(已下线)化学(人教版2019B卷)-学易金卷:2022-2023学年高一下学期期中考前必刷卷第六章 化学反应与能量(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)(已下线)第六章 化学反应与能量【单元测试B卷】
解题方法
9 . 某实验小组为探究CuSO4与Na2SO3反应后的产物,做如下探究实验。
【查阅资料】
①Cu2O为砖红色固体,不溶于水;
②Cu2SO3为黄色固体,不溶于水;
③[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃ 2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol∙L-1的Na2SO3溶液中滴加0.2mol∙L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)S元素在元素周期表中的位置为_______ 。N、O、S三种元素原子的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:_______ 。
(3)经检验,实验2所得溶液中有大量 、
、 生成。该实验中Cu2+表现
生成。该实验中Cu2+表现_______ 性,写出该实验中反应的离子方程式:_______ 。
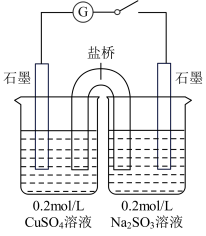
(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做_______ (填“正”或“负”)极,右侧烧杯中发生反应的电极反应式为_______ 。设计实验检验右侧烧杯中生成的阴离子,写出具体操作、现象和结论:_______ 。
【查阅资料】
①Cu2O为砖红色固体,不溶于水;
②Cu2SO3为黄色固体,不溶于水;
③[Cu(SO3)2]3-为无色配合离子、[Cu(NH3)2]+为无色配合离子、[Cu(NH3)4]2+为深蓝色配合离子。
【实验探究】
实验1:①向2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,开始出现黄色沉淀,但无气体产生。
②继续加入Na2SO3溶液,最终沉淀消失。经检验,溶液中生成[Cu(SO3)2]3-离子。
实验2:向90℃ 2mL0.2mol∙L-1的CuSO4溶液中滴加0.2mol∙L-1的Na2SO3溶液,直接生成砖红色沉淀。
实验3:向2mL0.2mol∙L-1的Na2SO3溶液中滴加0.2mol∙L-1的CuSO4溶液,开始阶段有蓝色沉淀出现。
(1)S元素在元素周期表中的位置为
(2)某同学认为实验1黄色沉淀中有少量Cu(OH)2,该同学认为是CuSO4、Na2SO3相互促进水解产生的,用离子方程式表示生成Cu(OH)2沉淀的过程:
(3)经检验,实验2所得溶液中有大量
 、
、 生成。该实验中Cu2+表现
生成。该实验中Cu2+表现(4)某同学设计了如图所示的电化学装置,探究CuSO4与Na2SO3的反应。该装置中左侧烧杯中的石墨电极做

您最近一年使用:0次
名校
解题方法
10 . 实验小组探究铝片做电极材料时的原电池反应,设计下表中装置进行实验并记录。
【实验1】
(1)实验1中,电解质溶液为盐酸,铝条做原电池的___________ 极
【实验2】
将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为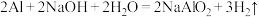 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为___________
实验2实际获得的现象如下:
(3)ⅰ中铝条表面放电的物质足溶解在溶液中的 ,则该电极反应式为
,则该电极反应式为___________
(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是___________
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
(5)根据实验3和实验4可获得的正确推论是___________(填字母序号)
(6)由实验1~实验4可推知,铝片做电极材料时的原电池反应与___________ 等因素有关
【实验1】
| 装置 | 实验现象 |
 | 左侧装置电流计指针向右偏转,灯泡亮 右侧装置电流计指针向右偏转,镁条、铝条表面产生无色气泡 |
【实验2】
将实验1中的电解质溶液换为NaOH溶液进行实验2。
(2)该小组同学认为,此时原电池的总反应为
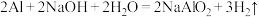 ,据此推测应该出现的实验现象为
,据此推测应该出现的实验现象为实验2实际获得的现象如下:
| 装置 | 实验现象 |
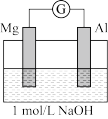 | ⅰ.电流计指针迅速向右偏转,镁条表面无气泡,铝条表面有气泡 ⅱ.电流计指针逐渐向零刻度恢复,经零刻度后继续向左偏转。镁条表面开始时无明显现象,一段时间后有少量气泡逸出,铝条表面持续有气泡逸出 |
 ,则该电极反应式为
,则该电极反应式为(4)ⅱ中“电流计指针逐渐向零刻度恢复”的原因是
【实验3和实验4】
为了排除Mg条的干扰,同学们重新设计装置并进行实验3和实验4,获得的实验现象如下:
| 编号 | 装置 | 实验现象 |
| 实验3 | 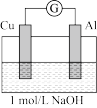 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约10分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
| 实验4 | 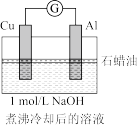 | 电流计指针向左偏转。铝条表面有气泡逸出,铜片没有明显现象;约3分钟后,铜片表面有少量气泡产生,铝条表面气泡略有减少。 |
A.上述两装置中,开始时铜片表面得电子的物质是 |
| B.铜片表面开始产生气泡的时间长短与溶液中溶解氧的多少有关 |
C.铜片表面产生的气泡为 |
D.由“铝条表面气泡略有减少”能推测 在铜片表面得电子 在铜片表面得电子 |
您最近一年使用:0次

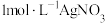 溶液加入到
溶液加入到 溶液中
溶液中

