名校
1 .  具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
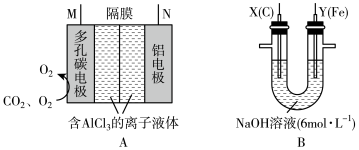
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的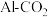 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
(1) 的电子式为
的电子式为___________ 。
(2)图A中正极反应式为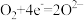 、
、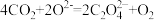 ,则该电池的总反应方程式为
,则该电池的总反应方程式为___________ 。
(3)图A中N极名称是___________ (填“正极”或“负极”),M极与图B___________ (填“X”或“Y”)极相连。
(4)电解过程中,图BX极区溶液的pH___________ (填“增大”“减小”或“不变”)。
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小___________ g。
 具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备
具有强氧化性,能够消毒杀菌,同时能够吸附水中悬浮杂质。可用电解法制备 ,采用的装置如图B所示,以
,采用的装置如图B所示,以 辅助的
辅助的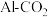 电池(如图A)为电源进行电解。
电池(如图A)为电源进行电解。
(1)
 的电子式为
的电子式为(2)图A中正极反应式为
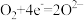 、
、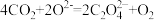 ,则该电池的总反应方程式为
,则该电池的总反应方程式为(3)图A中N极名称是
(4)电解过程中,图BX极区溶液的pH
(5)图B中两极均有气体产生,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况下的气体体积),则Y电极质量减小
您最近一年使用:0次
解题方法
2 . 某实验小组用铜和 溶液来制备
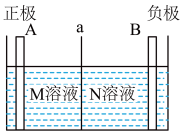
溶液来制备 溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
 溶液来制备
溶液来制备 溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
溶液,同时获得电能,装置如图所示,其中M、N为电解质,下列说法正确的是
| A.电极A为铜 |
B.a为阴离子交换膜,电解质N为 |
| C.理论上每生成1molN时会消耗1molM |
| D.当B电极质量减少6.4克,则N溶液质量增加6.4克 |
您最近一年使用:0次
2022-08-18更新
|
168次组卷
|
2卷引用:贵州省思南县梵净山中学2022-2023学年高三上学期11月月考化学试题
解题方法
3 . 盐酸羟胺(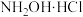 )是一种无机物,可用作合成抗癌药,其化学性质类似
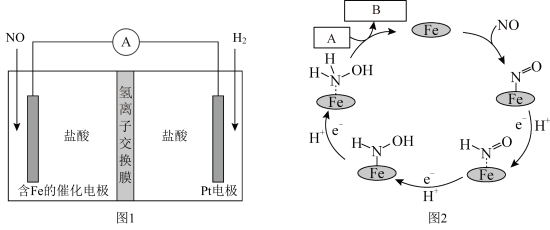
)是一种无机物,可用作合成抗癌药,其化学性质类似 。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
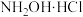 )是一种无机物,可用作合成抗癌药,其化学性质类似
)是一种无机物,可用作合成抗癌药,其化学性质类似 。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
| A.该装置能将电能转化为化学能,Pt电极为阳极 |
B.图2中,A为 ,B为 ,B为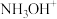 |
C.每制取0.1mol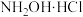 ,有3.36L(标准状况) ,有3.36L(标准状况) 参与反应 参与反应 |
| D.电池工作一段时间后,正极区溶液的pH下降 |
您最近一年使用:0次
4 . 回答下列问题
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是_______ 。(填“A”或“B”)

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
则生成1mol水可以放出热量 _______ kJ
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:_______ (填序号)。
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是_______ (填字母)。
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中 向铜片方向移动
向铜片方向移动
②乙中能量转化的主要形式为_______ 。
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是_______ ,当电路中转移0.25 mol电子时,消耗负极材料的质量为_______ g。
(1)从能量的变化和反应的快慢等角度研究反应:2H2 + O2 = 2H2O。已知该反应为放热反应,如图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如表:
| 化学键 | H-H | O=O | H-O |
| 键能kJ/mol | 436 | 496 | 463 |
(2)以下反应:①木炭与水制备水煤气②氯酸钾分解③炸药爆炸④酸与碱的中和反应⑤生石灰与水作用制熟石灰⑥ Ba(OH)2·8H2O与NH4Cl ⑦气态水液化,属于放热反应的有:
(3)分别按图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中A为电流表。请回答下列问题:

①以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极 B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液pH均增大 D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu F.乙溶液中
 向铜片方向移动
向铜片方向移动②乙中能量转化的主要形式为
③在乙实验中,如果把稀硫酸换成硫酸铜溶液,铜电极的电极反应式是
您最近一年使用:0次
名校
解题方法
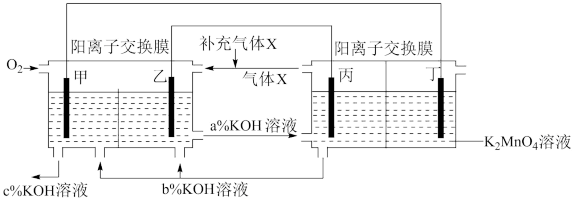
5 . 一种将燃料电池与电解池组合制备 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
 的装置如图所示
的装置如图所示 电极甲、乙、丙、丁均为惰性电极
电极甲、乙、丙、丁均为惰性电极 。该装置工作时,下列说法不正确的是
。该装置工作时,下列说法不正确的是
| A.甲为正极,丙为阴极 |
B.丁极的电极反应式为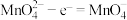 |
C.KOH溶液的质量分数: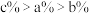 |
D.标准状况下,乙电极上每消耗 气体时,理论上有 气体时,理论上有 移入阴极区 移入阴极区 |
您最近一年使用:0次
2022-05-29更新
|
695次组卷
|
7卷引用:重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题
重庆市巫溪县中学校2020-2021学年高二上学期第二次月考化学试题河南省南阳市第一中学校2022-2023学年高三上学期12月月考化学试题(已下线)课时33 多池多室带膜电化学装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省株洲市第一中学2022届高三下学期第三次模拟考试化学试题四川省泸州市泸县第五中学2021-2022学年高三下学期二诊模拟考试理综化学试题
2013·广东揭阳·三模
解题方法
6 . 某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是
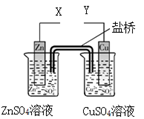

| A.X和Y与电流表连接,电子由Cu极流向Zn极 |
| B.X和Y与电流表连接,将Zn换成Fe测得电流更大 |
| C.X和Y分别与电源“—”、“+”极相连,Cu极质量减轻 |
| D.X和Y分别与电源“—”、“+”极相连,Zn极质量减轻 |
您最近一年使用:0次
名校
解题方法
7 . 有人设想利用电化学原理制备少量硫酸和绿色硝化剂N2O5,所用装置如图所示,下列说法正确的是
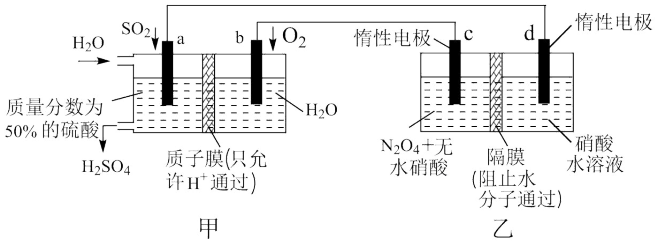

| A.图中的甲池为电解池,乙池为原电池 |
| B.N2O5在c极上产生,c极的电极反应为N2O4-2e-+H2O=N2O5+2H+ |
C.a极发生的电极反应为SO2-2e-+2H2O= +4H+ +4H+ |
| D.每转移2mol电子,生成1molN2O5和1molH2SO4 |
您最近一年使用:0次
2022-02-13更新
|
1233次组卷
|
3卷引用:河南省洛阳市宜阳县第一高级中学2022-2023学年高二上学期第五次能力达标测试化学试题
名校
解题方法
8 . 用石墨烯锂硫电池电解制备 的装置如图所示。电池放电时的反应为
的装置如图所示。电池放电时的反应为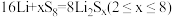 ,电解池两极材料分别为
,电解池两极材料分别为 和石墨,工作一段时间后,右侧玻璃管产生大量的白色沉淀。下列说法正确的是
和石墨,工作一段时间后,右侧玻璃管产生大量的白色沉淀。下列说法正确的是
 的装置如图所示。电池放电时的反应为
的装置如图所示。电池放电时的反应为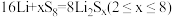 ,电解池两极材料分别为
,电解池两极材料分别为 和石墨,工作一段时间后,右侧玻璃管产生大量的白色沉淀。下列说法正确的是
和石墨,工作一段时间后,右侧玻璃管产生大量的白色沉淀。下列说法正确的是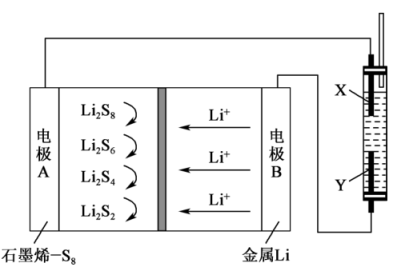
| A.Y是铁电极,发生氧化反应 |
B.电子流动的方向: |
C.正极可发生反应: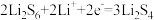 |
D.锂电极减重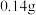 时,则电路中转移 时,则电路中转移 电子 电子 |
您最近一年使用:0次
2021-12-30更新
|
439次组卷
|
3卷引用:山西省运城市教育发展联盟2021-2022学年高二上学期12月月考化学试题
名校
解题方法
9 . 盐酸羟胺(NH3OHCl)是一种常见的还原剂和显像剂,其化学性质类似NH4Cl。工业上主要采用图1所示的方法制备。其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积变化,下列说法正确的是
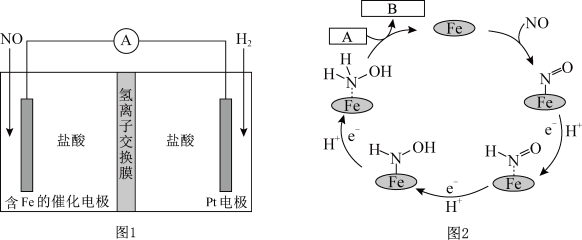
| A.电池工作时,Pt电极是正极 |
| B.图2中,A为H+和e-,B为NH3OH+ |
| C.电池工作时,每消耗2.24LNO(标准状况下),左室溶液质量增加3.3g |
| D.电池工作一段时间后,正、负极区溶液的pH均下降 |
您最近一年使用:0次
2022-04-20更新
|
2212次组卷
|
15卷引用:江苏省南京市雨花台中学2022-2023学年高二上学期10月月考化学试题
江苏省南京市雨花台中学2022-2023学年高二上学期10月月考化学试题湖南省常德市第一中学2022-2023学年高三下学期5月月考化学试题福建省漳州第一中学2023届高三下学期毕业班质检考化学试题福建省南平第一中学2023-2024学年高三上学期第二次阶段考化学试题福建省厦门第一中学2023-2024学年高二上学期10月月考试化学试题福建省福州市2022届高中毕业班(3月)第二次质量检测化学试题湖南省大联考雅礼十六校2021-2022学年高三第二次联考化学试题(已下线)秘籍12 原电池原理及应用-备战2022年高考化学抢分秘籍(全国通用)河北省石家庄市第二中学2022届高三下学期5月模拟考试化学试题江苏省南京市第十三中学2022届高三下学期适应性考试化学试题湖南省郴州市2023届高三下学期第三次教学质量监测化学试题江苏省镇江中学2022-2023学年高一下学期期中考试化学试题江苏省常州市第一中学2022-2023学年高一下学期期末测试化学试题江苏省前黄高级中学2023-2024学年高三上学期期中适应性考试化学试题江苏省徐州市铜山区2023-2024学年高二上学期11月期中考试化学试题(选择考)
10 . (一)己二腈(NC(CH2)4CN)是一种重要的化工产品,工业上先以丙烯为原料制备丙烯腈(CH2=CHCN),再用丙烯腈电合成己二腈,总反应式为CH2=CHCN+2H2O=2NC(CH2)4CN+O2↑。(已知丙烯腈难溶于水,易溶于有机溶剂)。如图为模拟工业电合成己二腈装置图,回答下列问题:

(1)碳棒电极为__ 极(填“阴”或“阳”),其电极反应方程式为__ 。
(2)在甲室中加入异丙醇的作用是__ 。
(3)在甲室中得到产品己二腈54g时,乙室中质量减轻___ g。
(二)2019年诺贝尔化学奖颁给了三个人,其中一个是Goodenough(古迪纳夫),他因为发明可充电锂离子电池而闻名于世,他建造了锂离子电池的神经系统,被业界称为“锂电池之父”。其中一款是钴酸锂(LiCoO2)电池,它的工作原理如图所示,图中电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2 C6+LiCoO2。
C6+LiCoO2。
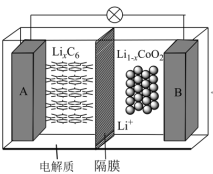
(4)放电时A电极为__ (填“正”或“负”)极,该电极的电极方程式为__ 。
(5)若该锂离子电池充电时,B电极的电极反应方程式为__ 。
(6)若用该锂离子电池给铁片上镀铜,铜片应连接该锂离子电池的极__ (填“A”或“B”),维持电流强度为1A,电池工作二十分钟,理论消耗Cu__ g(已知F=96500C•mol-1,保留两位有效数字)。

(1)碳棒电极为
(2)在甲室中加入异丙醇的作用是
(3)在甲室中得到产品己二腈54g时,乙室中质量减轻
(二)2019年诺贝尔化学奖颁给了三个人,其中一个是Goodenough(古迪纳夫),他因为发明可充电锂离子电池而闻名于世,他建造了锂离子电池的神经系统,被业界称为“锂电池之父”。其中一款是钴酸锂(LiCoO2)电池,它的工作原理如图所示,图中电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-xCoO2
 C6+LiCoO2。
C6+LiCoO2。
(4)放电时A电极为
(5)若该锂离子电池充电时,B电极的电极反应方程式为
(6)若用该锂离子电池给铁片上镀铜,铜片应连接该锂离子电池的极
您最近一年使用:0次



