名校
解题方法
1 . 回答下列问题。
(1)理论上不能设计为原电池的化学反应是___________ 。
a.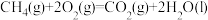
b.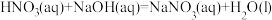
c.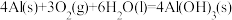
d.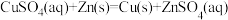
(2)某小组为探究 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为___________ ,盐桥中 向
向___________ 烧杯移动(填“甲”或“乙”)。___________ ,B电极的电极反应方程式为___________ 。 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式___________ 。
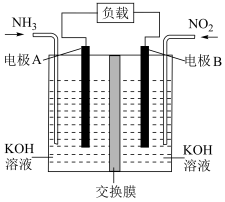
(5)汽车尾气中含有的 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示: 电极为
电极为___________ (填“正极”或“负极), 电极上发生的电极反应式为
电极上发生的电极反应式为___________ 。
(1)理论上不能设计为原电池的化学反应是
a.
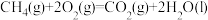
b.
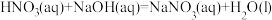
c.
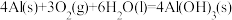
d.
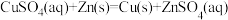
(2)某小组为探究
 与
与 能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和
能否发生氧化还原反应,设计如下图所示双液原电池(盐桥中为饱和 溶液的琼脂)。该装置石墨棒上发生的电极反应式为
溶液的琼脂)。该装置石墨棒上发生的电极反应式为 向
向
 为电解质。工作时负极的电极反应式
为电解质。工作时负极的电极反应式(5)汽车尾气中含有的
 是造成城市空气污染的主要因素之一,通过
是造成城市空气污染的主要因素之一,通过 传感器可监测汽车尾气史
传感器可监测汽车尾气史 含量,其工作原理如图所示:
含量,其工作原理如图所示:
 电极为
电极为 电极上发生的电极反应式为
电极上发生的电极反应式为
您最近一年使用:0次
名校
解题方法
2 . 有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。在101 kPa下,1 g氢气完全燃烧生成液态水放出142.9 kJ的热量。
(1)请写出表示氢气燃烧热的热化学方程式__________________ 。
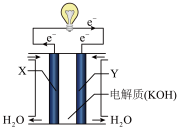
(2)将上述反应设计成下图所示的原电池,其中Y为________ 极(填“正”或“负”),该极电极反应式为___________________ 。

(1)请写出表示氢气燃烧热的热化学方程式
(2)将上述反应设计成下图所示的原电池,其中Y为
您最近一年使用:0次
名校
解题方法
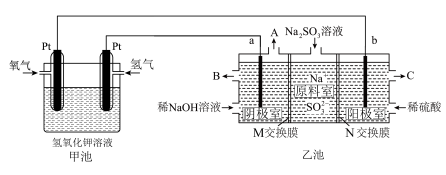
3 . 工业上常用 溶液除去烟气中的
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。_______ 极(填“正”或“负”),写出通入氢气的电极反应式_______ 。
(2)①乙池中阳极室 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为_______ (填“阳”或“阴”)离子交换膜,写出阳极室的电极反应式_______ 。
②阴极室中 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的_______ (用离子符号或化学式填空,下同)得电子反应生成_______ ,其浓度减小,使溶液中_______ 浓度增大,为了保持阴极室溶液中阴阳离子电荷平衡,_______ 从原料室向阴极室迁移,从而使阴极室中 的浓度增大。
的浓度增大。
(3)在标准状况下,若甲池中有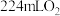 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成_______ 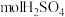 。
。
(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上, 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为_______ 。
 溶液除去烟气中的
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。
(2)①乙池中阳极室
 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为②阴极室中
 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的 的浓度增大。
的浓度增大。(3)在标准状况下,若甲池中有
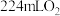 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成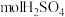 。
。(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上,
 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为
您最近一年使用:0次
2024-01-21更新
|
139次组卷
|
2卷引用:广东省深圳市光明区2023-2024学年高二上学期1月期末学业水平调研化学试题
解题方法
4 . 原电池是直接把化学能转化为电能的装置。
(1)某研究性学习小组的同学对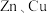 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和 溶液,起到连通电路的作用)。
溶液,起到连通电路的作用)。
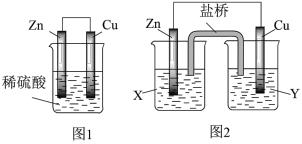
①实验表明,图1中锌电极为_____ 极(填写“正”或“负”),电极反应为:_____ 。
②图2中实验过程中只有 极上产生气泡,则X是
极上产生气泡,则X是_____ 溶液,正极的电极反应式为_____ 。
(2)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为: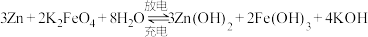
①放电时,正极反应为_____ 。
②放电时,_____ (填“正”或“负”)极附近溶液的碱性增强。
(3)新型固体燃料电池的电解质是固体氧化锆和氧化钇,高温下允许氧离子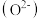 在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:
在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:_____ 。

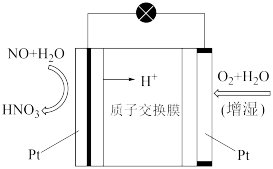
(4)一氧化氮—空气质子交换膜燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如图所示,写出放电过程中负极的电极反应式:_____ ,若过程中产生 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为_____ L。
(1)某研究性学习小组的同学对
 、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和
、稀硫酸组成的原电池进行了探究,其中甲同学利用如图1所示装置进行探究,乙同学经过查阅资料后设计了图2装置进行探究(盐桥内含有某种电解质的饱和 溶液,起到连通电路的作用)。
溶液,起到连通电路的作用)。
①实验表明,图1中锌电极为
②图2中实验过程中只有
 极上产生气泡,则X是
极上产生气泡,则X是(2)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:
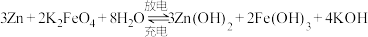
①放电时,正极反应为
②放电时,
(3)新型固体燃料电池的电解质是固体氧化锆和氧化钇,高温下允许氧离子
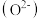 在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:
在其间通过。如图所示,其中多孔电极不参与电极反应。写出该电池的负极电极反应式:
(4)一氧化氮—空气质子交换膜燃料电池将化学能转化为电能的同时,实现了制硝酸、发电、环保三位一体的结合,其工作原理如图所示,写出放电过程中负极的电极反应式:
 ,则消耗标准状况下
,则消耗标准状况下 的体积为
的体积为
您最近一年使用:0次
22-23高一下·广东深圳·期中
名校
5 . 电池是人类生产和生活中的重要能量来源。人们应用原电池原理制作了多种电池以满足不同的需要。在现代生活、生产和科学技术发展中,电池发挥着越来越重要的作用。
(1)知识源于实践。学习原电池知识后,某学习小组以 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
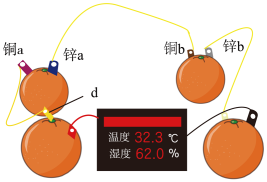
(2)生活中利用原电池原理生产了各种各样的电池,下列有关电池的叙述正确的是_______(填字母)。
(3)将 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
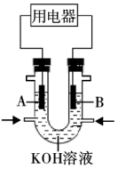
实验测得电子定向移向 电极,则
电极,则_______ (填“ ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为_______ 。
(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为: ,请回答下列问题:
,请回答下列问题:
①放电时,正极反应式为_______ 。
②放电时,负极附近溶液的碱性_______ 。(填“增强”或“减弱”)
(5) 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
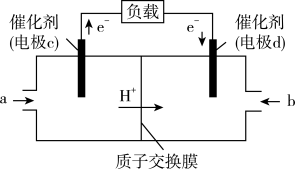
电池总反应为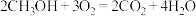 ,则
,则 电极反应式为
电极反应式为_______ ,若线路中转移 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为_______  。
。
(1)知识源于实践。学习原电池知识后,某学习小组以
 和
和 为电极材料,制作了如图所示的水果电池(水果果汁中含游离的
为电极材料,制作了如图所示的水果电池(水果果汁中含游离的 )。该组电池放电时,下列说法正确的是_______(填字母)。
)。该组电池放电时,下列说法正确的是_______(填字母)。
A.每个水果果汁中的 移向正极 移向正极 |
B.锌 、 、 发生的电极反应式为 发生的电极反应式为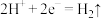 |
C.四个水果电池串联,则电极 为铜片 为铜片 |
D.铜 为电池正极,发生氧化反应 为电池正极,发生氧化反应 |
| A.锌锰电池工作一段时间后碳棒会变细 |
| B.氢氧燃料电池具有高效的特点,能量转化率可达100% |
| C.太阳能电池的主要材料是高纯度的二氧化硅 |
D.铅蓄电池负极是 ,正极是 ,正极是 |
 设计成燃料电池,共利用率更高,装置如图所示(
设计成燃料电池,共利用率更高,装置如图所示( 、
、 为多孔碳棒)
为多孔碳棒)
实验测得电子定向移向
 电极,则
电极,则 ”或“
”或“ ”)电极入口通甲烷,其电极反应式为
”)电极入口通甲烷,其电极反应式为(4)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为:
 ,请回答下列问题:
,请回答下列问题:①放电时,正极反应式为
②放电时,负极附近溶液的碱性
(5)
 与
与 反应还可制备
反应还可制备 ,
, 可作为燃料使用,用
可作为燃料使用,用 和
和 组合形成的质子交换膜燃料电池的结构示意图如图:
组合形成的质子交换膜燃料电池的结构示意图如图:
电池总反应为
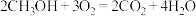 ,则
,则 电极反应式为
电极反应式为 电子,则上述
电子,则上述 燃料电池,消耗的
燃料电池,消耗的 的质量为
的质量为 。
。
您最近一年使用:0次
名校
6 . 按要求回答下列问题:
(1)已知H2和O2反应时放热,且断裂1molH-H键、1molO=O键、1molO-H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ。下列关系一定正确的是_________。
(2)下列变化中满足如图图示的是_________ (填选项字母)。
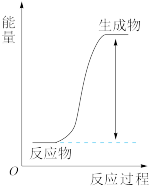
A镁和稀盐酸的反应 B.Ba(OH)2•8H2O与NH4Cl的反应 C.氯化铵固体加入水中 D.氢气燃烧 E.H-O-H→2H+O
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为_________ (填选项字母)。
A铝片、铜片 B.铜片、铝片 C.铝片、铝片
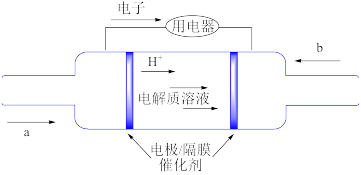
(4)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢燃料电池被誉为氢能源汽车的心脏。某种氢燃料电池的内部结构如图所示,a 处通入气体的是_________ ,左侧的电极为电池的_________ (填“正极”或“负极”), 右侧电极发生的反应为:_________ 。
(1)已知H2和O2反应时放热,且断裂1molH-H键、1molO=O键、1molO-H键需要吸收的能量分别为Q1kJ、Q2kJ、Q3kJ。下列关系一定正确的是_________。
| A.Q1+Q2>Q3 | B.2Q1+Q2>2Q3 | C.2Q1+Q2<4Q3 | D.2Q1+Q2>4Q3 |

A镁和稀盐酸的反应 B.Ba(OH)2•8H2O与NH4Cl的反应 C.氯化铵固体加入水中 D.氢气燃烧 E.H-O-H→2H+O
(3)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A铝片、铜片 B.铜片、铝片 C.铝片、铝片
(4)2020年上海进博会展览中,诸多氢能源汽车纷纷亮相。氢燃料电池被誉为氢能源汽车的心脏。某种氢燃料电池的内部结构如图所示,a 处通入气体的是

您最近一年使用:0次
名校
7 . 填空。
(1)请你写出以强酸溶液为电解质溶液的甲烷燃料电池的负极的电极反应式_______ 。若线路中转移2mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。请你写出铅蓄电池的正极的电极反应式_______ 。
(2)已知2Fe3++Cu=2Fe2++Cu2+,利用这一反应,试设计一个原电池,画出示意图,标明电极材料名称,电解质溶液_______ 。在该电池中,正极是_______ ,电极反应式_______ 。
(1)请你写出以强酸溶液为电解质溶液的甲烷燃料电池的负极的电极反应式
 在标准状况下的体积为
在标准状况下的体积为(2)已知2Fe3++Cu=2Fe2++Cu2+,利用这一反应,试设计一个原电池,画出示意图,标明电极材料名称,电解质溶液
您最近一年使用:0次
解题方法
8 . 运用原电池原理可研究物质的性质或进行工业生产。
(1)某兴趣小组设计图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是____ (填“锌”或“铜”);当正极质量增加12.8g时,转移了____ mol电子。

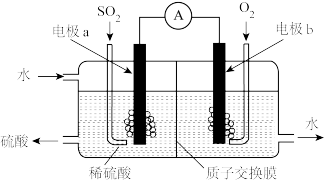
(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。a是____ 极(填“正”或“负”),b电极反应式为____ ,生产过程中H+向____ (填“a”或“b”)电极区域运动。
(1)某兴趣小组设计图装置用锌、铜作电极材料,硫酸铜溶液为电解质溶液的进行原电池实验。负极材料是

(2)如图所示,运用原电池原理可将SO2转化成硫酸。其中质子交换膜将该原电池分隔成氧化反应室和还原反应室,能阻止气体通过而允许H+通过。a是

您最近一年使用:0次
名校
解题方法
9 . 把化学能转化为电能的装置叫做原电池。
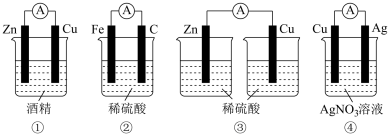
(1)装置①、②、③中,能组成原电池的是装置_______ 。
(2)装置④中,正极材料是_______ ;负极的电极反应式为_______ ;电池工作时,总反应的离子方程式为_______ ;烧杯中 向
向_______ 电极移动(填“Cu”或“Ag”);导线中电子的流动方向为_______ (填“Cu到Ag”或“Ag到Cu”)。

(1)装置①、②、③中,能组成原电池的是装置
(2)装置④中,正极材料是
 向
向
您最近一年使用:0次
10 . 载人航天器中的物质和能量资源都十分宝贵。利用萨巴蒂尔反应再生氧气的大体流程如下图所示。

(1)从元素转化角度来看,上述流程中萨巴蒂尔反应的缺点是___________ 。
飞行时间较长时可用如下图所示的电化学富集法富集二氧化碳。
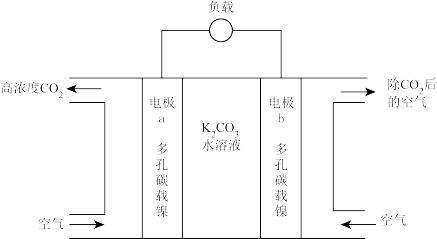
(2)电极材料采用多孔碳载镍,“多孔”的优点是___________ 。
(3)电极a是___________ (填“正极”或“负极”),电极反应式为___________ 。
(4)电极b发生反应___________ (填“氧化”或还原”),电极反应式为___________ 。
(5)K+向电极___________ (填"a”或b”)方向移动。

(1)从元素转化角度来看,上述流程中萨巴蒂尔反应的缺点是
飞行时间较长时可用如下图所示的电化学富集法富集二氧化碳。

(2)电极材料采用多孔碳载镍,“多孔”的优点是
(3)电极a是
(4)电极b发生反应
(5)K+向电极
您最近一年使用:0次
2022-01-23更新
|
309次组卷
|
2卷引用:广东省广州市五校2021-2022学年高二上学期期末联考化学试题



