解题方法
1 . 2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
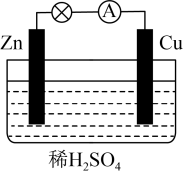
(1)下图是_______ 装置,能量转化是,_____ 能转化为_____ 能。______ 极,发生_____ (填“氧化”或“还原”)反应。
(3)Cu棒,上发生的电极反应是______ 。
(4)溶液中H⁺向______ (填“Zn”或“Cu”)电极定向移动。
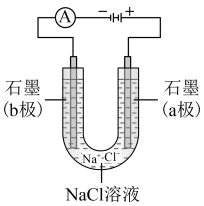
(5)下图是_____ 装置,a极是该电池的_______ 极,b极是该电池的_____ 极。
(1)下图是
(3)Cu棒,上发生的电极反应是
(4)溶液中H⁺向
(5)下图是
您最近一年使用:0次
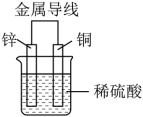
2 . 如图为Zn-Cu原电池的示意图,请回答:_______ 极,铜片为原电池的_______ 极 (填“正”或“负”) 。
(2)锌电极反应式是_______ ,属于_______ 反应(填“氧化”或“还原”);铜电极反应式是_______ ,属于_______ 反应(同上)。
(3)若锌片减轻0.1mol,则另一极放出气体的物质的量为_______ mol。
(2)锌电极反应式是
(3)若锌片减轻0.1mol,则另一极放出气体的物质的量为
您最近一年使用:0次
3 . 按要求回答下列问题:
(1)下列各组微粒:
① 与
与 ;②
;② 和
和 ;③H、D、T;④金刚石和石墨;⑤
;③H、D、T;④金刚石和石墨;⑤ 和
和 ;⑥
;⑥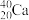 和
和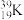 。
。
互为同位素的是___________ (填序号),透过蓝色钴玻璃观察K元素燃烧时的焰色为___________ 色。
(2)现有如下三个反应:
A.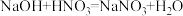
B.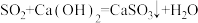
C.
根据三个反应本质,能设计成原电池的是___________ (填“A”、“B”或“C”)。该原电池的负极材料为___________ ,若导线上转移电子0.6mol,则电极减少的质量是___________ g。
(1)下列各组微粒:
①
 与
与 ;②
;② 和
和 ;③H、D、T;④金刚石和石墨;⑤
;③H、D、T;④金刚石和石墨;⑤ 和
和 ;⑥
;⑥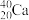 和
和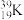 。
。互为同位素的是
(2)现有如下三个反应:
A.
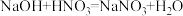
B.
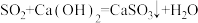
C.

根据三个反应本质,能设计成原电池的是
您最近一年使用:0次
4 . 电化学技术的发展是近年来科技的热点。请结合电化学知识回答下列问题:
(1)如图甲所示的电化学装置。盐桥为浸泡了饱和氯化钾溶液的琼脂。反应一段时间,向两烧杯中分别滴加几滴酚酞,___________ (填“m”或“ 烧杯中溶液变红,盐桥中的K+向
烧杯中溶液变红,盐桥中的K+向___________ (填“m”或“n”)烧杯移动。 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 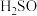 4和NaOH。
4和NaOH。___________ 。
②电解池中同时制备 和NaOH的总反应为
和NaOH的总反应为___________ 。
③d膜为___________ (填“阳”或“阴”)离子交换膜。
④当电解池中产生标准状况下22.4L H2时,理论上正极区CuSO4浓度变为___________ mol/L。
⑤从电池开始工作到停止放电,制备NaOH的质量为204g。若该电化学装置的工作效率= 。则该过程的工作效率为
。则该过程的工作效率为___________ 。
(1)如图甲所示的电化学装置。盐桥为浸泡了饱和氯化钾溶液的琼脂。反应一段时间,向两烧杯中分别滴加几滴酚酞,
 烧杯中溶液变红,盐桥中的K+向
烧杯中溶液变红,盐桥中的K+向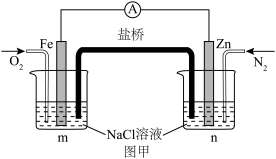
 溶液(a、b电极均为石墨电极),可以制得
溶液(a、b电极均为石墨电极),可以制得 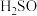 4和NaOH。
4和NaOH。
②电解池中同时制备
 和NaOH的总反应为
和NaOH的总反应为③d膜为
④当电解池中产生标准状况下22.4L H2时,理论上正极区CuSO4浓度变为
⑤从电池开始工作到停止放电,制备NaOH的质量为204g。若该电化学装置的工作效率=
 。则该过程的工作效率为
。则该过程的工作效率为
您最近一年使用:0次
解题方法
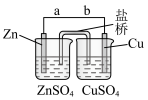
5 . 某学生利用下面实验装置探究盐桥式原电池的工作原理。
(1)锌电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ ;铜电极为电池的___________ 极,电极上发生的是___________ 反应(“氧化”或“还原”),电极反应式为___________ 。
(2)导线中电子流向由___________ 流向___________ (用a、b表示)。
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为___________ ;
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
(5)反应一段时间后右侧烧杯中Cu2+浓度是___________ (填增大,减小或不变)。
(1)锌电极为电池的
(2)导线中电子流向由
(3)若装置中铜电极的质量增加0.64g,则导线中转移的电子的物质的量为
(4)若ZnSO4溶液中含有杂质Cu2+,会加速Zn电极的腐蚀、还可能导致电流在较短时间内衰减。欲除去Cu2+,最好选用下列试剂中的___________(填代号)。
| A.NaOH | B.Zn | C.Fe | D.H2SO4 |
(5)反应一段时间后右侧烧杯中Cu2+浓度是
您最近一年使用:0次
6 . 电解工作原理的实际应用非常广泛。
(1)电解精炼银时,粗银作___________ ,阴极反应为___________ 。
(2)工业上为了处理含有Cr2O 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
(3)某同学设计了如图装置进行以下电化学实验。
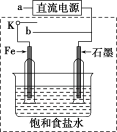
①当开关K与a连接时,两极均有气泡产生,则阴极为___________ 电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为___________ 。请写出此时Fe电极上的电极反应___________ 。
(4)1 L某溶液中含有的离子如下表:
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是___________(填字母)。
(1)电解精炼银时,粗银作
(2)工业上为了处理含有Cr2O
 的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。
的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是___________(填字母)。| A.阳极反应:Fe-2e-=Fe2+ | B.阴极反应:2H++2e-=H2↑ |
| C.在电解过程中工业废水由酸性变为碱性 | D.可以将铁电极改为石墨电极 |

①当开关K与a连接时,两极均有气泡产生,则阴极为
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为
(4)1 L某溶液中含有的离子如下表:
| 离子 | Cu2+ | Al3+ | NO | Cl- |
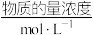 | 1 | 1 | a | 1 |
| A.电解后溶液呈酸性 | B.a=3 |
| C.阳极生成1.5 mol Cl2 | D.阴极析出的金属是铜与铝 |
您最近一年使用:0次
名校
解题方法
7 . 全钒液流电池是化学储能领域的一个研究热点,储能容量大、使用寿命长,利用该电池电解处理含 的废水制备硝酸和氨水的原理如图所示,
的废水制备硝酸和氨水的原理如图所示,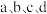 电极均为惰性电极。
电极均为惰性电极。
回答下列问题:
(1) 电极为
电极为___________ (填“正极”或“负极”), 电极反应式为
电极反应式为___________ 。
(2)隔膜1为___________ 交换膜(填“阴离子”或“阳离子”),q口流出液含有的溶质为___________ (填化学式),d电极的电极反应式为___________ 。
(3)B装置中产生的气体总量为 (标准状况下)时,通过质子交换膜的
(标准状况下)时,通过质子交换膜的  的物质的量为
的物质的量为___________  。
。
 的废水制备硝酸和氨水的原理如图所示,
的废水制备硝酸和氨水的原理如图所示, 电极均为惰性电极。
电极均为惰性电极。
回答下列问题:
(1)
 电极为
电极为 电极反应式为
电极反应式为(2)隔膜1为
(3)B装置中产生的气体总量为
 (标准状况下)时,通过质子交换膜的
(标准状况下)时,通过质子交换膜的  的物质的量为
的物质的量为 。
。
您最近一年使用:0次
8 . 随着工业的发展,如何高效处理污水成为人类亟待解决的问题。
(1)利用原电池原理,酸性废水中的 在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
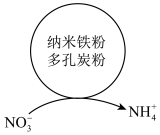
①图中,纳米铁粉作__________ (填“正极”或“负极”),多孔炭粉的作用为__________ 。
②正极上的电极反应式为__________ 。
(2)科研人员利用垃圾渗透液实现发电、环保二位一体,装置如图(a、b为离子交换膜)。
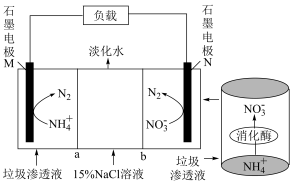
①石墨电极M上的电极反应式为__________ 。
②a为__________ (填“阴离子”或“阳离子”)交换膜。
③在放电过程中, 由中间室向
由中间室向__________ (填“M”或“N”)极室移动。
④理论上M极每处理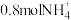 ,电路中通过的电子数为
,电路中通过的电子数为__________  。
。
(1)利用原电池原理,酸性废水中的
 在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
在水处理剂(主要成分为铁粉、炭粉)表面的变化如图所示。
①图中,纳米铁粉作
②正极上的电极反应式为
(2)科研人员利用垃圾渗透液实现发电、环保二位一体,装置如图(a、b为离子交换膜)。

①石墨电极M上的电极反应式为
②a为
③在放电过程中,
 由中间室向
由中间室向④理论上M极每处理
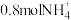 ,电路中通过的电子数为
,电路中通过的电子数为 。
。
您最近一年使用:0次
名校
解题方法
9 . 电池是日常生活中最常见的一种提供电能的装置,研究各种新型电池成为新能源研究的一种方向。
(1)如图是一种甲烷燃料电池的装置。
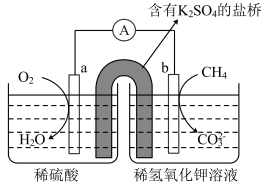
①铂电极a是__________ 填“正极”“负极”“阳极”或“阴极”),发生__________ (填“氧化”或“还原”)反应。
②电子从__________ (填“a”或“b”)电极流出,该电极的电极反应式是__________ 。
③盐桥中的 向
向__________ (填“稀硫酸”或“稀氢氧化钾”)溶液移动。
(2)白铁是日常生活中常见的一种金属材料,俗称“锌包钢”,一旦划破后就会发生电化学反应,此时负极材料是__________ ,在潮湿的碱性或中性环境中,铁电极上发生反应的电极反应式是__________ 。金属铁被保护而不易腐蚀,这种防腐的方法叫__________ (填名称)。
(1)如图是一种甲烷燃料电池的装置。

①铂电极a是
②电子从
③盐桥中的
 向
向(2)白铁是日常生活中常见的一种金属材料,俗称“锌包钢”,一旦划破后就会发生电化学反应,此时负极材料是
您最近一年使用:0次
名校
解题方法
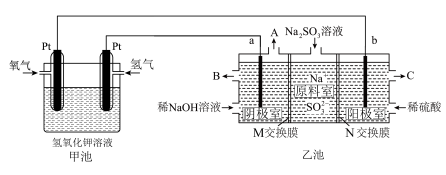
10 . 工业上常用 溶液除去烟气中的
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。_______ 极(填“正”或“负”),写出通入氢气的电极反应式_______ 。
(2)①乙池中阳极室 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为_______ (填“阳”或“阴”)离子交换膜,写出阳极室的电极反应式_______ 。
②阴极室中 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的_______ (用离子符号或化学式填空,下同)得电子反应生成_______ ,其浓度减小,使溶液中_______ 浓度增大,为了保持阴极室溶液中阴阳离子电荷平衡,_______ 从原料室向阴极室迁移,从而使阴极室中 的浓度增大。
的浓度增大。
(3)在标准状况下,若甲池中有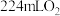 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成_______ 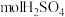 。
。
(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上, 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为_______ 。
 溶液除去烟气中的
溶液除去烟气中的 ,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物
,某小组设计如图所示装置(a、b电极均为石墨),对除硫后产物 溶液进行电解,制得
溶液进行电解,制得 和循环再生
和循环再生 。
。
(2)①乙池中阳极室
 口流出的是较浓的
口流出的是较浓的 ,则
,则 为
为②阴极室中
 溶液浓度增大的原因是:阴极室中水电离出的
溶液浓度增大的原因是:阴极室中水电离出的 的浓度增大。
的浓度增大。(3)在标准状况下,若甲池中有
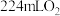 参加反应,理论上乙池可生成
参加反应,理论上乙池可生成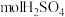 。
。(4)比能量是指参与反应单位质量的电极材料所能输出电能的多少,电池输出电能与反应的电子转移数目成正比。理论上,
 与
与 均作负极时,它们的比能量之比为
均作负极时,它们的比能量之比为
您最近一年使用:0次
2024-01-21更新
|
139次组卷
|
2卷引用:广东省深圳市光明区2023-2024学年高二上学期1月期末学业水平调研化学试题



