2023高三·全国·专题练习
1 . 某小组同学欲探究NaHSO3与Cu2+的反应,经查阅资料后提出假设,并进行实验验证。已知:氯化亚铜(CuCl)是不溶于水的白色沉淀。
假设1:Cu2+与HSO 仅发生相互促进的水解反应。
仅发生相互促进的水解反应。
假设2:HSO 可以还原Cu2+。
可以还原Cu2+。
设计实验如下:
实验I:向2mL1mol•L-1NaHSO3溶液中加入2ml1mol•L-1CuSO4溶液,得到绿色溶液,放置一段时间后无明显变化。
实验II:向I所得绿色溶液中加入适量NaCl固体,开始时无明显变化,30s后有无色气体和白色沉淀生成,同时溶液颜色变浅。
(1)实验证实假设______ (填“1”或“2”)合理,设计实验验证实验II中产生的无色气体为SO2:______ 。
(2)从化学平衡的角度解释产生实验II中现象的原因:______ 。
(3)某同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差E=Eθ- lg
lg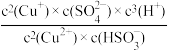 [其中Eθ(标准电极电势)、R(理想气体常数)、F(法拉第常数)为定值],为进一步验证上述结论,在恒温条件下设计如表实验。
[其中Eθ(标准电极电势)、R(理想气体常数)、F(法拉第常数)为定值],为进一步验证上述结论,在恒温条件下设计如表实验。
①根据实验I、II的结论,推测甲、乙两实验现象的区别:______ (写出两条即可)。
②根据所查资料,解释产生上述现象的原因:______ 。
假设1:Cu2+与HSO
 仅发生相互促进的水解反应。
仅发生相互促进的水解反应。假设2:HSO
 可以还原Cu2+。
可以还原Cu2+。设计实验如下:
实验I:向2mL1mol•L-1NaHSO3溶液中加入2ml1mol•L-1CuSO4溶液,得到绿色溶液,放置一段时间后无明显变化。
实验II:向I所得绿色溶液中加入适量NaCl固体,开始时无明显变化,30s后有无色气体和白色沉淀生成,同时溶液颜色变浅。
(1)实验证实假设
(2)从化学平衡的角度解释产生实验II中现象的原因:
(3)某同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差E=Eθ-
 lg
lg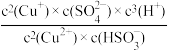 [其中Eθ(标准电极电势)、R(理想气体常数)、F(法拉第常数)为定值],为进一步验证上述结论,在恒温条件下设计如表实验。
[其中Eθ(标准电极电势)、R(理想气体常数)、F(法拉第常数)为定值],为进一步验证上述结论,在恒温条件下设计如表实验。| 编号 | 甲 | 乙 |
| 实验 |  | 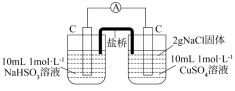 |
②根据所查资料,解释产生上述现象的原因:
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
2 . 某化学学习小组同学利用Fe3+与I-发生的氧化还原反应设计一个原电池,并进行有关实验探究。请回答相关问题:
(1)画出简单的示意图,并标明所使用的用品。供选择的实验用品:KCl溶液,FeCl3溶液,FeCl2溶液,KI溶液,铜片,锌片,铁片,石墨棒,烧杯,盐桥,导线,灵敏电流计______ 。
(2)利用(1)中设计好的装置,控制适合的条件对反应2Fe3++2I- 2Fe2++I2进行实验探究:
2Fe2++I2进行实验探究:
①反应开始时,右池中电极上发生氧化反应,电极反应式为______ ,盐桥中的_____ (填“阳”或“阴”)离子向右池移动。
②电流计指针不发生偏转时,反应达到化学平衡状态,在左池中加入FeCl2固体,右池的电极作______ (填“正”“负”)极。
(1)画出简单的示意图,并标明所使用的用品。供选择的实验用品:KCl溶液,FeCl3溶液,FeCl2溶液,KI溶液,铜片,锌片,铁片,石墨棒,烧杯,盐桥,导线,灵敏电流计
(2)利用(1)中设计好的装置,控制适合的条件对反应2Fe3++2I-
 2Fe2++I2进行实验探究:
2Fe2++I2进行实验探究:①反应开始时,右池中电极上发生氧化反应,电极反应式为
②电流计指针不发生偏转时,反应达到化学平衡状态,在左池中加入FeCl2固体,右池的电极作
您最近一年使用:0次
名校
3 . 科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示。下列说法错误的是


A.电极 为电池的负极 为电池的负极 |
| B.电极b上发生的电极反应:O2+4H++4e-=2H2O |
| C.电路中每通过4mol电子,则负极消耗(标准状况下)44.8LH2S |
| D.每17gH2S参与反应,则有2molH+经质子膜进入正极区 |
您最近一年使用:0次
2023-02-17更新
|
660次组卷
|
5卷引用:四川省青神中学校2022-2023学年高二下学期3月月考化学试题
四川省青神中学校2022-2023学年高二下学期3月月考化学试题河南省郑州中学2023-2024学年高三上学期第二次月考化学试题(已下线)专题09 原电池-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)广东省深圳外国语学校2022-2023学年高二上学期期末考试化学试题广东省化州市第一中学2023-2024学年高二上学期12月质量检测化学试卷
解题方法
4 . 净化含尿素和酸性 废水的微生物燃料电池工作原理如图。下列说法错误的是
废水的微生物燃料电池工作原理如图。下列说法错误的是
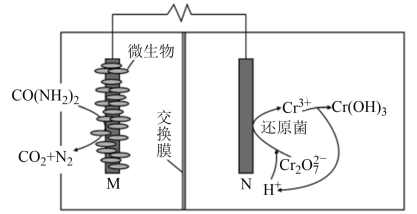
 废水的微生物燃料电池工作原理如图。下列说法错误的是
废水的微生物燃料电池工作原理如图。下列说法错误的是
| A.放电时,电子由M电极沿导线流向N电极 |
| B.放电时,负极的电极反应为CO(NH2)2+H2O-6e-=CO2↑ + N2↑+ 6H+ |
C.当废水中 的浓度或酸性过大时,电池的效率都会降低 的浓度或酸性过大时,电池的效率都会降低 |
D.1 mol  被净化时,有8 mol H+从M室迁移到N室 被净化时,有8 mol H+从M室迁移到N室 |
您最近一年使用:0次
2023-02-14更新
|
489次组卷
|
4卷引用:河北省唐山市2022-2023学年高二上学期期末考试化学试题
河北省唐山市2022-2023学年高二上学期期末考试化学试题河北省唐山市2022-2023学年高二下学期开学考试化学试题(已下线)题型18 微生物电池的应用(已下线)专题09 原电池-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)
名校
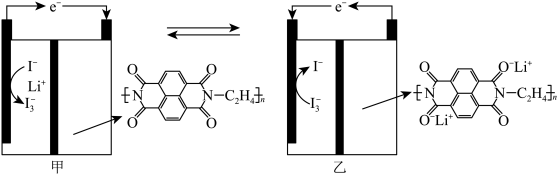
5 . 一种新型的 电池原理如图所示.其电解质为
电池原理如图所示.其电解质为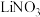 溶液,正极采用含有
溶液,正极采用含有 、
、 的水溶液,负极采用固体有机聚合物,聚合物离子交换膜将正负极分隔开.已知:
的水溶液,负极采用固体有机聚合物,聚合物离子交换膜将正负极分隔开.已知: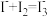 (
( 为棕色),下列不正确的是
为棕色),下列不正确的是
 电池原理如图所示.其电解质为
电池原理如图所示.其电解质为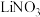 溶液,正极采用含有
溶液,正极采用含有 、
、 的水溶液,负极采用固体有机聚合物,聚合物离子交换膜将正负极分隔开.已知:
的水溶液,负极采用固体有机聚合物,聚合物离子交换膜将正负极分隔开.已知: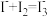 (
( 为棕色),下列不正确的是
为棕色),下列不正确的是
| A.图甲是原电池工作原理图,图乙是电池充电原理图 |
| B.放电时,正极液态电解质溶液的颜色变浅 |
C.充电时, 从左向右通过聚合物离子交换膜 从左向右通过聚合物离子交换膜 |
D.放电时,负极的电极反应式为: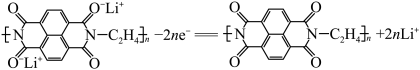 |
您最近一年使用:0次
2023-02-14更新
|
412次组卷
|
4卷引用:北京市海淀区教师进修学校2022-2023学年高三下学期开学检测化学试题
北京市海淀区教师进修学校2022-2023学年高三下学期开学检测化学试题(已下线)专题卷16 离子隔膜在电化学中的应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)江西省南昌市八一中学2023届高三下学期三模理综化学试题2023届宁夏回族自治区石嘴山市第三中学高三下学期第三次模拟考试理综试题
2023高三·全国·专题练习
解题方法
6 . 锂—铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀“现象”产生电能,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是
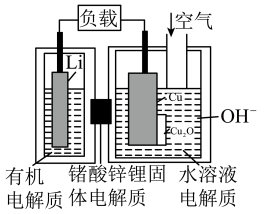

| A.放电时,Li+透过固体电解质向Cu极移动 |
B.放电时,正极的电极反应式为 |
| C.通空气时,铜被腐蚀,表面产生Cu2O |
| D.整个反应过程中,氧化剂为O2 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
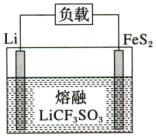
7 .  电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的反应为
电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的反应为 。下列说法错误的是
。下列说法错误的是
 电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的反应为
电池是目前电池中综合性能最好的一种电池,其结构如图所示。已知电池放电时的反应为 。下列说法错误的是
。下列说法错误的是
A. 为电池的负极 为电池的负极 |
B.电池工作时, 向正极移动 向正极移动 |
C.正极的电极反应式为 |
D.将熔融的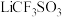 改为 改为 的水溶液,电池性能更好 的水溶液,电池性能更好 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
8 . 当反应物中的某离子或过量反应物影响产物的检验时,用电化学装置探究,将产物与反应物隔离开,能更准确地检验产物。例如,某实验小组对KSCN的性质进行探究,设计了如下实验:
(1)实验步骤ii中溶液变红的原因:_______ 、_______ (用离子方程式说明)。
(2)针对实验步骤ii中红色褪去的原因,该实验小组同学认为是 被酸性
被酸性 溶液氧化为
溶液氧化为 ,由于硫酸酸化的高锰酸钾溶液中存在
,由于硫酸酸化的高锰酸钾溶液中存在 ,所以不能直接取褪色后的溶液来验证
,所以不能直接取褪色后的溶液来验证 的氧化产物是
的氧化产物是 ,故设计了如图所示实验装置来证实上述猜想是成立的。
,故设计了如图所示实验装置来证实上述猜想是成立的。

检验产物中 的操作及现象是
的操作及现象是_______ 。
| 装置 | 实验步骤 | 现象 |
 | i.先加 溶液 溶液 | 无明显现象 |
ii.再加硫酸酸化的 溶液 溶液 | 溶液先变红后褪色 |
(2)针对实验步骤ii中红色褪去的原因,该实验小组同学认为是
 被酸性
被酸性 溶液氧化为
溶液氧化为 ,由于硫酸酸化的高锰酸钾溶液中存在
,由于硫酸酸化的高锰酸钾溶液中存在 ,所以不能直接取褪色后的溶液来验证
,所以不能直接取褪色后的溶液来验证 的氧化产物是
的氧化产物是 ,故设计了如图所示实验装置来证实上述猜想是成立的。
,故设计了如图所示实验装置来证实上述猜想是成立的。
检验产物中
 的操作及现象是
的操作及现象是
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
9 . 钴酸锂电池的正极材料含有钴酸锂(LiCoO2)、导电剂乙炔黑、铝箔及少量铁,通过如图工艺流程可回收铝、钴、锂。

回答下列问题:
(1)钴酸锂电池放电时负极反应式为LixC6-xe-=C6+xLi+,拆解废旧电池前进行放电处理,既可保证安全又有利于回收锂。有利于回收锂的原因是______ 。
(2)“酸浸”时Co、Li元素的浸出率随温度的变化如图所示:

“酸浸”的适宜温度是______ ,该过程有多个反应,钴酸锂发生的主要反应的离子方程式为______ 。
(3)沉锂过程要对所得滤渣进行洗涤,检验沉淀是否洗净的操作为______ 。
(4)沉钴的化学方程式为_____ 。将100mL0.50mol•L-1CoSO4溶液沉钴所得晶体配成溶液,经过一系列处理后通过滴定实验测得消耗0.50mol•L-1碘标准溶液48.50mL,则沉钴过程中CoC2O4•2H2O的产率为_____ (已知:在“一系列处理”过程中二价钴被碘氧化成三价钴)。

回答下列问题:
(1)钴酸锂电池放电时负极反应式为LixC6-xe-=C6+xLi+,拆解废旧电池前进行放电处理,既可保证安全又有利于回收锂。有利于回收锂的原因是
(2)“酸浸”时Co、Li元素的浸出率随温度的变化如图所示:

“酸浸”的适宜温度是
(3)沉锂过程要对所得滤渣进行洗涤,检验沉淀是否洗净的操作为
(4)沉钴的化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 电化学制氢是实现氢经济的重要途径。中国科学院近来提出了一种新型的可充电锌—肼(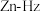 )电池,采用双功能电催化剂实现了独立的析氢反应,原理如图,下列说法不正确的是
)电池,采用双功能电催化剂实现了独立的析氢反应,原理如图,下列说法不正确的是
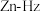 )电池,采用双功能电催化剂实现了独立的析氢反应,原理如图,下列说法不正确的是
)电池,采用双功能电催化剂实现了独立的析氢反应,原理如图,下列说法不正确的是
A.放电时,左侧电极反应式: |
B.充电时,右侧电极反应式: |
C.电池工作时, 与 与 可同时在右侧生成 可同时在右侧生成 |
D.放电时,每转移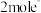 ,可产生标况下 ,可产生标况下 气体 气体 |
您最近一年使用:0次
2023-02-11更新
|
1066次组卷
|
4卷引用:辽宁省东北育才学校等五校2022-2023学年高三上学期期末考试化学试题



