1 . 亚硫酸氢钠在染料、造纸制革、化学合成等工业中可用作还原剂。
(一)制备NaHSO3(装置如图所示)。
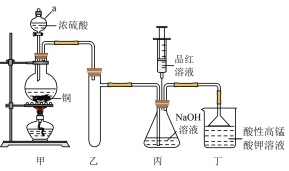
(1)装置丁的作用有①___________ ;②___________ ;③吸收尾气,防止环境污染。
(2)将丙中针筒内品红溶液推进锥形瓶中,若发现___________ ,则说明NaOH已完全转化为NaHSO3。
(二)小组同学欲探究NaHSO3与 的反应,经查阅资料后提出假设,并进行实验验证。
的反应,经查阅资料后提出假设,并进行实验验证。
已知:氯化亚铜(CuCl)是不溶于水的白色沉淀
假设1: 与
与 仅发生双水解反应
仅发生双水解反应
假设2: 可以还原
可以还原
设计实验如下:
①向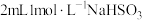 溶液中加入
溶液中加入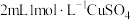 溶液,得到绿色溶液,放置一段时间无明显变化。
溶液,得到绿色溶液,放置一段时间无明显变化。
②向①所得绿色溶液中加入适量NaCl固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。
(3)实验证实假设___________ 合理,实验①发生的离子方程式为___________ 。
(4)甲、乙同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差 [其中
[其中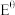 (标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
(标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
①根据上述实验结论,对比甲、乙两实验,写出乙同学实验现象为___________ (写出两条即可)。
②根据相关资料,解释产生上述现象的原因为___________ 。
(一)制备NaHSO3(装置如图所示)。

(1)装置丁的作用有①
(2)将丙中针筒内品红溶液推进锥形瓶中,若发现
(二)小组同学欲探究NaHSO3与
 的反应,经查阅资料后提出假设,并进行实验验证。
的反应,经查阅资料后提出假设,并进行实验验证。已知:氯化亚铜(CuCl)是不溶于水的白色沉淀
假设1:
 与
与 仅发生双水解反应
仅发生双水解反应假设2:
 可以还原
可以还原
设计实验如下:
①向
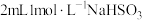 溶液中加入
溶液中加入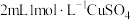 溶液,得到绿色溶液,放置一段时间无明显变化。
溶液,得到绿色溶液,放置一段时间无明显变化。②向①所得绿色溶液中加入适量NaCl固体,开始无明显变化,30s后有无色气体和白色沉淀生成,同时上层溶液颜色变浅。
(3)实验证实假设
(4)甲、乙同学经查阅资料得知,两电极之间的电势差E越大,反应进行的程度越大,电势差
 [其中
[其中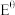 (标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:
(标准电极电势)、R(气体常数)、T(温度)、F(法拉第常数)固定不变],为进一步验证上述结论,设计如下实验:| 编号 | 甲 | 乙 |
| 实验 |  | 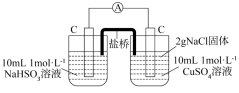 |
②根据相关资料,解释产生上述现象的原因为
您最近一年使用:0次
2 . 下图所选装置和试剂均合理且能达到实验目的的是
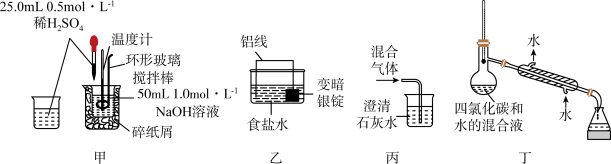

| A.图甲:测定中和热 | B.图乙:洗涤变暗银锭(表面附着Ag2S) |
| C.图丙:检验SO2中混有少量CO2 | D.图丁:分离四氯化碳和水的混合液 |
您最近一年使用:0次
解题方法
3 . 下图所选装置和试剂均合理且能达到实验目的的是
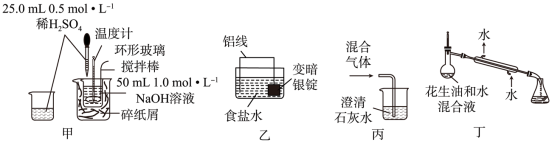

| A.图甲:测定中和热 | B.图乙:洗涤变暗银锭(表面附着Ag2S) |
| C.图丙:检验SO2中混有少量CO2 | D.图丁:分离花生油和水 |
您最近一年使用:0次
名校
4 . 下列实验装置符合实验目的的是
| 目的 | 粗铜的精炼 | 验证含酚酞的饱和氯化钠溶液电解产物 | 铁制品上镀铜 | 将铁和氯化铁溶液反应设计成原电池 |
| 装置 |  |  |  |  |
| 选项 | A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-27更新
|
430次组卷
|
3卷引用:四川省内江市第六中学2020-2021学年高二下学期半期考试化学试题
解题方法
5 . 用a、b、c、d四种金属片进行如下实验,实验装置和现象如下表所示:
据此判断,这四种金属的活动性顺序为
| 装置 |  |  |  |
| 现象 | a电极附近产生大量气泡 | 电子由c电极经导线流向d电极 | 电解质溶液颜色变浅,b电极质量增加 |
| A.a>b>c>d | B.a>b>d>c | C.b>a,b>d>c | D.c>d>b>a |
您最近一年使用:0次
名校
6 . (1)利用原电池装置可以验证Fe3+与Cu2+氧化性相对强弱,如下图所示。

该方案的实验原理是自发进行的氧化还原反应可以设计为原电池。写出该氧化还原反应的离子方程式:__________ 。该装置中的负极材料是______ (填化学式),正极反应式是_______ 。
(2)某研究性学习小组为证明2Fe3++2I-⇌2Fe2++I2为可逆反应,设计如下两种方案。
方案一:
取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,再继续加入2mLCCl4,充分振荡、静置、分层,再取上层清液,滴加KSCN溶液。
①方案一中能证明该反应为可逆反应的现象是______ 。
②有同学认为方案一设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是(用离子方程式表示)_____ 。
方案二:
设计如下图原电池 装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。当指针读数变零后,在右管中加入1mol/L FeCl2溶液。

③方案二中,“读数变为零”是因为____________ .
④“在右管中加入1mol/L FeCl2溶液”后,观察到灵敏电流计的指针______ 偏转(填“向左”、“向右”或“不”),可证明该反应为可逆反应。

该方案的实验原理是自发进行的氧化还原反应可以设计为原电池。写出该氧化还原反应的离子方程式:
(2)某研究性学习小组为证明2Fe3++2I-⇌2Fe2++I2为可逆反应,设计如下两种方案。
方案一:
取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,再继续加入2mLCCl4,充分振荡、静置、分层,再取上层清液,滴加KSCN溶液。
①方案一中能证明该反应为可逆反应的现象是
②有同学认为方案一设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是(用离子方程式表示)
方案二:
设计如下图

③方案二中,“读数变为零”是因为
④“在右管中加入1mol/L FeCl2溶液”后,观察到灵敏电流计的指针
您最近一年使用:0次
7 . 高锰酸钾(KMnO4)和双氧水(H2O2)都是常见的消毒试剂,在日常生活和工业生产中都有广泛的应用。回答下面问题:
(1)酸性高锰酸钾与双氧水混合有气体产生,经检验产生的气体为氧气。写出反应的离子方程式____ 。
(2)H2O2是一种二元弱酸,与NaOH反应的化学方程式为NaOH+H2O=NaHO2+H2O,写出H2O2电离的方程式____ (只写第一步)。在酸性条件下H2O2的分解速度变大,利用平衡移动的原理进行解释:____ 。
(3)现有H2O2-Al燃料电池电解尿素[CO(NH2)2]制备氢气的装置,b、c、d为石墨电极,电解池中的隔膜只阻止气体通过,如图:

①a电极是Al,写出电极反应____ ,反应后b电极区溶液的pH____ (填“增大”“减小”或“不变”)。
②c电极是____ (填“正极”“负极”“阴极”或“阳极”),d电极的电极反应为____ 。
(4)某化学兴趣小组为了探究KMnO4与H2O2氧化性强弱,设计了如图实验装置:

①当闭合电键K时,电流表指针向左偏转,甲烧杯中溶液颜色逐渐变浅,则石墨电极a上发生反应____ (填“氧化”或“还原”),石墨电极b上发生的电极反应为____ 。
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻转,最后向右偏转,说明KMnO4与H2O2氧化性与____ 有关。
(1)酸性高锰酸钾与双氧水混合有气体产生,经检验产生的气体为氧气。写出反应的离子方程式
(2)H2O2是一种二元弱酸,与NaOH反应的化学方程式为NaOH+H2O=NaHO2+H2O,写出H2O2电离的方程式
(3)现有H2O2-Al燃料电池电解尿素[CO(NH2)2]制备氢气的装置,b、c、d为石墨电极,电解池中的隔膜只阻止气体通过,如图:

①a电极是Al,写出电极反应
②c电极是
(4)某化学兴趣小组为了探究KMnO4与H2O2氧化性强弱,设计了如图实验装置:

①当闭合电键K时,电流表指针向左偏转,甲烧杯中溶液颜色逐渐变浅,则石墨电极a上发生反应
②反应一段时间后,向甲烧杯中滴加KOH溶液,同时向乙烧杯中滴加硫酸溶液,发现电流表指针逐渐翻转,最后向右偏转,说明KMnO4与H2O2氧化性与
您最近一年使用:0次
2022-11-02更新
|
212次组卷
|
2卷引用:河南省许平汝联盟2022-2023学年高二上学期期中联考化学试题
解题方法
8 . 有关下列实验装置的说法中正确的是
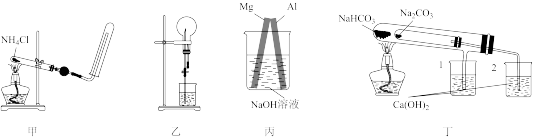
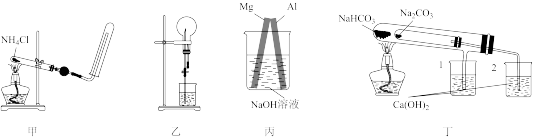
| A.实验室用装置甲制备少量氨气 |
| B.选用合适的溶液,HCl、NH3、CO2和SO2均能用装置乙作喷泉实验 |
| C.装置丙中Mg电极上出现气泡,说明Al的活泼性比Mg强 |
| D.装置丁可用于比较Na2CO3和NaHCO3的热稳定性 |
您最近一年使用:0次
2022-04-24更新
|
276次组卷
|
3卷引用:浙江省宁波市六校2021-2022学年高一下学期期中联考化学试题
名校
9 . 填空。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极b作
的原理示意图。电极b作_______ 极,表面发生的电极反应为_______ 。

(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如下图所示,该电池从浓缩海水中提取 的同时又获得了电能。
的同时又获得了电能。
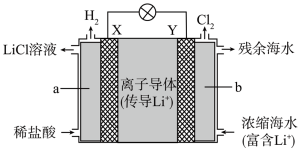
①X为_______ 极,Y极反应式为_______ 。
②Y极生成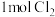 时,
时,_______ 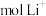 移向
移向_______ (填“X”或“Y”)极。
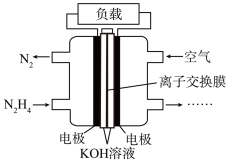
(3)一种以肼(N2H4)为液体燃料的电池装置如下图所示。该电池用空气中的氧气作氧化剂, 作电解质。负极反应式为
作电解质。负极反应式为_______ ;正极反应式为_______ 。
(1)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。下图是通过人工光合作用,以
 和
和 为原料制备
为原料制备 和
和 的原理示意图。电极b作
的原理示意图。电极b作
(2)浓差电池中的电动势是由于电池中存在浓度差而产生的。某浓差电池的原理如下图所示,该电池从浓缩海水中提取
 的同时又获得了电能。
的同时又获得了电能。
①X为
②Y极生成
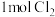 时,
时,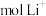 移向
移向(3)一种以肼(N2H4)为液体燃料的电池装置如下图所示。该电池用空气中的氧气作氧化剂,
 作电解质。负极反应式为
作电解质。负极反应式为
您最近一年使用:0次
解题方法
10 . 近日,科学家设计一种具有石墨正极的高容量可充电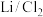 锂金属电池,原理如图所示。氯化铝(
锂金属电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(
)中,以氟化物( )为添加剂作为电解质。回答下列问题:
)为添加剂作为电解质。回答下列问题:
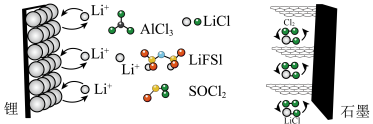
(1)放电时,能量主要转化形式是___________ 。
(2)放电时,锂离子由___________ (填“锂”或“石墨”,下同)极向___________ 极迁移,石墨极反应式为___________ 。
(3)充电时,石墨极与电源___________ (填“正”或“负”)极连接。转移 个电子时锂电极理论上净增
个电子时锂电极理论上净增___________ g锂( 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(4)该装置不能使用水、醇、酸作溶剂,其理由是___________ 。
(5) 在
在 中完全燃烧放出热量为
中完全燃烧放出热量为 。写出热化学方程式:
。写出热化学方程式:___________ 。
(6)工业上制备亚硫酰氯: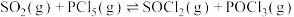
 。下列措施能提高
。下列措施能提高 平衡转化率的是___________(填字母)。
平衡转化率的是___________(填字母)。
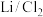 锂金属电池,原理如图所示。氯化铝(
锂金属电池,原理如图所示。氯化铝( )溶解在亚硫酰氯(
)溶解在亚硫酰氯( )中,以氟化物(
)中,以氟化物( )为添加剂作为电解质。回答下列问题:
)为添加剂作为电解质。回答下列问题: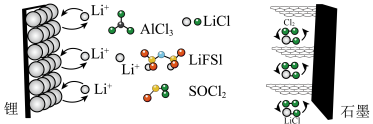
(1)放电时,能量主要转化形式是
(2)放电时,锂离子由
(3)充电时,石墨极与电源
 个电子时锂电极理论上净增
个电子时锂电极理论上净增 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(4)该装置不能使用水、醇、酸作溶剂,其理由是
(5)
 在
在 中完全燃烧放出热量为
中完全燃烧放出热量为 。写出热化学方程式:
。写出热化学方程式:(6)工业上制备亚硫酰氯:
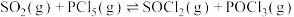
 。下列措施能提高
。下列措施能提高 平衡转化率的是___________(填字母)。
平衡转化率的是___________(填字母)。| A.升高温度 | B.增大压强 | C.加入催化剂 | D.分离 |
您最近一年使用:0次



