1 . 以甲醇为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。
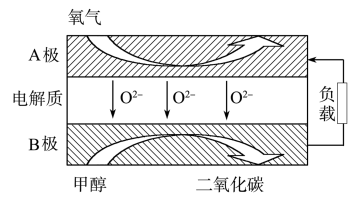
回答下列问题:
(1)B极上的电极反应式为_______ 。
(2)若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到33.6L(标准状况)气体时,消耗甲醇的质量为_______ g,若要使溶液复原,可向电解后的溶液中加入的物质有_______ 。
(3)目前已开发出用电解法制取ClO2的新工艺。
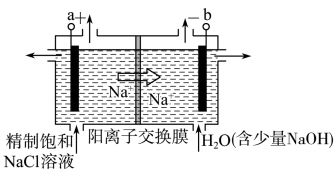
①如图示意用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。若用上述甲醇燃料电池进行电解,则电解池的电极a接甲醇燃料电池的_______ (填“A”或“B”)极,写出阳极产生ClO2的电极反应式:_______ 。
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为_______ mol。

回答下列问题:
(1)B极上的电极反应式为
(2)若用该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到33.6L(标准状况)气体时,消耗甲醇的质量为
(3)目前已开发出用电解法制取ClO2的新工艺。

①如图示意用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。若用上述甲醇燃料电池进行电解,则电解池的电极a接甲醇燃料电池的
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解。通过阳离子交换膜的阳离子的物质的量为
您最近一年使用:0次
名校
解题方法
2 . 一种应用比较广泛的甲醇燃料电池,电解液是酸性溶液,其工作原理如图所示,下列说法正确的是


A.若有 生成,则有 生成,则有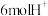 从甲池通过交换膜进入乙池 从甲池通过交换膜进入乙池 |
B.N极电极反应为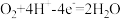 |
C.甲池溶液 增大,乙池溶液 增大,乙池溶液 减小 减小 |
| D.M极为负极,发生还原反应 |
您最近一年使用:0次
2021-11-20更新
|
628次组卷
|
4卷引用:河北省张家口市宣化第一中学2021-2022学年高二上学期期中考试化学试题
河北省张家口市宣化第一中学2021-2022学年高二上学期期中考试化学试题(已下线)第25讲 化学电源(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)江苏省宿迁市北大附属宿迁实验学校2022-2023学年高二上学期开学考试化学试题辽宁省朝阳市建平县高级中学2021-2022学年高二上学期第二次月考化学试题
解题方法
3 . 请回答下列问题:
(1)由A、B、C、D四种金属按下表装置图进行实验。
根据实验现象回答问题:四种金属活动性由强到弱的顺序是___________ 。
(2)某兴趣小组的同学以甲醇燃料电池为电源研究有关电化学的问题。

①甲池中,通入甲醇一极的电极反应式为___________ 。
②乙池中,B极 石墨
石墨 电极的电极反应式为
电极的电极反应式为___________ 。
③丙池中,通电前C、D两电极的质量相同,通电一段时间后。
a.溶液中c(Ag+)将___________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
b.两极的质量相差17.28g,则甲池中消耗O2的体积为___________ mL(标准状况下 。
。
 丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。
丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。
a.Ti电极附近溶液的碱性将___________  填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。
b.Cu电极的电极反应式为___________ 。
(1)由A、B、C、D四种金属按下表装置图进行实验。
| 装置 |  |  |  |
| 现象 | 金属A不断溶解 | C极质量增加 | A上有气体产生 |
(2)某兴趣小组的同学以甲醇燃料电池为电源研究有关电化学的问题。

①甲池中,通入甲醇一极的电极反应式为
②乙池中,B极
 石墨
石墨 电极的电极反应式为
电极的电极反应式为③丙池中,通电前C、D两电极的质量相同,通电一段时间后。
a.溶液中c(Ag+)将
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。b.两极的质量相差17.28g,则甲池中消耗O2的体积为
 。
。 丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。
丁池中,利用离子交换膜控制电解液中c(OH-)来制备纳米Cu2O,离子交换膜为阴离子交换膜。a.Ti电极附近溶液的碱性将
 填“增大”“减小”或“不变”
填“增大”“减小”或“不变” 。
。b.Cu电极的电极反应式为
您最近一年使用:0次
名校
4 . 按要求书写
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是_______ (填“化学腐蚀”或“电化学腐蚀”)
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为_______
(3)书写基态铜原子价电子排布轨道表达式_______
(4)甲醇燃料电池(氢氧化钾作电解质溶液)负极电极方程式_______
(5)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式_______
(1)炒菜用的铸铁锅不用时会因腐蚀而出现红褐色锈斑,这时铁锅的锈蚀主要是
(2)基态Fe2+与Fe3+离子中未成对的电子数之比为
(3)书写基态铜原子价电子排布轨道表达式
(4)甲醇燃料电池(氢氧化钾作电解质溶液)负极电极方程式
(5)镓(Ga)与铝同族。写出镓的氯化物和氨水反应的化学方程式
您最近一年使用:0次
名校
5 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流表的指针发生了偏转。请回答下列问题:
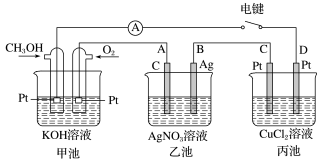
(1)甲池为___ (填“原电池”“电解池”或“电镀池”),通入CH3OH电极的电极反应式为___ 。甲池溶液pH值___ (填升高、降低或不变)
(2)乙池中A(石墨)电极的名称为___ (填“正极”“负极”“阴极”或“阳极”),总反应式为__ 。
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为___ mL(标准状况下),丙池中__ 极析出___ g铜。

(1)甲池为
(2)乙池中A(石墨)电极的名称为
(3)当乙池中B极质量增加5.40g时,甲池中理论上消耗O2的体积为
您最近一年使用:0次
解题方法
6 . 2018年,美国退出了《巴黎协定》实行在工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年来我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究。实现可持续发展。
(1)以CO2(g)和H2(g)为原料合成甲醇,反应过程的能量变化如图所示
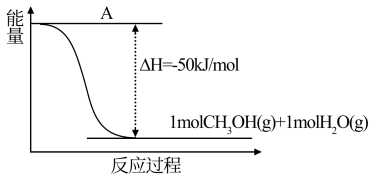
①补全上图:图中A处应填入__________ 。
②该反应需要加入钢-锌基催化剂。加入催化刺后。该反应的△H_______ (填“变大”“变小”“不变”)
③为提高CH3OH的产率。理论上规采用的反应条件是________ 。(填字母)。
a.高温高压 b.低温低压 c.高温低压 d.低温高压
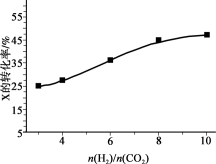
(2)250℃,在恒容密闭容器中由CO2催化氢化合成CH3OH(g)。如图为不同投料比(n(H2)/n(CO2)时某反应物X的平衡转化率变化曲线。反应物X是____ (填CO2或H2)。
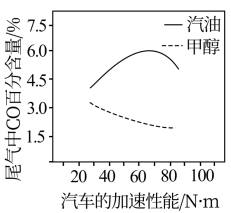
(3)甲醇可以替代汽油和柴油作为内燃机燃料。某研究者分别以甲醇和汽油做燃料。实骑侧得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。根据图信息分析,与汽油相比。甲醇作为燃料的优点是_______ 。
(4)250℃在容积为2.0L的恒容密闭容器中加入6molH2、2molCO2,和催化剂。10min时反应达到平衡,测得c(CH3OH)=0.75mol∙L-1
①10min的平均反应速率v(H2)=______ ;
②该温度下平衡常数K的数值为_____ (结果保留两位小数)。
(1)以CO2(g)和H2(g)为原料合成甲醇,反应过程的能量变化如图所示

①补全上图:图中A处应填入
②该反应需要加入钢-锌基催化剂。加入催化刺后。该反应的△H
③为提高CH3OH的产率。理论上规采用的反应条件是
a.高温高压 b.低温低压 c.高温低压 d.低温高压
(2)250℃,在恒容密闭容器中由CO2催化氢化合成CH3OH(g)。如图为不同投料比(n(H2)/n(CO2)时某反应物X的平衡转化率变化曲线。反应物X是

(3)甲醇可以替代汽油和柴油作为内燃机燃料。某研究者分别以甲醇和汽油做燃料。实骑侧得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如图所示。根据图信息分析,与汽油相比。甲醇作为燃料的优点是

(4)250℃在容积为2.0L的恒容密闭容器中加入6molH2、2molCO2,和催化剂。10min时反应达到平衡,测得c(CH3OH)=0.75mol∙L-1
①10min的平均反应速率v(H2)=
②该温度下平衡常数K的数值为
您最近一年使用:0次
2021-11-06更新
|
90次组卷
|
2卷引用:山西省太原市第五十六中学2021-2022学年高二上学期10月月考化学试题
解题方法
7 . 某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键 时,观察到电流表的指针发生了偏转。请回答下列问题:
时,观察到电流表的指针发生了偏转。请回答下列问题:

(1)乙池为___________ (填“原电池”“电解池”“电镀池”), 电极的电极反应式为:
电极的电极反应式为:___________ 。
(2)丙池中 电极为
电极为___________ (填“正极”、“负极”、“阴极”或“阳极”),写出电解时总反应的离子方程式___________ 。
(3)当乙池中 极质量变化
极质量变化 时,甲池中
时,甲池中 电极理论上消耗
电极理论上消耗 的体积为
的体积为___________  (标准状况)。
(标准状况)。
(4)一段时间后,断开电键 。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。
。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。
(5)若丙池通电一段时间后,向所得的溶液中加入 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和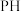 (不考虑
(不考虑 的溶解),则电解过程中转移的电子
的溶解),则电解过程中转移的电子___________  。
。
 时,观察到电流表的指针发生了偏转。请回答下列问题:
时,观察到电流表的指针发生了偏转。请回答下列问题:
(1)乙池为
 电极的电极反应式为:
电极的电极反应式为:(2)丙池中
 电极为
电极为(3)当乙池中
 极质量变化
极质量变化 时,甲池中
时,甲池中 电极理论上消耗
电极理论上消耗 的体积为
的体积为 (标准状况)。
(标准状况)。(4)一段时间后,断开电键
 。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。
。下列物质能使乙池恢复到反应前浓度的是___________(填选项字母)。A. | B. | C. | D. |
 后恰好恢复到电解前的浓度和
后恰好恢复到电解前的浓度和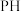 (不考虑
(不考虑 的溶解),则电解过程中转移的电子
的溶解),则电解过程中转移的电子 。
。
您最近一年使用:0次
8 . Ⅰ.某研究性学习小组,为了探究电极与原电池的电解质之间关系,设计了下列实验方案:用铝片、铜片、镁片作电极,分别与下列溶液构成原电池,并接电流表。
(1)若电解质溶液为0.5mol/L硫酸,电极为铜片和铝片,铝片上的电极的反应式为___________ 。
(2)若用浓硝酸作电解质溶液,电极为铜片和铝片,铝片为___________ 极(填“正”或“负”)。正极上发生的电极反应式为___________ 。
(3)若电解质溶液为0.5mol/L氢氧化钠溶液,电极为镁片和铝片,则正极发生的电极反应为_____ 。
Ⅱ.肼( )又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
(4)肼-空气燃料电池放电时:正极的电极反应式是___________ 。
(1)若电解质溶液为0.5mol/L硫酸,电极为铜片和铝片,铝片上的电极的反应式为
(2)若用浓硝酸作电解质溶液,电极为铜片和铝片,铝片为
(3)若电解质溶液为0.5mol/L氢氧化钠溶液,电极为镁片和铝片,则正极发生的电极反应为
Ⅱ.肼(
 )又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。
)又称联氨,在常温下是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。(4)肼-空气燃料电池放电时:正极的电极反应式是
您最近一年使用:0次
名校
解题方法
9 . 甲醇是一种重要的化工原料,具有开发和应用的广阔前景。
(1)已知甲醇燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OHg+H2Og=CO2g+3H2g ΔH=49.0kJ•mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ•mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ•mol-1
又知:③H2Og=H2Ol ΔH=-44kJ•mol-1
则表示甲醇摩尔燃烧焓的热化学方程式为_____ 。
II.如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:

(2)甲池燃料电池的负极反应方程式为_____ 。
(3)写出乙池中电解总反应的化学方程式:_____ 。
(4)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生______ g沉淀,此时乙池中溶液的体积为400mL,该溶液的c(H+)=______ 。
(5)若以该甲醇燃料电池为电源,用石墨做电极电解200mL含有如下离子的溶液。
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),电路中转移的电子的物质的量是_____ mol。
(1)已知甲醇燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OHg+H2Og=CO2g+3H2g ΔH=49.0kJ•mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ•mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9kJ•mol-1又知:③H2Og=H2Ol ΔH=-44kJ•mol-1
则表示甲醇摩尔燃烧焓的热化学方程式为
II.如图所示,其中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:

(2)甲池燃料电池的负极反应方程式为
(3)写出乙池中电解总反应的化学方程式:
(4)甲池中消耗224mL(标准状况下)O2,此时丙池中理论上最多产生
(5)若以该甲醇燃料电池为电源,用石墨做电极电解200mL含有如下离子的溶液。
| 离子 | Cu2+ | H+ | Cl- | SO |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象),电路中转移的电子的物质的量是
您最近一年使用:0次
2021-11-01更新
|
309次组卷
|
2卷引用:山东省济钢高级中学2021-2022学年高二上学期第二次教学检测化学试题
解题方法
10 .  是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料,已知
是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料,已知 的能量变化如图所示。
的能量变化如图所示。

(1)下列说法正确的是_______ (填字母)。
 .CH3OH转变成
.CH3OH转变成 的过程是一个吸收能量的过程
的过程是一个吸收能量的过程
 .
. 的生成速率与CH3OH的消耗速率之比为1:2
的生成速率与CH3OH的消耗速率之比为1:2
 .化学变化不仅有新物质生成,同时也一定有能量变化
.化学变化不仅有新物质生成,同时也一定有能量变化
 .1molO-H键断裂的同时1molC-C键断裂,则反应达最大限度
.1molO-H键断裂的同时1molC-C键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得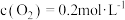 ,4min内平均反应速率
,4min内平均反应速率 =
=_______ ,则CH3OH的转化率为_______ 。
(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的工作原理示意图如图所示,a、b均为惰性电极。
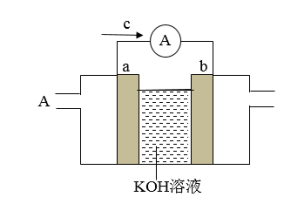
①A口通入的气体为_______ (填名称)。
②负极反应式为_______ 。
 是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料,已知
是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料,已知 的能量变化如图所示。
的能量变化如图所示。
(1)下列说法正确的是
 .CH3OH转变成
.CH3OH转变成 的过程是一个吸收能量的过程
的过程是一个吸收能量的过程 .
. 的生成速率与CH3OH的消耗速率之比为1:2
的生成速率与CH3OH的消耗速率之比为1:2 .化学变化不仅有新物质生成,同时也一定有能量变化
.化学变化不仅有新物质生成,同时也一定有能量变化 .1molO-H键断裂的同时1molC-C键断裂,则反应达最大限度
.1molO-H键断裂的同时1molC-C键断裂,则反应达最大限度(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得
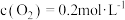 ,4min内平均反应速率
,4min内平均反应速率 =
=(3)CH3OH燃料电池是目前开发最成功的燃料电池之一,这种燃料电池由甲醇、空气(氧气)、KOH(电解质溶液)构成。电池的工作原理示意图如图所示,a、b均为惰性电极。

①A口通入的气体为
②负极反应式为
您最近一年使用:0次



