名校
解题方法
1 . 微生物燃料电池是一种利用微生物将化学能直接转化成电能的装置。已知某种甲醇微生物燃料电池中,电解质溶液为酸性,示意图如图。下列说法正确的是
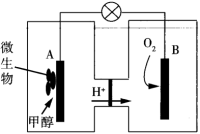

| A.该电池中外电路电子的流动方向为从B到A |
| B.A极的电极反应式为CH3OH+H2O-6e-=6H++CO2↑ |
| C.电池工作一段时间后,正、负极消耗或产生气体的物质的量相同 |
| D.工作结束后,B极室溶液的pH与工作前相同 |
您最近一年使用:0次
解题方法
2 . 其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

(1)甲池中,通入甲醇电极反应式为___________ 。
(2)甲池是___________ 装置,乙池是___________ 装置。
(3)乙池中,总反应式为___________ 。
(4)若甲池中甲醇与氧气互换,则乙池中,A端反应式为___________ ,B端现象为___________ 。

(1)甲池中,通入甲醇电极反应式为
(2)甲池是
(3)乙池中,总反应式为
(4)若甲池中甲醇与氧气互换,则乙池中,A端反应式为
您最近一年使用:0次
2022-08-03更新
|
154次组卷
|
2卷引用:天津市静海区四校2021-2022学年高二上学期12月份阶段性检测化学试题
3 . 二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳的排放。
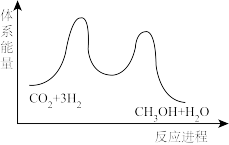
(1)二氧化碳加氢制甲醇的总反应为 ,能量变化如图所示,该反应为
,能量变化如图所示,该反应为_______ (“放热”或“吸热”)反应。
(2)在恒温恒容条件下进行二氧化碳加氢制甲醇反应。起始时,向反应容器中充入 和
和 ,反应达到平衡时生成
,反应达到平衡时生成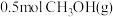 。
。
①下列能够说明总反应已达到化学平衡状态的是_______ (填标号)。
A.气体的平均相对分子质量保持不变 B.容器内总压强不再改变
C. 的比值保持不变 D.
的比值保持不变 D. 的体积分数不再改变
的体积分数不再改变
②达到平衡时, 的转化率是
的转化率是_______ ,容器内起始压强与平衡压强之比是_______ 。
(3)一定条件下,将 与
与 以体积比1∶2置于密闭容器中发生上述反应,测定甲醇时空收率随温度的变化曲线如图所示,已知:甲醇时空收率表示在1mol催化剂表面,生成甲醇的平均速率。
以体积比1∶2置于密闭容器中发生上述反应,测定甲醇时空收率随温度的变化曲线如图所示,已知:甲醇时空收率表示在1mol催化剂表面,生成甲醇的平均速率。
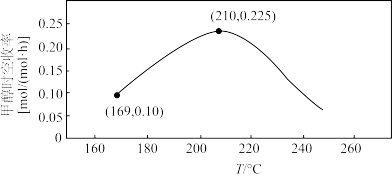
①使用1mol活性镓镍催化剂时,若反应温度由169℃升高到210℃,生成甲醇的平均速率之比
_______ 。
②温度高于210℃时,甲醇时空收率降低的原因可能是_______ 。
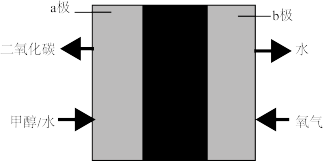
(4)直接甲醇燃料电池工作原理如图所示。a极是电池的_______ (“正极”或“负极”),b极电极反应式为_______ 。
(1)二氧化碳加氢制甲醇的总反应为
 ,能量变化如图所示,该反应为
,能量变化如图所示,该反应为
(2)在恒温恒容条件下进行二氧化碳加氢制甲醇反应。起始时,向反应容器中充入
 和
和 ,反应达到平衡时生成
,反应达到平衡时生成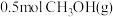 。
。①下列能够说明总反应已达到化学平衡状态的是
A.气体的平均相对分子质量保持不变 B.容器内总压强不再改变
C.
 的比值保持不变 D.
的比值保持不变 D. 的体积分数不再改变
的体积分数不再改变②达到平衡时,
 的转化率是
的转化率是(3)一定条件下,将
 与
与 以体积比1∶2置于密闭容器中发生上述反应,测定甲醇时空收率随温度的变化曲线如图所示,已知:甲醇时空收率表示在1mol催化剂表面,生成甲醇的平均速率。
以体积比1∶2置于密闭容器中发生上述反应,测定甲醇时空收率随温度的变化曲线如图所示,已知:甲醇时空收率表示在1mol催化剂表面,生成甲醇的平均速率。
①使用1mol活性镓镍催化剂时,若反应温度由169℃升高到210℃,生成甲醇的平均速率之比

②温度高于210℃时,甲醇时空收率降低的原因可能是
(4)直接甲醇燃料电池工作原理如图所示。a极是电池的

您最近一年使用:0次
2022-08-01更新
|
445次组卷
|
2卷引用:山东省淄博市2021-2022学年高一下学期期末考试化学试题
4 . 甲醇是重要的工业原料和燃料。
(1)甲醇燃料电池(DMFC)为现代便携式电子产品提供了电能。在以KOH为电解质的甲醇燃料电池中,CH3OH在电源_______ (填“正”或“负”)极反应,当电路中转移0.6mol电子时,消耗CH3OH的物质的量是_______ ;该电池工作一段时间后,电解质溶液的pH_______ (填“增大”“减小”或“不变”)。
(2)利用甲醇通过惰性电解法先获得α-羟基缩酮,α-羟基缩酮再在酸性条件下水解得到一种食品增香剂3-羟基丁酮,其原理如图所示。
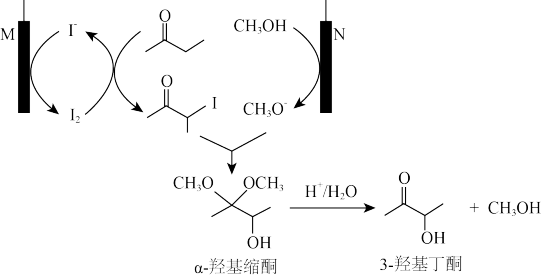
①M极上发生_______ (填“氧化反应”或“还原反应”)。
②N为电解池的_______ 极(填“阴”或“阳”),电极反应式是_______ 。
③此法合成3-羟基丁酮的总反应式是_______ (不用写反应条件)。
(1)甲醇燃料电池(DMFC)为现代便携式电子产品提供了电能。在以KOH为电解质的甲醇燃料电池中,CH3OH在电源
(2)利用甲醇通过惰性电解法先获得α-羟基缩酮,α-羟基缩酮再在酸性条件下水解得到一种食品增香剂3-羟基丁酮,其原理如图所示。

①M极上发生
②N为电解池的
③此法合成3-羟基丁酮的总反应式是
您最近一年使用:0次
2022-07-11更新
|
96次组卷
|
2卷引用:河南省南阳市六校2021-2022学年高二下学期6月联考化学试题
5 . 甲醇( )是应用广泛的化工原料和前景乐观的燃料。
)是应用广泛的化工原料和前景乐观的燃料。
Ⅰ.一定条件下,在5L密闭容器中充入1mol 和3 mol
和3 mol ,发生反应:
,发生反应: 。测得
。测得 和
和 的物质的量随时间变化如图所示。据图回答下列问题。
的物质的量随时间变化如图所示。据图回答下列问题。

(1)x=_______ ;0~3min内 的平均反应速率
的平均反应速率
_______ mol/(L·min)。
(2)下列措施能提高正反应速率的是_______(填字母)。
Ⅱ.甲醇燃料电池可使甲醇作燃料时的能量转化更高效,某种甲醇燃料电池的工作原理如图所示,其电极反应如下:


(3)电极A的名称是_______ (填“正极”或“负极”);甲醇从_______ (填“b”或“c”)处通入。
(4)甲醇燃料电池供电时的总反应方程式为_______
(5)当该装置消耗64g甲醇时,转移电子的数目为_______ ;若这部分电子全部用于电解水,理论上可产生标准状况下氢气_______ L。
 )是应用广泛的化工原料和前景乐观的燃料。
)是应用广泛的化工原料和前景乐观的燃料。Ⅰ.一定条件下,在5L密闭容器中充入1mol
 和3 mol
和3 mol ,发生反应:
,发生反应: 。测得
。测得 和
和 的物质的量随时间变化如图所示。据图回答下列问题。
的物质的量随时间变化如图所示。据图回答下列问题。
(1)x=
 的平均反应速率
的平均反应速率
(2)下列措施能提高正反应速率的是_______(填字母)。
| A.降低温度 | B.增加 的量 的量 |
| C.及时分离出甲醇 | D.使用催化剂 |
Ⅱ.甲醇燃料电池可使甲醇作燃料时的能量转化更高效,某种甲醇燃料电池的工作原理如图所示,其电极反应如下:



(3)电极A的名称是
(4)甲醇燃料电池供电时的总反应方程式为
(5)当该装置消耗64g甲醇时,转移电子的数目为
您最近一年使用:0次
名校
解题方法
6 . 2022年2月在北京举办了冬季奥运会,冬奥会奖牌是金镶玉材料,而玉的成分是硅酸盐和二氧化硅,回答下面问题:
(1)向硅酸钠溶液中通入少量CO2,生成一种凝胶硅酸,写出反应的离子方程式:_______ 。
(2)工业上可以用CO2来生产甲醇(CH3OH)燃料。在体积为2 L的密闭容器中,充入1 molCO2和3 mol H2,一定条件下发生反应CO2(g) +3H2(g) CH3OH(g) +H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示:
CH3OH(g) +H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示:
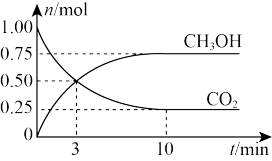
①反应开始到10 min, 用CO2表示的反应速率为。_______
②达到平衡时,H2的转化率为_______
③达到平衡后,下列措施中,能使正反应速率增大的有_______ (填字母)。
A.充入一定量CO2 B.充入一定量的Ar
C.改用催化效率更高的催化剂 D.容器体积扩大至原来2倍
(3)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇。
①写出甲醇燃烧的化学方程式:_______ ;
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:

a电极是_______ 极,将上图中的H2改为甲醇就构成了碱性甲醇燃料电池,a电极发生的电极反应式是_______ 。
(1)向硅酸钠溶液中通入少量CO2,生成一种凝胶硅酸,写出反应的离子方程式:
(2)工业上可以用CO2来生产甲醇(CH3OH)燃料。在体积为2 L的密闭容器中,充入1 molCO2和3 mol H2,一定条件下发生反应CO2(g) +3H2(g)
 CH3OH(g) +H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示:
CH3OH(g) +H2O(g)。测得CH3OH和CO2的物质的量随时间变化如图所示:
①反应开始到10 min, 用CO2表示的反应速率为。
②达到平衡时,H2的转化率为
③达到平衡后,下列措施中,能使正反应速率增大的有
A.充入一定量CO2 B.充入一定量的Ar
C.改用催化效率更高的催化剂 D.容器体积扩大至原来2倍
(3)北京冬奥会基本实现100%绿电供应和碳中和,利用CO2和H2在光催化酶作用下可以高效合成甲醇。
①写出甲醇燃烧的化学方程式:
②氢气燃料电池和甲醇燃料电池在北京冬奥会上得到广泛应用。如图是碱性氢燃料电池的模拟示意图:

a电极是
您最近一年使用:0次
2022-05-24更新
|
137次组卷
|
2卷引用:山西省太原师范学院附属中学、太原市师苑中学校2021-2022学年高一下学期第四次月考化学试题
名校
解题方法
7 . 我国科学家成功利用 人工合成淀粉,使淀粉生产方式从农业种植转为工业制造成为可能,其原理如下所示。下列说法错误的是
人工合成淀粉,使淀粉生产方式从农业种植转为工业制造成为可能,其原理如下所示。下列说法错误的是
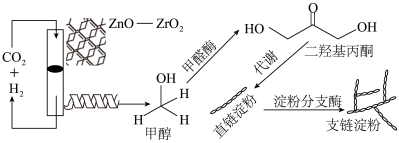
 人工合成淀粉,使淀粉生产方式从农业种植转为工业制造成为可能,其原理如下所示。下列说法错误的是
人工合成淀粉,使淀粉生产方式从农业种植转为工业制造成为可能,其原理如下所示。下列说法错误的是 
| A.甲醇可用于燃料电池的正极反应物 |
| B.淀粉可用于制备葡萄糖 |
| C.该过程有利于实现“碳达峰,碳中和” |
| D.化妆品中添加二羟基丙酮的主要作用为保湿 |
您最近一年使用:0次
2022-05-20更新
|
205次组卷
|
2卷引用:山东省烟台市第二中学等校2021-2022学年高二下学期期中考试化学试题
名校
解题方法
8 . 甲醇是重要的燃料,化学教材《选择性必修1》100页第5题介绍了甲醇( )酸性燃料电池,资料显示其结构如图所示。
)酸性燃料电池,资料显示其结构如图所示。

(1)A为燃料电池的_______ (填“正”或“负”)极, 在其表面发生
在其表面发生_______ 反应(填“氧化”或“还原”)。
(2)放电过程中,经过交换膜时, 的迁移方向是
的迁移方向是_______ (填“A→B”或“B→A”)。
(3)正极反应式_______ 。
(4)负极反应式为_______ 。
(5)在电池反应中,每生成1mol二氧化碳,理论上消耗标准状况下氧气的体积是_______ 。
(6)在25℃、101kPa下,1g液态甲醇燃烧生成 和液态水时放热22.5kJ,其热化学方程式为
和液态水时放热22.5kJ,其热化学方程式为_______ ;研究表明,甲醇用于火力发电的能量转化率_______ 于燃料电池(填“高”或“低”)。
(7)合成甲醇的反应为: △H。已知CO的结构式为
△H。已知CO的结构式为 ,甲醇的结构式为
,甲醇的结构式为 ,相关键能数据如下:
,相关键能数据如下:
由此计算△H=_______  。
。
 )酸性燃料电池,资料显示其结构如图所示。
)酸性燃料电池,资料显示其结构如图所示。
(1)A为燃料电池的
 在其表面发生
在其表面发生(2)放电过程中,经过交换膜时,
 的迁移方向是
的迁移方向是(3)正极反应式
(4)负极反应式为
(5)在电池反应中,每生成1mol二氧化碳,理论上消耗标准状况下氧气的体积是
(6)在25℃、101kPa下,1g液态甲醇燃烧生成
 和液态水时放热22.5kJ,其热化学方程式为
和液态水时放热22.5kJ,其热化学方程式为(7)合成甲醇的反应为:
 △H。已知CO的结构式为
△H。已知CO的结构式为 ,甲醇的结构式为
,甲醇的结构式为 ,相关键能数据如下:
,相关键能数据如下:| 化学键 | H-H | C-O |  | H-O | C-H |
 | 436 | 343 | 1076 | 465 | 413 |
 。
。
您最近一年使用:0次
解题方法
9 . 甲醇(CH3OH)燃料电池可以作为笔记本电脑、汽车等的能量来源,其工作原理如下图所示。下列说法正确的是


| A.放电过程中,电能转化成化学能 |
| B.放电过程中,H+由a极区向b极区迁移 |
| C.电极a上反应为CH3OH+ H2O-4e- =CO2↑+ 6H+ |
| D.放电过程中1 mol CH3OH参与反应,理论上需通入33.6 LO2 |
您最近一年使用:0次
名校
解题方法
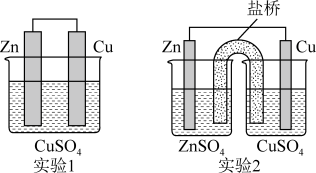
10 . 成都外国语学校化学兴趣小组探究了原电池、电解池的相关工作原理。
(1)小组同学进行了如下两个实验,其中电池工作效率更高的应是实验_______ 。实验2中,盐桥(含KCl饱和溶液的琼胶)中K+流向_______ (选填“ZnSO4”或“CuSO4”)溶液,如果Zn的消耗速率为1×10-3mol·s-1,则K+的迁移速率为_______ mol·s-1。
(2)小组同学分析研究甲醇和氧气以强碱(用NaOH表示)做电解质溶液的新型电池。甲醇在_______ 极反应;电极反应式为_______ 。
(3)小组同学设计了如下装置,用电解法把Na2CrO4转化为Na2Cr2O7。
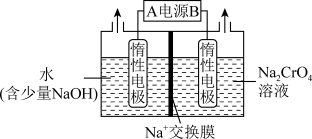
电解过程中,Na+的移动方向为_______ (填“左至右”或“右至左”)。Na2Cr2O7在阳极区产生的原理为_______ 。
(1)小组同学进行了如下两个实验,其中电池工作效率更高的应是实验

(2)小组同学分析研究甲醇和氧气以强碱(用NaOH表示)做电解质溶液的新型电池。甲醇在
(3)小组同学设计了如下装置,用电解法把Na2CrO4转化为Na2Cr2O7。

电解过程中,Na+的移动方向为
您最近一年使用:0次



