名校
解题方法
1 . 以V2O5为原料制备氧钒(Ⅳ)碱式碳酸铵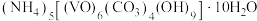 .其过程
.其过程 溶液
溶液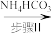 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品
已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为___________ ,使用此仪器的优点是_________________________ 。
②步骤Ⅰ生成 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为_____________________________________ 。
(2)步骤Ⅱ可在如下图装置中进行.
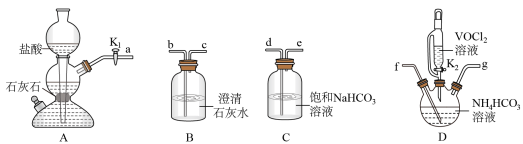
①接口的连接顺序为
___________ 。
②实验开始时,关闭 ,打开
,打开 ,其目的是
,其目的是__________________________ .当___________ 时(写实验现象),再关闭 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。
(3)测定产品纯度
称取 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。
(已知: )
)
产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为 )的质量分数为
)的质量分数为___________ 。
(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.
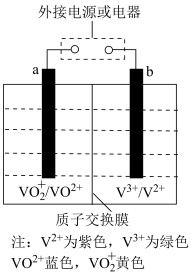
其充电时,阳极的电极方程式为_______________________________________ 。
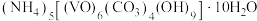 .其过程
.其过程 溶液
溶液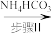 氧钒(Ⅳ)碱式碳酸铵粗产品
氧钒(Ⅳ)碱式碳酸铵粗产品已知VO2+能被O2氧化,回答下列问题:
(1)步骤Ⅰ的反应装置如右图(夹持及加热装置略去)

①仪器a的名称为
②步骤Ⅰ生成
 的同时,还生成一种无色无污染的气体,该反应的化学方程式为
的同时,还生成一种无色无污染的气体,该反应的化学方程式为(2)步骤Ⅱ可在如下图装置中进行.

①接口的连接顺序为

②实验开始时,关闭
 ,打开
,打开 ,其目的是
,其目的是 ,打开
,打开 ,充分反应,静置,得到固体。
,充分反应,静置,得到固体。(3)测定产品纯度
称取
 氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以
氧钒(Ⅳ)碱式碳酸铵粗产品经处理后,钒(V)元素均以 的形式存在,然后用
的形式存在,然后用 标准溶液滴定达终点时,消耗体积为
标准溶液滴定达终点时,消耗体积为 。
。(已知:
 )
)产品中氧钒(Ⅳ)碱式碳酸铵(摩尔质量为
 )的质量分数为
)的质量分数为(4)全钒液流电池是一种新型的绿色环保储能电池,工作原理如图所示,a、b均为惰性电极,放电时左槽溶液颜色由黄色变为蓝色.

其充电时,阳极的电极方程式为
您最近一年使用:0次
名校
解题方法
2 . 新型锂电池的电极材料LiFePO4可通Li2CO3+H2C2O4+2FePO4=2LiFePO4+H2O+3CO2制得。该电池充电时,LiFePO4变成Li1-xFePO4(0<x<1)。(在制备和充电时:H、Li、P、O化合价不变,分别为+1、+1、+5、-2)。下列说法正确的是
| A.该制备原理中H2C2O4作氧化剂 |
| B.由LiFePO4变成Li1-xFePO4时,属于还原反应 |
| C.常温常压下生成4.4gCO2时,反应中转移0.1mol电子 |
| D.当Li1-xFePO4中x=0.4时,Li1-xFePO4中的Fe2+和Fe3+的个数值比为3∶2 |
您最近一年使用:0次
名校
解题方法
3 . 我国科学家研究出一种钠离子可充电电池的工作示意图如下,该电池主要依靠钠离子在正极和负极之间移动来工作,电池反应为
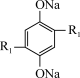 +
+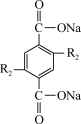

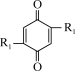 +
+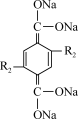
(-R1代表没参与反应的-COONa,-R2代表没参与反应的-ONa),下列有关说法不正确的是
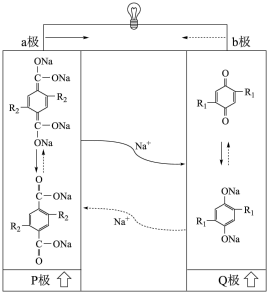
 +
+

 +
+
(-R1代表没参与反应的-COONa,-R2代表没参与反应的-ONa),下列有关说法不正确的是

| A.钠离子电池相比于锂离子电池,具有原料储量丰富,价格低廉的优点 |
| B.放电时,a极为负极,发生氧化反应 |
C.充电时,阴极发生反应为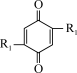 +2e-+2Na+= +2e-+2Na+=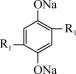 |
| D.充电时,当电路中转移0.3mol电子时,P极质量增加6.9g |
您最近一年使用:0次
2022-05-22更新
|
116次组卷
|
4卷引用:安徽师范大学附属中学2022届高三下学期第十八次综合测试理综化学试题
安徽师范大学附属中学2022届高三下学期第十八次综合测试理综化学试题福建省龙岩第一中学2022届高三下学期第一次模拟考试化学试题(已下线)专项11 电化学基础-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)福建省南平第一中学2023-2024学年高三上学期10月月考化学试题
名校
4 . 我国科学家研发了一种水系可逆Zn-CO2电池,电池工作时,复合膜(由a、b膜复合而成)层间的H2O解离成H+和OH-,在外加电场中可透过相应的离子膜定向移动。当闭合K1时,Zn-CO2电池工作原理如图所示。下列说法不正确的是
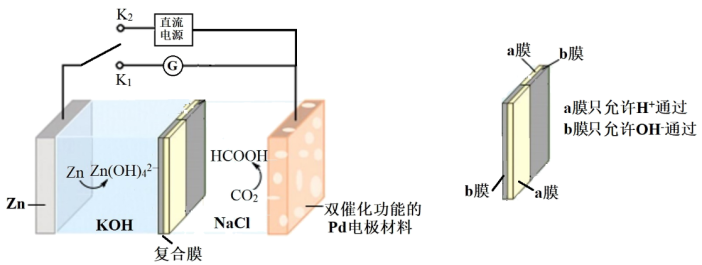

| A.闭合K1时,Pd电极电势高于Zn电极电势 |
| B.Pd电极还具有高效双催化性能,有利于CO2 和HCOOH的相互转化 |
| C.闭合K 2时,OH-通过b膜向Pd 电极方向移动 |
| D.闭合K1时,Pd表面的电极反应式为CO2+ 2H++2e-= HCOOH |
您最近一年使用:0次
名校
解题方法
5 . 化学电池在通讯、交通及日常生活中有着广泛的应用。回答下列问题:
(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是_______ ,负极发生的电极反应式为_______ 。若反应消耗16.25g负极材料,则电池中转移电子的物质的量为_______ mol。

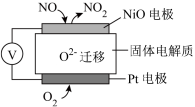
(2)氮氧化物是重要的大气污染物,下图是监测NO含量的传感器工作原理示意图。NiO电极发生_______ (填“氧化”或“还原”)反应,Pt电极上的电极反应式为_______ 。
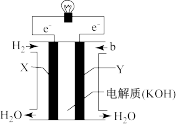
(3)下图为氢氧燃料电池的构造示意图,X极为电池的_______ (填“正”或“负”)极,Y极的电极反应式为_______ 。
(1)锌锰干电池是应用最普遍的电池之一(如图所示),锌锰干电池的负极材料是

(2)氮氧化物是重要的大气污染物,下图是监测NO含量的传感器工作原理示意图。NiO电极发生

(3)下图为氢氧燃料电池的构造示意图,X极为电池的

您最近一年使用:0次
解题方法
6 . 工业上用双极膜电解槽电解糠醛溶液,制备糠醇和糠酸盐,电解时MnO2/MnOOH在电极与糠醛之间传递电子,电解过程如图所示,图中的双极膜中间层中的H2O解离为H+和OH-,并在直流电场作用下分别向两极迁移。下列说法正确的是
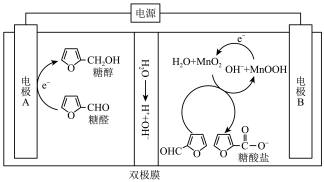

| A.电极A接直流电源的负极,糠醛被氧化为糠醇 |
| B.电解时,阳极反应为MnOOH-e-+OH-=MnO2+H2O |
| C.制得0.1mol糠酸盐,理论上外电路中迁移了0.1mol电子 |
| D.通电时双极膜将水解离为H+和OH-,H+向电极B方向移动 |
您最近一年使用:0次
7 . 图为2021年新研发的车载双电极镍氢电池,该电池相当于两电池用铜箔串联在一起,放电时a、c电极的反应物为吸附了氢气的稀土合金,可表示为MH;充电时b、d电极的反应物为吸附的Ni(OH)2,下列叙述正确的是
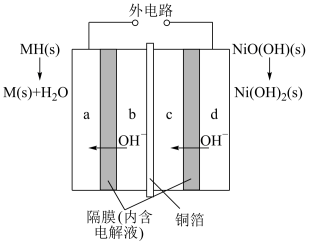

| A.a、b为电池负极,c、d为电池正极 |
| B.充电时,c极上的反应可表示为H2O+M+e-=MH+OH- |
| C.图示显示的是电池放电的过程,放电时电池正极质量减小 |
| D.充电时电子流动路径为外接电源负极→a、d→外接电源正极,而a→b、b→c、c→d的导电过程均借助离子迁移完成 |
您最近一年使用:0次
名校
解题方法
8 . 下图属于日本产业研究所和日本学术振兴会共同开发研究的大容量锂空气电池。下列说法不正确的是
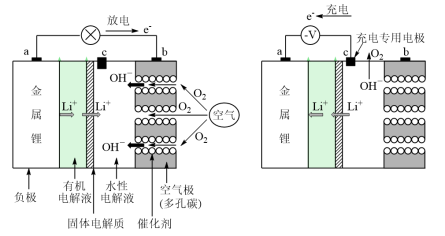

| A.充电时,a为阴极固体电解质催化剂 |
| B.放电时,b极附近pH增大 |
| C.放电时,在有机电解液中加入少量NaCl溶液,可提高导电性 |
| D.用此装置电解CuSO4溶液,当电路中转移0.2mol电子时,阴极析出铜单质6.4g |
您最近一年使用:0次
名校
解题方法
9 . 氟离子电池是一种前景广阔的新型电池,其能量密度是目前锂电池的十倍以上且不会因为过热而造成安全风险。如图是氟离子电池工作示意图,其中充电时F-从乙电极移向甲电极,下列关于该电池的说法正确的是
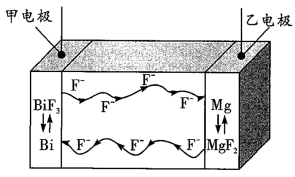

| A.放电时,甲电极的电极反应式为Bi-3e-+3F-=BiF3 |
| B.充电时,外加电源的正极与乙电极相连 |
| C.放电时,乙电极电势比甲电极电势高 |
| D.充电时,导线上每通过0.1mole-,甲电极质量增加1.9g |
您最近一年使用:0次
2021-02-02更新
|
419次组卷
|
8卷引用:安徽省芜湖市2021届高三上学期期末考试理综化学试题
解题方法
10 . I.氮和氮的化合物在国防、工农业生产和生活中都有极其广泛的用途。请回答下列问题:
(1)亚硝酰氯(结构式为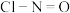 )是有机合成中的重要试剂,它可由
)是有机合成中的重要试剂,它可由 和
和 在常温常压条件下反应制得,反应方程式为:
在常温常压条件下反应制得,反应方程式为: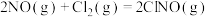 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:
则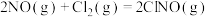

________  。
。
(2)在一个恒容密闭容器中充入 和
和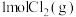 发生(1)中的反应,在温度分别为
发生(1)中的反应,在温度分别为 ℃、
℃、 ℃时测得
℃时测得 的物质的量(单位:mol)与时间的关系如下表所示:
的物质的量(单位:mol)与时间的关系如下表所示:
①
________  (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。
②温度为 时,起始时容器内的压强为
时,起始时容器内的压强为 ,则该反应的平衡常数
,则该反应的平衡常数
________ (用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)(化为最简式)。
物质的量分数)(化为最简式)。
(3)近年来,地下水中的氮污染已成为世界性的环境问题。在金属 、
、 和依(
和依( )的催化作用下,
)的催化作用下, 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),其工作原理如图所示。
),其工作原理如图所示。
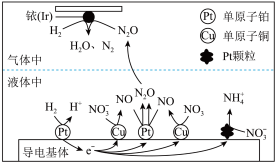
① 表面发生反应的化学方程式为:
表面发生反应的化学方程式为:________ 。
②若导电基体上的 颗粒增多,造成的后果是
颗粒增多,造成的后果是________ 。
Ⅱ.利用电化学原理,将 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
制成燃料电池,模拟工业电解法精炼银,装置如下图所示。

(4)①甲池工作时, 转变成绿色硝化剂
转变成绿色硝化剂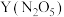 ,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为
,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为________ 。
②若用10A的电流电解50min后,乙中阴极得到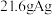 ,则该电解池的电解效率为
,则该电解池的电解效率为________ %。(保留小数点后一位。通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为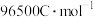 )
)
(1)亚硝酰氯(结构式为
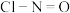 )是有机合成中的重要试剂,它可由
)是有机合成中的重要试剂,它可由 和
和 在常温常压条件下反应制得,反应方程式为:
在常温常压条件下反应制得,反应方程式为: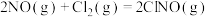 。已知几种化学键的键能数据如表所示:
。已知几种化学键的键能数据如表所示:| 化学键 |  |  | 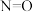 |  |
键能 | 243 | 200 | 607 | 630 |
则
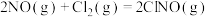

 。
。(2)在一个恒容密闭容器中充入
 和
和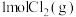 发生(1)中的反应,在温度分别为
发生(1)中的反应,在温度分别为 ℃、
℃、 ℃时测得
℃时测得 的物质的量(单位:mol)与时间的关系如下表所示:
的物质的量(单位:mol)与时间的关系如下表所示:t/min 温度  | 0 | 5 | 8 | 13 |
 | 2 | 1.5 | 1.3 | 1.0 |
 | 2 | 1.15 | 1.0 | 1.0 |
①

 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。②温度为
 时,起始时容器内的压强为
时,起始时容器内的压强为 ,则该反应的平衡常数
,则该反应的平衡常数
 总压
总压 物质的量分数)(化为最简式)。
物质的量分数)(化为最简式)。(3)近年来,地下水中的氮污染已成为世界性的环境问题。在金属
 、
、 和依(
和依( )的催化作用下,
)的催化作用下, 可高效转化酸性溶液中的硝态氮(
可高效转化酸性溶液中的硝态氮( ),其工作原理如图所示。
),其工作原理如图所示。
①
 表面发生反应的化学方程式为:
表面发生反应的化学方程式为:②若导电基体上的
 颗粒增多,造成的后果是
颗粒增多,造成的后果是Ⅱ.利用电化学原理,将
 、
、 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
制成燃料电池,模拟工业电解法精炼银,装置如下图所示。
(4)①甲池工作时,
 转变成绿色硝化剂
转变成绿色硝化剂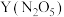 ,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为
,可循环使用,则石墨Ⅱ附近发生的电极反应方程式为②若用10A的电流电解50min后,乙中阴极得到
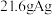 ,则该电解池的电解效率为
,则该电解池的电解效率为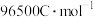 )
)
您最近一年使用:0次



