1 . Al-H2O2电池是一种新型电池,已知H2O2是一种弱酸,在强碱性溶液中以HO 形式存在。现以Al-H2O2为电源(如甲池所示,电池总反应为2Al+3HO
形式存在。现以Al-H2O2为电源(如甲池所示,电池总反应为2Al+3HO =2AlO
=2AlO +OH-+H2O),电解处理有机质废水(如乙池所示)。下列说法正确的是
+OH-+H2O),电解处理有机质废水(如乙池所示)。下列说法正确的是

 形式存在。现以Al-H2O2为电源(如甲池所示,电池总反应为2Al+3HO
形式存在。现以Al-H2O2为电源(如甲池所示,电池总反应为2Al+3HO =2AlO
=2AlO +OH-+H2O),电解处理有机质废水(如乙池所示)。下列说法正确的是
+OH-+H2O),电解处理有机质废水(如乙池所示)。下列说法正确的是
| A.电池工作时,甲池、乙池用导线连接的顺序为a连c,b连d |
| B.电池工作一段时间后甲池中pH值减小 |
| C.乙池工作时,质子将从B电极室移向A电极室 |
| D.若B电极上转化1.5molCO2,则甲池中溶解4molAl |
您最近半年使用:0次
名校
解题方法
2 . 包覆纳米硅复合材料(GS-Si)的可充电石墨烯电池工作原理如图所示。放电时,GS-Si包覆石墨烯电极上的物质变化为:C6Li→C6Li1-x;多元含锂过渡金属氧化物电极上的物质变化为:Li1-xMO2→LiMO2,下列说法错误的是
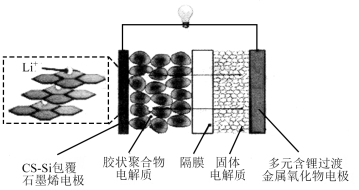

| A.放电时,胶状聚合物电解质和固体电解质的作用均为传导离子,构成闭合回路 |
| B.若放电前两个电极质量相等,转移0.1mol电子后两个电极质量相差0.7g |
| C.充电时,与正极连接的电极反应为LiMO2-xe-=Lil-xMO2+xLi+ |
| D.为保护电池,GS-Si包覆石墨烯的电极反应不能进行至C6Li-e-=C6+Li+ |
您最近半年使用:0次
2021-05-14更新
|
1697次组卷
|
8卷引用:山东省日照市2021届高三下学期第三次模拟考试化学试题
山东省日照市2021届高三下学期第三次模拟考试化学试题福建省厦门外国语学校2021届高三5月高考适应性考试化学试题安徽省淮北市树人高级中学2020-2021学年高二下学期期末考试化学试题福建省连城县第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)专题07 电化学之原电池-【微专题·大素养】备战2022年高考化学讲透提分要点湖南省娄底市第五中学2021-2022学年高三下学期期中考试化学试题(已下线)押江苏卷第12题 电化学及其应用 -备战2022年高考化学临考题号押题(江苏卷)进阶训练4
3 . 研究人员研制出一种可快速充放电的超性能铝离子电池,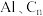 为电极,有机阳离子与阴离子(
为电极,有机阳离子与阴离子( 、
、 )组成的离子液体为电解质,该电池放电过程示意图如下。下列说法正确的是
)组成的离子液体为电解质,该电池放电过程示意图如下。下列说法正确的是
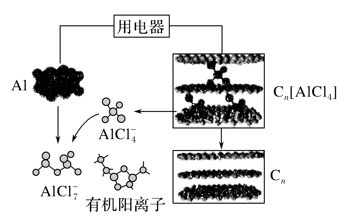
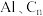 为电极,有机阳离子与阴离子(
为电极,有机阳离子与阴离子( 、
、 )组成的离子液体为电解质,该电池放电过程示意图如下。下列说法正确的是
)组成的离子液体为电解质,该电池放电过程示意图如下。下列说法正确的是
A.充电时, 电极接外接电源正极 电极接外接电源正极 |
B.充电时,每生成 铝,同时消耗 铝,同时消耗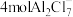 |
| C.放电时,电解质中的有机阳离子向铝电极方向移动 |
D.放电时,正极反应式为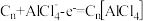 |
您最近半年使用:0次
名校
解题方法
4 . 由于存在同种电解质溶液的浓度差而产生电动势的电池称为浓差电池。利用浓差电池电解硫酸钠溶液可以制得氧气、氢气、硫酸和氢氧化钠,其装置如图所示(a、b电极均为石墨电极)。下列说法正确的是(已知:溶液A为 1L 1mol/L AgNO3溶液; 溶液B为 1L 4mol/L AgNO3溶液)
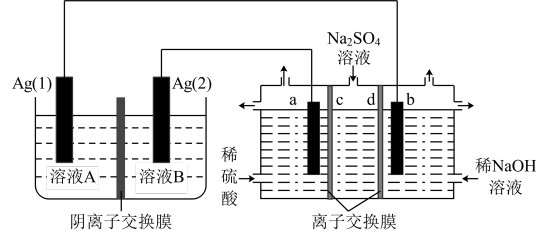

| A.电池放电过程中Ag(1)为正极,电极反应为Ag+ + e-= Ag |
| B.a电极的电极反应为2H2O-4e-=O2↑+4H+,b电极上发生的是还原反应 |
| C.c、d离子交换膜依次为阳离子交换膜和阴离子交换膜 |
| D.电池从开始工作到停止放电,电解池理论上可制得80g氢氧化钠 |
您最近半年使用:0次
2021-04-30更新
|
1091次组卷
|
6卷引用:宁夏银川一中2020-2021学年高二下学期期中考试化学试题
宁夏银川一中2020-2021学年高二下学期期中考试化学试题(已下线)2022年浙江1月高考真题变式题(21-25)福建省三明市四地四校2021-2022学年高二上学期期中联考协作卷化学试题河南省南阳市2022-2023学年高二上学期10月期中考试化学试题(已下线)化学-2023年高考押题预测卷01(全国乙卷)(含考试版、全解全析、参考答案、答题卡)河南省南阳市方城县第一高级中学2022-2023学年高二上学期11月期中考试化学试题
解题方法
5 . 2019年诺贝尔化学奖授予美国固体物理学家约翰·巴尼斯特·古迪纳夫( )、英国化学家斯坦利·威廷汉(
)、英国化学家斯坦利·威廷汉( )和日本化学家吉野彰(
)和日本化学家吉野彰( ),以表彰他们发明锂离子电池方面做出的贡献。下面说法
),以表彰他们发明锂离子电池方面做出的贡献。下面说法不正确 的是

 )、英国化学家斯坦利·威廷汉(
)、英国化学家斯坦利·威廷汉( )和日本化学家吉野彰(
)和日本化学家吉野彰( ),以表彰他们发明锂离子电池方面做出的贡献。下面说法
),以表彰他们发明锂离子电池方面做出的贡献。下面说法
A.将钴酸锂( )作为电池的阴极,将除锂之外的金属材料作为阳极,能够实现高密度的能量储存 )作为电池的阴极,将除锂之外的金属材料作为阳极,能够实现高密度的能量储存 |
| B.锌-锰电池虽然具有低成本的优势,但电压和电容量距离锂电池有较大差距 |
| C.锂电池和锂离子电池区别在于锂离子电池是一次电池,只能放电;锂电池是二次电池可充电也可以放电 |
D.某新型电池发生总反应为:  放电过程中,正极附近溶液的 放电过程中,正极附近溶液的 变大 变大 |
您最近半年使用:0次
6 . 某研究机构使用Li—SO2Cl2电池作为电源电解制备Ni(H2PO2)2,其工作原理如图所示。已知电池反应为2Li+SO2Cl2=2LiCl+SO2↑,下列说法正确的是


| A.电池的f极连接电解池的h极 |
| B.膜a、c是阴离子交换膜,膜b是阳离子交换膜 |
| C.电池中C电极的电极反应式为SO2Cl2+2e-=2Cl-+SO2↑ |
| D.电解池中不锈钢电极溶解,需要及时更换补充 |
您最近半年使用:0次
名校
解题方法
7 . 以NOx为主要成分的雾霾的综合治理是当前重要的研究课题。
I.汽车尾气中的 NO(g)和 CO(g)在一定条件下可发生反应生成无毒的N2和 CO2:
2NO(g)+2CO(g) N2(g)+2CO2(g) △H =-746.5 kJ/mol ①
N2(g)+2CO2(g) △H =-746.5 kJ/mol ①
(1)某研究小组在三个容积为 5 L 的恒容密闭容器中,分别充入 0.4mol NO 和 0.4 mol CO,发生反应① 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图1所示:
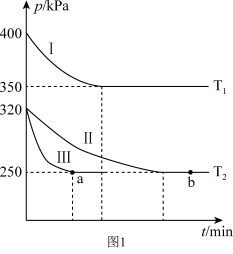
①温度:T1___________ T2(填“<”“=”或“>”)。
②CO 的平衡转化率:Ⅰ___________ Ⅱ___________ Ⅲ(填“<”“=”或“>”)。
③反应速率:a 点的 v(逆)___________ b 点的 v(正) (填“<”“=”或“>”)。
④T2时的平衡常数 Kp=___________ 。(Kp表示用平衡分压表示的平衡常数,各物质的分压=总压×各物质在混合气体中所占的物质的量分数)
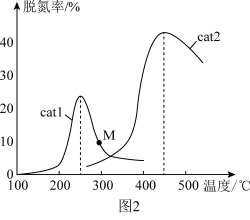
(2)将 NO和 CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即 NO的转化率)如图2所示。M 点___________ (填“是”或“不是”)对应温度下的平衡脱氮率, 说明理由___________ 。
II.将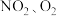 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如图3所示。
制成燃料电池,模拟工业电解法精炼银,装置如图3所示。

(3)①甲池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅱ附近发生的电极反应方程式为___________ 。
②若用10A的电流电解50min后,乙中阴极得到21.6gAg,则该电解池的电解效率为___________ %。(保留小数点后一位)。已知:通过一定电量时阴极上实际沉积的金属质量与通过相同电量时理论上应沉积的金属质量之比叫电解效率。法拉第常数为96500C•mol﹣1
I.汽车尾气中的 NO(g)和 CO(g)在一定条件下可发生反应生成无毒的N2和 CO2:
2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H =-746.5 kJ/mol ①
N2(g)+2CO2(g) △H =-746.5 kJ/mol ①(1)某研究小组在三个容积为 5 L 的恒容密闭容器中,分别充入 0.4mol NO 和 0.4 mol CO,发生反应① 。在三种不同实验条件下进行上述反应(体系各自保持温度不变),反应体系总压强随时间的变化如图1所示:

①温度:T1
②CO 的平衡转化率:Ⅰ
③反应速率:a 点的 v(逆)
④T2时的平衡常数 Kp=
(2)将 NO和 CO以一定的流速通过两种不同的催化剂(cat1、cat2)进行反应,相同时间内测量的脱氮率(脱氮率即 NO的转化率)如图2所示。M 点

II.将
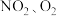 和熔融
和熔融 制成燃料电池,模拟工业电解法精炼银,装置如图3所示。
制成燃料电池,模拟工业电解法精炼银,装置如图3所示。
(3)①甲池工作时,NO2转变成绿色硝化剂Y(N2O5),可循环使用,则石墨Ⅱ附近发生的电极反应方程式为
②若用10A的电流电解50min后,乙中阴极得到21.6gAg,则该电解池的电解效率为
您最近半年使用:0次
8 . 硼化钒(VB2)—空气电池是目前储电能力最高的电池之一。如图所示,在VB电极发生反应:VB2+16OH--11e-=VO +2B(OH)
+2B(OH) +4H2O。该电池工作时,下列说法错误的是
+4H2O。该电池工作时,下列说法错误的是
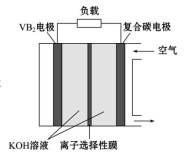
 +2B(OH)
+2B(OH) +4H2O。该电池工作时,下列说法错误的是
+4H2O。该电池工作时,下列说法错误的是
| A.电子从VB2电极流出 |
| B.正极区溶液的pH升高 |
C.电池总反应为4VB2+11O2+20OH-+6H2O=8B(OH) +4VO +4VO |
| D.如果将负载换成惰性电极电解足量硫酸铜溶液的电解池,当复合碳电极有0.224L(标准状况)O2参与反应时,电解池阳极析出1.28gCu |
您最近半年使用:0次
解题方法
9 . 水体中的含氮化合物是引起富营养化的主要污染物,控制水体中的含氮污染物,对水资源的循环利用意义重大。
25℃时,亚硝酸( )和连二次硝酸(
)和连二次硝酸( )的电离常数如下表所示:
)的电离常数如下表所示:
(1)下列不能说明 是弱电解质的是
是弱电解质的是___________ (填序号)。
A.室温下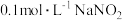 溶液的
溶液的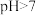
B.用一定浓度的 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗
C.等pH、等体积的盐酸和 溶液分别与足量锌反应,
溶液分别与足量锌反应, 溶液放出的氢气较多
溶液放出的氢气较多
(2) 溶液呈
溶液呈___________ 性(填“酸”“碱”或“中”),原因是___________ (用离子方程式表示)。
(3)室温下,物质的量浓度相同的溶液: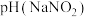
___________ 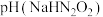 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
(4)25℃时,用 的
的 溶液滴定
溶液滴定 溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为
溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为___________ 。
(5)亚硝酸盐对人体健康的损害不亚于农药,可采用电解含 、
、 废水的方法除去
废水的方法除去 (生成物为
(生成物为 ,同时再生
,同时再生 ,其原理如图所示。
,其原理如图所示。
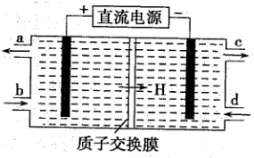
① 从电解槽的
从电解槽的___________ (填字母)口流出。
②写出阴极的电极反应式___________ 。
(6)新的研究表明,将含 的废水与含
的废水与含 的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为
的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为___________ 。
25℃时,亚硝酸(
 )和连二次硝酸(
)和连二次硝酸( )的电离常数如下表所示:
)的电离常数如下表所示:| 化学式 |  |  |
| 电离常数 | 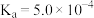 | 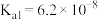 、 、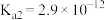 |
(1)下列不能说明
 是弱电解质的是
是弱电解质的是A.室温下
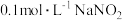 溶液的
溶液的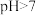
B.用一定浓度的
 溶液做导电实验,灯泡很暗
溶液做导电实验,灯泡很暗C.等pH、等体积的盐酸和
 溶液分别与足量锌反应,
溶液分别与足量锌反应, 溶液放出的氢气较多
溶液放出的氢气较多(2)
 溶液呈
溶液呈(3)室温下,物质的量浓度相同的溶液:
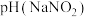
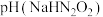 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(4)25℃时,用
 的
的 溶液滴定
溶液滴定 溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为
溶液,当两者恰好完全反应生成正盐时,溶液中离子浓度由大到小的顺序为(5)亚硝酸盐对人体健康的损害不亚于农药,可采用电解含
 、
、 废水的方法除去
废水的方法除去 (生成物为
(生成物为 ,同时再生
,同时再生 ,其原理如图所示。
,其原理如图所示。
①
 从电解槽的
从电解槽的②写出阴极的电极反应式
(6)新的研究表明,将含
 的废水与含
的废水与含 的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为
的废水按一定比例混合,直接转化为无毒气体,该反应的离子方程式为
您最近半年使用:0次
10 . 一氧化氮-空气质子交换膜燃料电池将化学能转化为电能,实现了制硝酸、发电、环保三位一体的结合。如图所示,某同学设计用该电池探究将雾霾中的SO2、NO转化为(NH4)2SO4 的原理和粗铜的精炼原理。

(1)甲装置燃料电池放电过程中正极的电极反应式_________ 。
(2)乙装置中物质 A 是_____ (填化学式);电解过程中阳极附近 pH_____ (填“增大”“减小”或“不变”);
(3)如果粗铜中含有锌、银等杂质,丙装置中阴极的电极反应式是_____ ,反应一段时间,CuSO4 溶液的浓度将_____ (填“增大”、“减小”或“不变”)。
(4)若在标准状况下,甲装置有 22.4 L O2 参加反应,则乙装置中转化 SO2 和 NO 的物质的量共有_____ mol;丙装置中阴极析出铜的质量为_____ g。

(1)甲装置燃料电池放电过程中正极的电极反应式
(2)乙装置中物质 A 是
(3)如果粗铜中含有锌、银等杂质,丙装置中阴极的电极反应式是
(4)若在标准状况下,甲装置有 22.4 L O2 参加反应,则乙装置中转化 SO2 和 NO 的物质的量共有
您最近半年使用:0次



