10-11高一下·河北·期中
1 . 根据下图,回答下列问题:
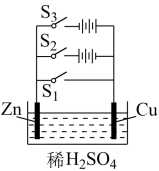
(1)若闭合S1,装置属于___________ ,锌极作___________ 。
(2)若闭合S2,装置属于___________ ,锌极上的反应为___________ 。
(3)若闭合S3,装置属于___________ ,总反应为___________ 。

(1)若闭合S1,装置属于
(2)若闭合S2,装置属于
(3)若闭合S3,装置属于
您最近半年使用:0次
9-10高一下·浙江宁波·期中
2 . 有如图电化学装置,以多孔石墨为电极、AgNO3为电解质溶液。改变开关K1、K2的闭合状态,回答下列问题。
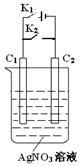
(1)若打开K2、闭合K1,此时,该装置为_______ (原电池或电解池),C1上发生的电极反应式为:_______ 。
(2)当两电极质量不再改变时,断开K1、闭合K2.此时,C1上发生的电极反应式为:_______ ,电化学装置内发生的总反应方程式:_______ 。

(1)若打开K2、闭合K1,此时,该装置为
(2)当两电极质量不再改变时,断开K1、闭合K2.此时,C1上发生的电极反应式为:
您最近半年使用:0次
名校
3 . 关于下列各装置图的叙述中,不正确 的是
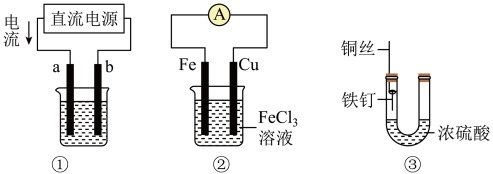

| A.用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B.用装置①进行电镀,镀件接在b极上 |
| C.装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ |
| D.装置③中的铁钉几乎没被腐蚀 |
您最近半年使用:0次
2016-12-01更新
|
487次组卷
|
14卷引用:吉林省长春市第二十九中学2019-2020学年高一下学期第三次月考化学(理)试题
吉林省长春市第二十九中学2019-2020学年高一下学期第三次月考化学(理)试题吉林省长春汽车经济技术开发区第六中学2019-2020学年高一下学期期末考试化学试题(已下线)2013-2014学年山东省潍坊市高二上学期期末统考化学试卷2015-2016学年山东枣庄三中高二10月学情调查化学卷2016-2017学年河北省邯郸市成安一中、永年二中高二上期中化学卷福建省三明市第一中学2017-2018学年高二上学期第一次月考化学试题山东省济南市第一中学2017-2018学年高二10月阶段测试化学试题河北省邯郸市2016-2017学年高二上学期期中考试化学试题山东省泰安第四中学2018-2019学年高二上学期12月月考化学试题(已下线)第24讲 电解池与金属腐蚀与保护-2021年高考化学一轮复习名师精讲练山东省潍坊第四中学2021-2022学年高三上学期10月月考化学试题山东省潍坊市昌乐二中2021-2022学年高三10月月考化学试题甘肃省嘉峪关市等3地2022-2023学年高二上学期12月期末化学试题甘肃省临夏甘南两地联考2022-2023学年高二上学期12月期中考试化学试题
名校
4 . 用酸性氢氧燃料电池为电源进行电解的实验装置示意图如下图所示。下列说法中,正确的是


| A.燃料电池工作时,正极反应为:O2 + 2H2O + 4e-= 4OH- |
| B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 |
| C.a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 |
| D.a、b两极均是石墨时,在相同条件下a极产生的气体与电池中消耗的H2体积相等 |
您最近半年使用:0次
2016-07-25更新
|
855次组卷
|
14卷引用:【全国百强校】北京市第四中学2017-2018学年高一下学期期末考试化学(选考)试题
【全国百强校】北京市第四中学2017-2018学年高一下学期期末考试化学(选考)试题河北省石家庄一中东校区2020-2021学年高一第二学期教学质量检测(二)化学试题(已下线)2012届山东省泰安市高三上学期期末检测化学试卷2015-2016学年河北省唐山市高二上学期期末考试化学试卷2016届甘肃省武威六中高三一轮复习阶段测(五)化学试卷2015-2016学年湖南省娄底市重点中学高二下学期期末化学试卷【校级联考】福建省平和一中、南靖一中等五校2018-2019学年高二上学期第一次联考化学试题安徽省池州市第一中学2019-2020学年高二上学期期中考试化学试题云南省临沧市双江县第一中学2019-2020学年高二上学期12月月考化学试题云南省通海三中2019-2020学年高二上学期期末考试化学试题广西壮族自治区田阳高中2019-2020学年高二下学期6月月考理科综合化学试题(已下线)专题05 化学反应与能量——备战2021年高考化学纠错笔记湖南省益阳市2020-2021学年高三上学期复学摸底考试化学试题黑龙江省黑河市五校(嫩江市第一中学,嫩江市职业高中,黑河七中,伊拉哈中学,海江中学)2021-2022学年高二上学期期末联考化学试题
5 . 一种新型钠硫电池结构示意图如图,下列有关该电池的说法正确的是


| A.B极中填充多孔的炭或石墨毡,目的是为了增加导电性 |
| B.电池放电时,A极电极反应为:2Na++xS+2e-=Na2SX |
| C.电池放电时,Na+向电极A极移动 |
| D.电池放电的总反应为2Na+xS=Na2SX,每消耗1molNa转移2mol电子 |
您最近半年使用:0次
2016-06-28更新
|
308次组卷
|
3卷引用:江西省南昌市新建区第二中学2019-2020学年高一下学期“新星计划”体验营7月期终考试化学试题
江西省南昌市新建区第二中学2019-2020学年高一下学期“新星计划”体验营7月期终考试化学试题2016届江苏省清江中学高三考前周练模拟化学试卷(已下线)第20讲 原电池 化学电源(精练)-2021年高考化学一轮复习讲练测
解题方法
6 . 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池。下图为RFC工作原理示意图,有关说法正确的是( )
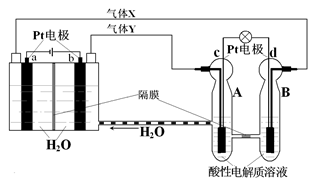

| A.转移0.1mol电子时,a电极产生1.12LH2。 |
| B.b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- |
| C.c电极上发生还原反应,B电池中的H+可以通过隔膜进入A池 |
| D.d电极上发生的电极反应是:O2+4H++4e-=2H2O |
您最近半年使用:0次
2016-06-25更新
|
235次组卷
|
6卷引用:2015-2016学年辽宁省沈阳二中高一下期中化学试卷
11-12高三上·河南三门峡·期中
名校
7 . 下图所示甲、乙是电化学实验装置。
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为__________________________________ 。
②乙中总反应的离子方程式为____________________________________ 。
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为_________ 。
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为__________________________ 。
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入________ (填写物质的化学式)________ g。
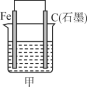
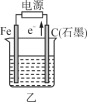
(1)若甲、乙两烧杯中均盛有NaCl溶液。
①甲中石墨棒上的电极反应式为
②乙中总反应的离子方程式为
③将湿润的淀粉KI试纸放在乙烧杯上方,发现试纸先变蓝后褪色,这是因为过量的Cl2氧化了生成的I2。若反应中Cl2和I2的物质的量之比为5∶1,且生成两种酸,该反应的化学方程式为
(2)若甲、乙两烧杯中均盛有CuSO4溶液。
①甲中铁棒上的电极反应式为
②如果起始时乙中盛有200 mL pH=5的CuSO4溶液(25 ℃),一段时间后溶液的pH变为1,若要使溶液恢复到电解前的状态,可向溶液中加入
您最近半年使用:0次
2011-12-12更新
|
814次组卷
|
14卷引用:2012-2013学年吉林省吉林一中高一4月月考化学试卷
(已下线)2012-2013学年吉林省吉林一中高一4月月考化学试卷(已下线)2012届河南省三门峡市高三上学期调研考试化学试卷(已下线)2012届山东省潍坊市寿光现代中学高三12月月考化学试卷(已下线)2011-2012学年河南省平顶山市高二上学期期末考试化学试卷(已下线)2011-2012年湖北宜昌金东方学校高二上学期期末考试化学试卷(已下线)2014年化学高考总复习单元检测 第九章电化学基础练习卷(已下线)2014年高考化学苏教版总复习 6-3 原电池金属的腐蚀及防护练习卷(已下线)2013-2014河南省封丘一中高二上学期期末考试化学试卷2014-2015湖南省娄底市高二上学期期末考试化学(理)试卷2017届福建省厦门大学附中高三上学期第二次月考化学试卷江西省玉山县第一中学2017届高三化学板块复习测试:基本理论(已下线)考点10 电解原理 金属的腐蚀与防护——备战2019年浙江新高考化学考点江西省南城县第二中学2018-2019学年高二上学期第二次月考化学试题江西省南昌市进贤一中2019-2020学年高二上学期期末考试化学试题
10-11高一下·江苏盐城·期末
8 . 铅蓄电池属于二次电池,其电极材料分别是Pb和PbO2,电解质溶液为一定浓度的硫酸,工作时,该电池的总反应为PbO2+Pb+2H2SO4=2PbSO4+2H2O;PbSO4不溶。
(1)该蓄电池工作时负极的电极反应式为_______________________________________
(2)将质量相等的铁棒和石墨棒分别插入CuSO4溶液中,铁棒接该蓄电池Pb极,石墨棒接该蓄电池PbO2极,一段时间后测得铁棒比石墨棒增加了3.2克,则CuSO4溶液质量_________ (增加、减少)_________ 克;如果要求将CuSO4溶液恢复成与开始时完全相同,则可以加入下列物质中的___________
E.Cu固体 F. Cu2(OH) 2CO3固体
(3)若用该蓄电池作电源(都用惰性材料做电极)电解400克饱和食盐水,如果电池内硫酸的的体积为5升,当其浓度从1.5mol/L降至1.3mol/L时,计算剩余溶液中氯化钠的质量分数_________ (该温度下氯化钠的溶解度为32克)。
(1)该蓄电池工作时负极的电极反应式为
(2)将质量相等的铁棒和石墨棒分别插入CuSO4溶液中,铁棒接该蓄电池Pb极,石墨棒接该蓄电池PbO2极,一段时间后测得铁棒比石墨棒增加了3.2克,则CuSO4溶液质量
| A.CuSO4溶液 | B.CuCO3固体 | C.CuO固体 | D.Cu(OH)2固体 |
E.Cu固体 F. Cu2(OH) 2CO3固体
(3)若用该蓄电池作电源(都用惰性材料做电极)电解400克饱和食盐水,如果电池内硫酸的的体积为5升,当其浓度从1.5mol/L降至1.3mol/L时,计算剩余溶液中氯化钠的质量分数
您最近半年使用:0次
10-11高一下·浙江温州·期末
9 . 用下图装置加以必要的导线连接后达到粗铜精炼的目的。
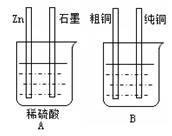
⑴A烧杯是________________ (填〝电解池〞或〝原电池〞),
B烧杯是________________ (填〝电解池〞或〝原电池〞)。
⑵其中Zn接B烧杯中的___________ ,(填“粗铜”或“纯铜”),B烧杯中应该盛____________ 溶液。
⑶分别写出石墨棒和纯铜棒的电极反应式
石墨棒:____________________________________ ,
纯铜棒:____________________________________ 。
⑷若锌减少了0.65 g,则纯Cu的质量增加了________ g。

⑴A烧杯是
B烧杯是
⑵其中Zn接B烧杯中的
⑶分别写出石墨棒和纯铜棒的电极反应式
石墨棒:
纯铜棒:
⑷若锌减少了0.65 g,则纯Cu的质量增加了
您最近半年使用:0次
2011-07-07更新
|
1184次组卷
|
3卷引用:2010-2011学年浙江省瑞安中学高一下学期期末联考化学试卷
(已下线)2010-2011学年浙江省瑞安中学高一下学期期末联考化学试卷新疆昌吉市教育共同体2019-2020学年高二年级上学期期末考试化学试题天津市西青区2019-2020学年高二上学期期末考试化学试题



