名校
解题方法
1 . 科研人员新研发了一种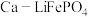 可充电电池,工作原理如图,电池总反应为
可充电电池,工作原理如图,电池总反应为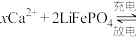
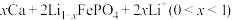 。下列说法不正确的是
。下列说法不正确的是
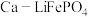 可充电电池,工作原理如图,电池总反应为
可充电电池,工作原理如图,电池总反应为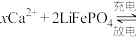
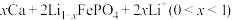 。下列说法不正确的是
。下列说法不正确的是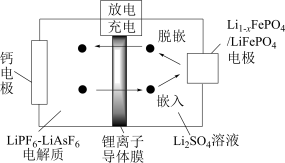
A.当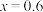 时, 时, 中的 中的 和 和 个数之比为2:3 个数之比为2:3 |
B.放电时,正极反应为 |
C.充电时,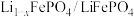 电极发生 电极发生 脱嵌, 脱嵌, 从右室移向左室 从右室移向左室 |
| D.充电时,理论上左室电解质的质量减轻4g,电路中有0.2mol电子转移 |
您最近半年使用:0次
2024-01-21更新
|
223次组卷
|
4卷引用:湖南省衡阳市衡阳县第二中学2023-2024学年高三下学期开学摸底考试化学试卷
名校
2 . 一种以Fe[Fe(CN)6]为代表的新型可充电钠离子电池的放电工作原理如图所示。下列说法正确的是
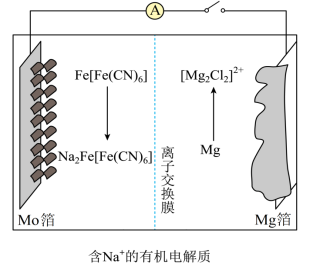

| A.放电时,Na+通过离子交换膜从左室移向右室 |
| B.充电时,电源的负极应与Mo箔连接 |
| C.充电时,溶液中通过0.2mol电子时,阳极质量变化2.3g |
| D.放电时,正极反应式为Fe[Fe(CN)6]+2Na++2e-=Na2Fe[Fe(CN)6] |
您最近半年使用:0次
2024-01-20更新
|
131次组卷
|
3卷引用:吉林省四校期初联考2023-2024学年高二下学期开学考试化学试题
名校
解题方法
3 .  为尖晶石型锰系锂离子电池材料,其晶胞由8个立方单元组成,这8个立方单元可分为A、B两种类型。电池充电过程的总反应可表示为:
为尖晶石型锰系锂离子电池材料,其晶胞由8个立方单元组成,这8个立方单元可分为A、B两种类型。电池充电过程的总反应可表示为: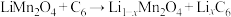 。已知:充放电前后晶体中锰的化合价只有+3、+4,分别表示为Mn(III)、Mn(IV)。
。已知:充放电前后晶体中锰的化合价只有+3、+4,分别表示为Mn(III)、Mn(IV)。
 为尖晶石型锰系锂离子电池材料,其晶胞由8个立方单元组成,这8个立方单元可分为A、B两种类型。电池充电过程的总反应可表示为:
为尖晶石型锰系锂离子电池材料,其晶胞由8个立方单元组成,这8个立方单元可分为A、B两种类型。电池充电过程的总反应可表示为: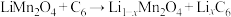 。已知:充放电前后晶体中锰的化合价只有+3、+4,分别表示为Mn(III)、Mn(IV)。
。已知:充放电前后晶体中锰的化合价只有+3、+4,分别表示为Mn(III)、Mn(IV)。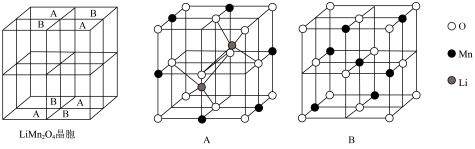
A.每个晶胞含8个 |
B.立方单元B中Mn、O原子个数比为 |
C.放电时,正极反应为 |
D.若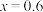 ,则充电后材料中Mn(Ⅲ)与Mn(Ⅳ)的比值为 ,则充电后材料中Mn(Ⅲ)与Mn(Ⅳ)的比值为 |
您最近半年使用:0次
2024-01-19更新
|
540次组卷
|
5卷引用:河南省郑州市宇华实验学校2023-2024学年高三下学期开学化学试题
名校
解题方法
4 . 某储能电池原理如图。下列说法正确 的是
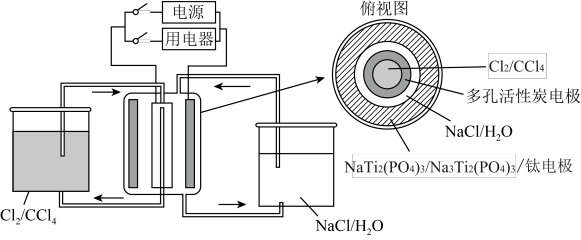

| A.放电时Cl-透过多孔活性炭电极向CCl4中迁移 |
| B.放电时每转移1mol电子,理论上CCl4吸收0.5molCl2 |
C.放电时负极反应: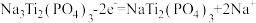 |
| D.充电过程中,NaCl溶液浓度增大 |
您最近半年使用:0次
2024-01-18更新
|
105次组卷
|
2卷引用:江西省宜春市丰城中学2023-2024学年高二下学期开学考试化学试题
名校
5 . 下列有关四个常用电化学装置的叙述中,正确的是
| 图Ⅰ | 图Ⅱ |
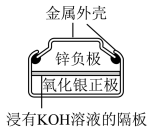 | 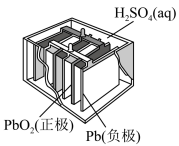 |
| 银锌纽扣电池Zn+Ag2O=2Ag+ZnO | 铅-硫酸蓄电池Pb+PbO2+2H2SO4 2PbSO4+2H2O 2PbSO4+2H2O |
| 图Ⅲ | 图Ⅳ |
 | 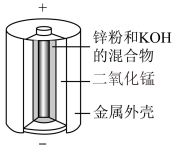 |
| 电解精炼铜 | 碱性锌锰电池Zn+2MnO2+2H2O=Zn(OH)2+2MnO(OH) |
| A.图Ⅰ所示电池中,Ag2O是氧化剂,在电池工作过程中被还原为Ag |
| B.图Ⅱ所示电池放电过程中,硫酸浓度不断增大 |
| C.图Ⅲ所示装置工作过程中,电解质溶液中c(Cu2+)始终不变 |
| D.图Ⅳ所示电池中,二氧化锰的作用是催化剂 |
您最近半年使用:0次
2024-01-14更新
|
137次组卷
|
2卷引用:四川省眉山北外附属东坡外国语学校2023-2024学年高二下学期开学化学试题
名校
解题方法
6 . 某兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装置的电键时,观察到电流计的指针发生了偏转。
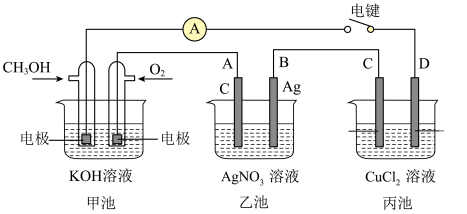
请回答下列问题:
(1)甲池中,通入CH3OH电极的电极反应式为___________ 。
(2)设乙池的体积为200mL,反应一段时间后,乙池中A、B两极都产生22.4mL(已换算成标准状况)的气体时,乙池中pH约为___________ ,反应开始前乙池中的AgNO3的浓度为___________ ,甲池中理论上消耗O2的体积为___________ mL(标准状况)。
(3)若要电解精炼铜,丙池中,粗铜应为___________ (填C或D)电极。
(4)若丙池中C、D两电极都为惰性电极,将其溶液换成NaCl溶液,总电池反应方程式为___________ ,为了获得氢气和氯气,该装置中需使用___________ (填阳离子、阴离子或质子)交换膜。

请回答下列问题:
(1)甲池中,通入CH3OH电极的电极反应式为
(2)设乙池的体积为200mL,反应一段时间后,乙池中A、B两极都产生22.4mL(已换算成标准状况)的气体时,乙池中pH约为
(3)若要电解精炼铜,丙池中,粗铜应为
(4)若丙池中C、D两电极都为惰性电极,将其溶液换成NaCl溶液,总电池反应方程式为
您最近半年使用:0次
2024-01-13更新
|
110次组卷
|
2卷引用:湖南省株洲市炎陵县2023-2024学年高二下学期开学化学试题
名校
7 . 钒电池是化学储能领域的一个研究热点,储能大、寿命长,利用该电池电解含 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。下列说法中正确的是
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。下列说法中正确的是

 的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。下列说法中正确的是
的废水制备硝酸和氨水的原理如图所示,a、b、c、d电极均为惰性电极。下列说法中正确的是
| A.用钒电池处理废水时,a电极区溶液由蓝色变成黄色 |
| B.电势:a极高于c极 |
C.膜2为阴离子交换膜,p口流出液为 |
D.当钒电池有 通过质子交换膜时,处理含 通过质子交换膜时,处理含 的废水 的废水 |
您最近半年使用:0次
2024-01-05更新
|
1019次组卷
|
3卷引用:陕西省渭南市蒲城县2023-2024学年高三下学期开学考试理综试题-高中化学
名校
8 . 将天然气(主要成分为CH4)中的CO2、H2S资源化转化在能源利用、环境保护等方面意义重大。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=-530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是___________
(2)CO2性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低___________ ,提高反应速率。
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应iii,工作原理如下所示。
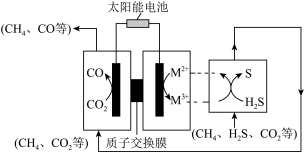
【方案1】若M3+/M2+=Fe3+/Fe2+。为了抑制离子水解,所含Fe3+、Fe2+的溶液调为较强的酸性。
①写出阳极区生成S的电极反应和离子方程式___________ 。
②结合电极反应和离子移动解释阴极区pH不变的原因(忽略溶液体积变化)___________
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+ (配合物)。
已知:电解效率η的定义:
η(B)=n(生成B所用的电子)/ n(通过电极的电子)×100%
③测得η(EDTA-Fe3+)≈100%,η(CO) ≈80%。阴极放电的物质有___________
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1.CO2通过电极反应产生CO
来源2.电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是___________ 。
方案2明显优于方案1.该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
(1)CO2转化为CO、H2S转化为S的反应如下:
i.2CO2(g)=2CO(g)+O2(g) △H1=+566kJ/mol
ii.2H2S(g)+O2(g)=2H2O(l)+2S(s) △H2=-530kJ/mol
iii.CO2、H2S转化生成CO、S等物质的热化学方程式是
(2)CO2性质稳定,是一种“惰性”分子。对于反应iii,通过设计合适的催化剂可以降低
a.活化能 b.△H c.平衡常数
(3)我国科学家研制新型催化剂,设计协同转化装置实现反应iii,工作原理如下所示。

【方案1】若M3+/M2+=Fe3+/Fe2+。为了抑制离子水解,所含Fe3+、Fe2+的溶液调为较强的酸性。
①写出阳极区生成S的电极反应和离子方程式
②结合电极反应和离子移动解释阴极区pH不变的原因(忽略溶液体积变化)
【方案2】若M3+/M2+=EDTA-Fe3+/EDTA-Fe2+ (配合物)。
已知:电解效率η的定义:
η(B)=n(生成B所用的电子)/ n(通过电极的电子)×100%
③测得η(EDTA-Fe3+)≈100%,η(CO) ≈80%。阴极放电的物质有
④为进一步确认CO2、H2S能协同转化,对CO的来源分析如下:
来源1.CO2通过电极反应产生CO
来源2.电解质(含碳元素)等物质发生降解,产生CO
设计实验探究,证实来源2不成立。实验方案是
方案2明显优于方案1.该研究成果为天然气的净化、资源化转化提供了工业化解决思路。
您最近半年使用:0次
名校
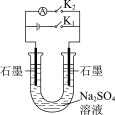
9 . 下列实验能达到实验目的的是
| A | B |
|
|
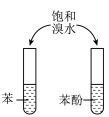
| 制作简单的燃料电池 | 证明苯环使羟基活化 |
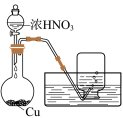
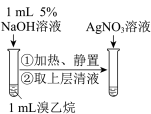
| C | D |
|
|
制备并收集 | 检验溴乙烷的水解产物 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2023-12-23更新
|
118次组卷
|
3卷引用:北京一零一中2023-2024学年高三上学期第一次月考(开学考)化学试卷
名校
10 . 甲烷燃料电池采用铂做电极材料,两个电极上分别通入 和
和 ,电解质溶液为KOH溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀银的实验(甲、乙、丙溶液均足量),如图所示,其中乙装置中X为离子交换膜。下列说法正确的是
,电解质溶液为KOH溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀银的实验(甲、乙、丙溶液均足量),如图所示,其中乙装置中X为离子交换膜。下列说法正确的是
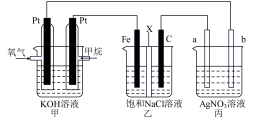
 和
和 ,电解质溶液为KOH溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀银的实验(甲、乙、丙溶液均足量),如图所示,其中乙装置中X为离子交换膜。下列说法正确的是
,电解质溶液为KOH溶液。某研究小组将上述甲烷燃料电池作为电源,进行电解饱和食盐水和电镀银的实验(甲、乙、丙溶液均足量),如图所示,其中乙装置中X为离子交换膜。下列说法正确的是
A.甲烷燃料电池正极电极反应式是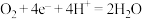 |
| B.为了防止生成的氯气和氢氧化钠接触,乙中X为阴离子交换膜 |
| C.当乙装置中两电极共产生标准状况的气体2.24L(假设气体完全逸出)时,丙装置中a极质量增加10.8g |
D.丙装置为银做阳极的电镀池,反应过程中 溶液的 溶液的 浓度减小 浓度减小 |
您最近半年使用:0次
2023-12-18更新
|
305次组卷
|
2卷引用:甘肃省天水市第一中学2023-2024学年高二下学期开学化学试题