1 . 2021年我国取得多项科研成果,如首套吨级氢液化系统调试成功、首次实现以CO2为原料人工合成淀粉等。下列说法不正确的是
| A.相同条件下,1gH2(l)完全燃烧放出的热量比1gH2(g)的多 |
| B.通过降温加压得到的液氢可存放于特制的绝热容器中 |
| C.通过遇碘变蓝的现象可证明有淀粉生成 |
| D.淀粉可用于生产乙醇、乙酸等化工产品 |
您最近半年使用:0次
2022-02-26更新
|
732次组卷
|
2卷引用:广东省深圳市普通高中2022届高三下学期第一次调研考试化学试题
2021高一·全国·专题练习
2 . 表是国家对加碘盐含碘量下调后精制碘盐包装说明书。
下列有关食品营养强化剂KIO3说法错误的是
| 配料表:氯化钠 碘酸钾KIO3 含碘量:20~30 mg·kg-1 重量:500 g 食用注意:烹调时等食品熟后加入碘盐 贮存方法:密封 避光 防潮 |
| A.缺碘和碘过量都不利于人体健康 |
| B.碘酸钾见光、受热易分解 |
| C.碘酸钾中碘的化合价为+5价 |
| D.可以用淀粉溶液证明加碘盐中是否含碘元素 |
您最近半年使用:0次
解题方法
3 . 在用淀粉制取葡萄糖的实验中,请设计实验方案证明:
(1)淀粉已发生水解________ ;
(2)淀粉已完全水解______ 。
(1)淀粉已发生水解
(2)淀粉已完全水解
您最近半年使用:0次
解题方法
4 . 已知烃A是一种重要的化工原料,其在标准状况下的密度为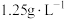 。
。
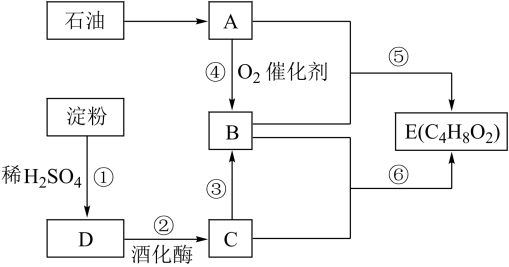
(1)物质B的官能团名称为_______ ;③的反应类型为_______ 。
(2)写出反应⑥的化学方程式_______ 。
(3)下列说法正确的是_______。
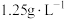 。
。
(1)物质B的官能团名称为
(2)写出反应⑥的化学方程式
(3)下列说法正确的是_______。
| A.向反应①所得溶液中直接加入碘水,若不变蓝,则证明淀粉已经完全水解 |
| B.B、C、E可以用饱和碳酸钠溶液鉴别 |
| C.一定条件下A发生加聚反应所得产物可以使溴的四氯化碳溶液褪色 |
| D.⑤和⑥的反应类型相同 |
您最近半年使用:0次
名校
5 . 将浓度均为0.01mol/L的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。该实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
(资料)
该“碘钟实验”的总反应:H2O2+2S2O +2H+=S4O
+2H+=S4O +2H2O
+2H2O
反应分两步进行:
反应A:H2O2+2I-+2H+=I2+2H2O
反应B:……
(1)反应B的离子方程式是____ 。对于总反应,I-的作用相当于____ 。
(2)为证明反应A、B的存在,进行实验I。
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是____ 。
(3)为探究溶液变蓝快慢的影响因素,进行实验II、实验III。(溶液浓度均为0.01mol/L)
溶液从混合时的无色变为蓝色的时间:实验II是30min、实验III是40min。
①实验III中,z的数值是____ 。
②对比实验II、实验III,可得出的实验结论是____ 。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验IV。
(溶液浓度均为0.01mol/L)
实验过程中,溶液始终 无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的原因:____ 。
(资料)
该“碘钟实验”的总反应:H2O2+2S2O
 +2H+=S4O
+2H+=S4O +2H2O
+2H2O反应分两步进行:
反应A:H2O2+2I-+2H+=I2+2H2O
反应B:……
(1)反应B的离子方程式是
(2)为证明反应A、B的存在,进行实验I。
a.向酸化的H2O2溶液中加入试剂X的水溶液,溶液变为蓝色。
b.再向得到的蓝色溶液中加入Na2S2O3溶液,溶液的蓝色褪去。
试剂X是
(3)为探究溶液变蓝快慢的影响因素,进行实验II、实验III。(溶液浓度均为0.01mol/L)
| 试剂 序号 用量(mL) | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | KI溶液(含淀粉) | H2O |
| 实验II | 5 | 4 | 8 | 3 | 0 |
| 实验III | 5 | 2 | x | y | z |
①实验III中,z的数值是
②对比实验II、实验III,可得出的实验结论是
(4)为探究其他因素对该“碘钟实验”的影响,进行实验IV。
(溶液浓度均为0.01mol/L)
| 试剂 序号 用量(mL) | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | KI溶液(含淀粉) | H2O |
| 实验IV | 4 | 4 | 9 | 3 | 0 |
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的原因:
您最近半年使用:0次
解题方法
6 . 草酸(HOOC-COOH,弱酸)及其化合物在工业中有重要作用。某实验小组同学在实验室利用两种方法制备草酸。回答下列问题:
(1)利用CO与亚硝酸甲酯(CH3ONO)先合成草酸二甲酯(CH3OOCCOOCH3),然后草酸二甲酯水解生成草酸。草酸二甲酯水解的化学方程式为_______ ;其中制备亚硝酸甲酯的反应为 ,实验室制备NO常用的试剂为
,实验室制备NO常用的试剂为_______ 。
(2)在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置(夹持仪器已省略)如图所示。
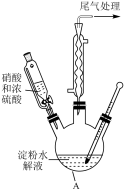
①仪器A的名称为_______ 。
②葡萄糖溶液可由反应 (淀粉)
(淀粉) (葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是
(葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是_______ 。
③反应在55℃~60℃进行,仪器A中除生成 外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗
外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗 的硝酸溶液的体积为
的硝酸溶液的体积为_______ mL。
④该实验中催化剂浓硫酸用量不宜过多,否则会导致草酸产率减少,其原因是_______ 。
(3)草酸具有较强的还原性,与氧化剂作用易被氧化成二氧化碳和水,故实验室可利用草酸测定次氯酸钠溶液的浓度。实验步骤如下:取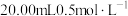 草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。
草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。
①次氯酸钠与草酸反应的离子方程式为_______ 。
②次氯酸钠溶液物质的量浓度为_______  。
。
(1)利用CO与亚硝酸甲酯(CH3ONO)先合成草酸二甲酯(CH3OOCCOOCH3),然后草酸二甲酯水解生成草酸。草酸二甲酯水解的化学方程式为
 ,实验室制备NO常用的试剂为
,实验室制备NO常用的试剂为(2)在浓硫酸催化作用下,用硝酸氧化葡萄糖可制取草酸,实验装置(夹持仪器已省略)如图所示。

①仪器A的名称为
②葡萄糖溶液可由反应
 (淀粉)
(淀粉) (葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是
(葡萄糖)得到。该实验中证明淀粉已经完全水解的实验操作及现象是③反应在55℃~60℃进行,仪器A中除生成
 外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗
外,同时也生成NO。要将16.2g淀粉完全水解后的淀粉水解液完全转化为草酸,理论上消耗 的硝酸溶液的体积为
的硝酸溶液的体积为④该实验中催化剂浓硫酸用量不宜过多,否则会导致草酸产率减少,其原因是
(3)草酸具有较强的还原性,与氧化剂作用易被氧化成二氧化碳和水,故实验室可利用草酸测定次氯酸钠溶液的浓度。实验步骤如下:取
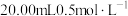 草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。
草酸溶液于锥形瓶中,用次氯酸钠溶液滴定,至终点时消耗次氯酸钠溶液为25.00mL。①次氯酸钠与草酸反应的离子方程式为
②次氯酸钠溶液物质的量浓度为
 。
。
您最近半年使用:0次
7 . 能证明淀粉已完全水解的现象是
| A.能发生银镜反应 | B.能溶于水 |
| C.有甜味 | D.遇碘不再变蓝 |
您最近半年使用:0次
2021-07-09更新
|
361次组卷
|
3卷引用:广东省广州市2020-2021学年高二下学期期末教学质量检测化学试题
8 . NaCl溶液中混有Na2SO4、CaCl2溶液和淀粉胶体,选择适当的试剂和方法从中提纯出NaCl晶体。相应的实验过程如下:
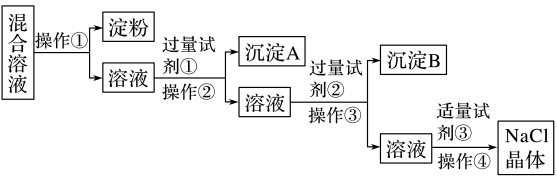
(1)写出上述实验过程中所用试剂(写化学式):试剂①_______ ;试剂③_______ 。
(2)判断试剂①已过量的方法是_______ 。
(3)用离子方程式表示加入试剂②的作用:_______ 。
(4)操作①是利用半透膜进行分离提纯。操作①的实验结果:淀粉_______ (填“能”或“不能”)透过半透膜;SO
_______ (填“能”或“不能”)透过半透膜。请用实验证明上述结果,完成下表(可不填满,也可增加)。限选试剂:1 mol·L-1 AgNO3溶液、1 mol·L-1 BaCl2溶液、1 mol·L-1 Ba(NO3)2溶液、碘水、稀盐酸、稀硝酸

(1)写出上述实验过程中所用试剂(写化学式):试剂①
(2)判断试剂①已过量的方法是
(3)用离子方程式表示加入试剂②的作用:
(4)操作①是利用半透膜进行分离提纯。操作①的实验结果:淀粉

| 编号 | 实验操作 | 预期现象和结论 |
| ① | ||
| ② |
您最近半年使用:0次
2021-10-18更新
|
380次组卷
|
6卷引用:2015-2016学年安徽师大附属中学高一上期中测试化学试卷
2015-2016学年安徽师大附属中学高一上期中测试化学试卷2016-2017学年广西陆川中学高一上期中化学卷【全国百强校】广东省佛山市第一中学2018-2019学年高一上学期第一次段考化学试题人教版(2019)高一必修第一册 第一章 物质及其变化 第二节 离子反应(已下线)3.3.1 粗盐提纯 从海水中提取溴(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省齐齐哈尔市龙江县第一中学2021-2022学年高一9月月考化学试题
名校
解题方法
9 . 为了检验淀粉水解的产物,设计如图实验方案:
淀粉液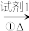 水解液
水解液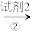 混合液
混合液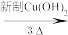 砖红色沉淀
砖红色沉淀
请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是_______ ;
(2)试剂2为_______ ,其作用是_______ ,使检验水解产物的实验得以顺利进行,发生反应的离子方程式为:_______ ;
(3)反应①的化学方程式为_______ ;
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是_______ ;
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的_______ (填”能”或”否”)否,若不能,其原因是_______ ,最简单的改正措施是_______ 。
淀粉液
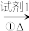 水解液
水解液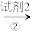 混合液
混合液 砖红色沉淀
砖红色沉淀请回答下列问题:
(1)试剂1为20%的H2SO4溶液,其作用是
(2)试剂2为
(3)反应①的化学方程式为
(4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是
(5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的
您最近半年使用:0次
10 . 化合物X仅含三种元素,通过如下实验推断其组成:
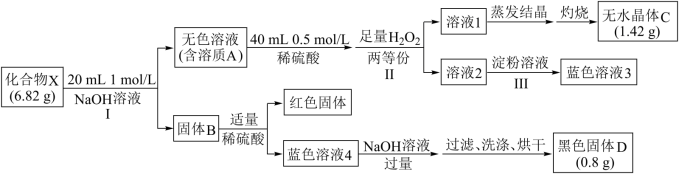
已知:X、A、B、C、D均为单一物质。
请回答:
(1)组成X的元素是___________ (填元素符号),X的化学式是___________ 。
(2)步骤Ⅰ,发生的化学方程式是___________ 。
(3)灼热黑色固体D投入乙醇中,固体变红,写出相应的化学方程式___________ 。
(4)步骤Ⅱ, 与A反应时理论消耗的物质的量之比是1∶2,但
与A反应时理论消耗的物质的量之比是1∶2,但 实际消耗量却明显偏大,其原因是
实际消耗量却明显偏大,其原因是___________ 。请设计实验证明___________ 。

已知:X、A、B、C、D均为单一物质。
请回答:
(1)组成X的元素是
(2)步骤Ⅰ,发生的化学方程式是
(3)灼热黑色固体D投入乙醇中,固体变红,写出相应的化学方程式
(4)步骤Ⅱ,
 与A反应时理论消耗的物质的量之比是1∶2,但
与A反应时理论消耗的物质的量之比是1∶2,但 实际消耗量却明显偏大,其原因是
实际消耗量却明显偏大,其原因是
您最近半年使用:0次



