名校
1 . 电子数相等的微粒叫等电子体,下列微粒组是等电子体的是
| A.N2O4和NO2 | B.Na+和Cl- | C. 和 和 | D.NO和O2 |
您最近一年使用:0次
2021-04-08更新
|
137次组卷
|
4卷引用:宁夏长庆高级中学2020-2021学年高二上学期期中考试化学试卷
名校
解题方法
2 . 我国科学家率先合成了新拓扑结构的储氢材料,镁、钛、钒、铁等一些金属形成的化合物及合金有异乎寻常的储氢能力。回答下列问题:
(1)基态铁原子失电子成为Fe3+,Fe3+的价电子排布图是___________ 。
(2)V2+与N2H4、H2O2、乙二胺(H2NCH2CH2NH2)等能形成配离子,在N2H4和H2O2中的非金属元素第一电离能由大到小的顺序是___________ ,N2H4中氮原子的杂化方式为___________ ,乙二胺和三甲胺[N(CH3)3]均属于胺,且相对分子质量相近,但乙二胺比三甲胺的沸点高得多,原因是___________ 。
(3)莫氏硬度是衡量矿物硬度的一种标准,其值越大则硬度越大。已知NaF和MgF2的莫氏硬度值分别为3.2和6.0,引起这种差异的主要原因是___________ 。
(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4)。 的空间构型为
的空间构型为___________ ,再写出与其互为等电子体的分子和离子___________ 、___________ 。
(5)配合物[Cu(CH3C≡N)4]BF4中铜的配位数为___________ ,配位体中σ键与π键个数之比为___________ 。
(6)某种铁镁合金储氢效率很高,其晶胞如图所示,
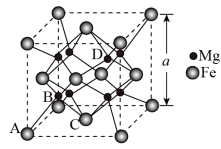
已知铁镁合金的晶胞参数为a pm,则铁镁之间的最短距离为___________ pm,该合金的密度为___________ g∙cm−3(只列出计算式即可)。
(1)基态铁原子失电子成为Fe3+,Fe3+的价电子排布图是
(2)V2+与N2H4、H2O2、乙二胺(H2NCH2CH2NH2)等能形成配离子,在N2H4和H2O2中的非金属元素第一电离能由大到小的顺序是
(3)莫氏硬度是衡量矿物硬度的一种标准,其值越大则硬度越大。已知NaF和MgF2的莫氏硬度值分别为3.2和6.0,引起这种差异的主要原因是
(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4)。
 的空间构型为
的空间构型为(5)配合物[Cu(CH3C≡N)4]BF4中铜的配位数为
(6)某种铁镁合金储氢效率很高,其晶胞如图所示,

已知铁镁合金的晶胞参数为a pm,则铁镁之间的最短距离为
您最近一年使用:0次
名校
3 . 中国科学家团队成功合成了五氮阴离子盐(N5)6(H3O)3(NH4)4Cl,五氮阴离子(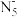 )是制备全氮类物质
)是制备全氮类物质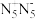 的中间体。下列说法正确的是
的中间体。下列说法正确的是
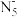 )是制备全氮类物质
)是制备全氮类物质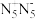 的中间体。下列说法正确的是
的中间体。下列说法正确的是A.键角: >H3O+ >H3O+ | B.电负性:N>O>H |
C.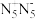 属于离子化合物 属于离子化合物 | D.基态Cl-的价电子排布图为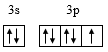 |
您最近一年使用:0次
2020-12-27更新
|
348次组卷
|
6卷引用:宁夏石嘴山市第三中学2021届高三上学期第三次月考(期末)化学试题
宁夏石嘴山市第三中学2021届高三上学期第三次月考(期末)化学试题山东省莱芜第一中学2021届高三12月检测化学试题四川省西昌市2020-2021学年高二下学期期中检测化学试题(已下线)卷14 物质结构与性质选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)专题4 分子空间结构与物质性质 本专题达标检测江西省景德镇一中2022-2023学年高二上学期期中考试化学试题
名校
4 . X、Y两元素可形成X2Y3型化合物,则X、Y原子基态时价电子的电子排布不可能是
| A.X:2s22p1Y:2s22p4 | B.X:3s23p1Y:2s22p4 |
| C.X:3s2Y:2s22p3 | D.X:2s22p3Y:2s22p4 |
您最近一年使用:0次
2020-10-29更新
|
416次组卷
|
4卷引用:宁夏银川一中2020-2021学年高二下学期期末考试化学试题



