名校
解题方法
1 . a、b、c、d、e、f分别是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:下图甲表示的是这六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。
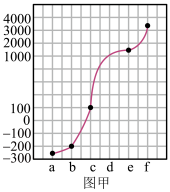
回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为___________ (用元素符号表示);
(2)元素b的单质的一个分子中含有___________ 个σ键和___________ 个π键;
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点___________ 乙的熔点(填>或<);
(4)元素d的基态原子的价电子排布式为___________ ;
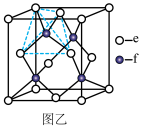
(5)元素e和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为___________ 丙的晶体类型为___________ ,在丙中,每个e原子周围最近的e原子数目为___________ 若晶胞参数为apm,则丙的密度表达式为___________ g・cm-3(用NA表示阿伏加德罗常数的值,丙的摩尔质量为Mg・mol-1)。

回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为
(2)元素b的单质的一个分子中含有
(3)c单质分别与氟气和氯气形成化合物甲和乙,则甲的熔点
(4)元素d的基态原子的价电子排布式为
(5)元素e和f可形成化合物丙(丙的晶胞结构如图乙所示),则丙的化学式为

您最近一年使用:0次
解题方法
2 . 金刚砂( )是重要的工业制品,可由二氧化硅与碳的反应制得:
)是重要的工业制品,可由二氧化硅与碳的反应制得: 。
。 的晶体结构与金刚石的相似,如本章如图所示,其中C原子和
的晶体结构与金刚石的相似,如本章如图所示,其中C原子和 原子的位置是交替的。
原子的位置是交替的。

(1)X是______ ?
(2)写出基态 原子的电子排布式
原子的电子排布式______ ; 中
中 的化合价是
的化合价是______ ?
(3)X可与氧气反应生成Y,判断Y分子的中心原子杂化轨道类型和键角______
(4) 晶体与晶体硅相比,熔点较高的是
晶体与晶体硅相比,熔点较高的是______ 晶体?请分析原因______
(5)在 中最小的环上有
中最小的环上有______ 个原子,已知 键的键能为a
键的键能为a ,理论上分解1
,理论上分解1
 形成气态原子所需要的能量是
形成气态原子所需要的能量是______ 。
 )是重要的工业制品,可由二氧化硅与碳的反应制得:
)是重要的工业制品,可由二氧化硅与碳的反应制得: 。
。 的晶体结构与金刚石的相似,如本章如图所示,其中C原子和
的晶体结构与金刚石的相似,如本章如图所示,其中C原子和 原子的位置是交替的。
原子的位置是交替的。
(1)X是
(2)写出基态
 原子的电子排布式
原子的电子排布式 中
中 的化合价是
的化合价是(3)X可与氧气反应生成Y,判断Y分子的中心原子杂化轨道类型和键角
(4)
 晶体与晶体硅相比,熔点较高的是
晶体与晶体硅相比,熔点较高的是(5)在
 中最小的环上有
中最小的环上有 键的键能为a
键的键能为a ,理论上分解1
,理论上分解1
 形成气态原子所需要的能量是
形成气态原子所需要的能量是
您最近一年使用:0次
3 . 不同尺寸的冠醚可以装载不同大小的金属离子,偶氮苯在紫外光与可见光的作用下会发生顺式与反式结构的转变。如下分子的结构中都包含冠醚和偶氮苯片段,请你想象这些分子具有怎样的性质特点、可能会有怎样的应用________ 。


您最近一年使用:0次
4 .  、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):

(1) 、金刚石和石墨三者的关系是互为_______。
、金刚石和石墨三者的关系是互为_______。
(2)固态时, 属于
属于_______ (填“离子”“共价”或“分子”)晶体。
(3)试根据金刚石和 的结构特点判断两者熔点的高低,并说明理由
的结构特点判断两者熔点的高低,并说明理由_______ 。
(4)硅晶体的结构跟金刚石相似, 硅晶体中含有
硅晶体中含有 键的数目是
键的数目是_______  个。
个。
(5)石墨层状结构中,平均每个正六边形占有的碳原子数是_______ 。
 、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
、金刚石和石墨的结构模型如下图所示(石墨仅表示出其中的一层结构):
(1)
 、金刚石和石墨三者的关系是互为_______。
、金刚石和石墨三者的关系是互为_______。| A.同分异构体 | B.同素异形体 | C.同系物 | D.同位素 |
 属于
属于(3)试根据金刚石和
 的结构特点判断两者熔点的高低,并说明理由
的结构特点判断两者熔点的高低,并说明理由(4)硅晶体的结构跟金刚石相似,
 硅晶体中含有
硅晶体中含有 键的数目是
键的数目是 个。
个。(5)石墨层状结构中,平均每个正六边形占有的碳原子数是
您最近一年使用:0次
解题方法
5 . 下列判断正确的是
| A.因为共价键有饱和性和方向性,所以原子晶体不遵循“紧密堆积”原理 |
| B.稳定性按 HF、HCl、HBr、HI 逐渐减弱,根本原因是 F、Cl、Br、I 非金属性减弱 |
| C.晶体中一定存在化学键,金属晶体熔点一定很高 |
| D.固体 SiO2 一定是晶体 |
您最近一年使用:0次
解题方法
6 . 下列说法中正确的是
| A.分子中键能越大,键角越大,则分子越稳定 |
| B.元素周期表中的ⅠA族(除H外)和ⅦA族元素的原子可能形成共价键 |
| C.水分子可表示为H-O-H,分子中键角为180° |
| D.H-O键键能为463KJ/mol,即18gH2O分解成H2和O2时,消耗能量为926kJ |
您最近一年使用:0次
名校
7 . 由金、氯、铯三种元素组成的晶体M的晶胞结构如图所示( 为铯,
为铯, 为氯,
为氯, 为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是
为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是

 为铯,
为铯, 为氯,
为氯, 为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是
为金),其中金原子有两种不同的化学环境,形成2种−1价的配离子。设阿伏加德罗常数的值为NA,下列说法错误的是
| A.M的化学式为CsAuCl |
B.金原子形成的两种配离子分别为AuCl 、AuCl 、AuCl |
| C.位于体心的Au处于由Au构成的八面体空隙中 |
D.金晶体(Au)是面心立方堆积,其晶胞参数为408pm,金晶体密度为 g∙cm−3 g∙cm−3 |
您最近一年使用:0次
2022-09-11更新
|
340次组卷
|
2卷引用:辽宁省抚顺市第二中学2021-2022学年高三上学期10月月考化学试题
2022·广东·高考真题
8 . 硒( )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为_______ 。
(2) 的沸点低于
的沸点低于 ,其原因是
,其原因是_______ 。
(3)关于I~III三种反应物,下列说法正确的有_______ 。
A.I中仅有 键
键
B.I中的 键为非极性共价键
键为非极性共价键
C.II易溶于水
D.II中原子的杂化轨道类型只有 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_______ 。
(5)硒的两种含氧酸的酸性强弱为
_______  (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为_______ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。_______ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为_______  (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 )是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(
)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光( )效应以来,
)效应以来, 在发光材料、生物医学等领域引起广泛关注。一种含
在发光材料、生物医学等领域引起广泛关注。一种含 的新型
的新型 分子
分子 的合成路线如下:
的合成路线如下: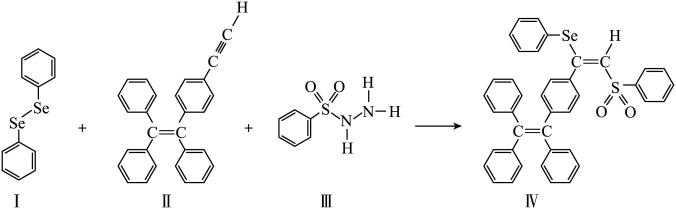
 与S同族,基态硒原子价电子排布式为
与S同族,基态硒原子价电子排布式为(2)
 的沸点低于
的沸点低于 ,其原因是
,其原因是(3)关于I~III三种反应物,下列说法正确的有
A.I中仅有
 键
键B.I中的
 键为非极性共价键
键为非极性共价键C.II易溶于水
D.II中原子的杂化轨道类型只有
 与
与
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有
(5)硒的两种含氧酸的酸性强弱为

 (填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠(
(填“>”或“<”)。研究发现,给小鼠喂食适量硒酸钠( )可减轻重金属铊引起的中毒。
)可减轻重金属铊引起的中毒。 的立体构型为
的立体构型为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
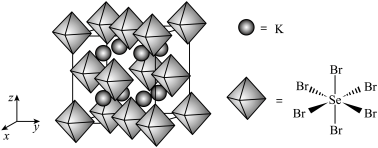
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 (列出计算式,
(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近一年使用:0次
2022-06-10更新
|
12208次组卷
|
28卷引用:专题九 物质结构与性质-实战高考·二轮复习核心突破
(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破2022年新高考广东化学高考真题(已下线)2022年广东卷高考真题变式题(17-21)(已下线)专题17 物质结构与性质(综合题)-2022年高考真题模拟题分项汇编(已下线)专题18 物质结构与性质(综合题)-三年(2020-2022)高考真题分项汇编(已下线)第19练 物质结构与性质综合题难点突破-2022年【暑假分层作业】高二化学(2023届一轮复习通用)山东省菏泽市单县二中2021-2022学年高二下学期期末测试化学试题山西省晋城市第一中学2022-2023学年高三上学期第五次调研考试化学试题(已下线)第一部分 二轮专题突破 大题突破4 物质结构与性质大题研究(选考)(已下线)题型11 物质结构与性质的综合分析与推断(已下线)回归教材重难点12 原子、分子和晶体结构再归纳-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)广东省广州中学2022-2023学年高二下学期期中考试化学试题江西省景德镇一中2022-2023学年高二下学期期中考试(19班)化学试题河南省淮滨高级中学2022-2023学年高二下学期期中教学质量检测化学试题(已下线)专题20 结构与性质(已下线)专题20 结构与性质(已下线)第21练 物质结构与性质综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)T35-物质结构与性质(已下线)专题17 物质结构与性质综合题-2023年高考化学真题题源解密(新高考专用)河南省信阳市第十高级中学2022-2023学年高二下学期期中教学质量检测化学试卷广东省汕头市金禧中学2023-024学年高三上学期第一次阶段考试化学试题上海市实验学校2023-2024学年高三上学期第一次月考化学试题四川省眉山市仁寿第一中学校(北校区)2023-2024学年高三上学期11月期中考试理综化学试题山东省日照神州天立高级中学高复部2023-2024学年高三上学期12月份阶段性测试化学试题北京市东直门中学2023-2024学年高三上学期12月阶段测试化学试题广东省四会中学、广信中学2023-2024学年高二下学期第一次联合考试化学试题2024届四川省眉山市仁寿县高三下学期三诊模拟联考理综试题-高中化学广东省广州市第六十五中学2023-2024学年高二下学期期中考试化学试题
名校
9 . 铁有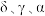 三种同素异形体,其晶胞结构如图所示,设NA为阿伏加德罗常数的值。下列说法正确的是
三种同素异形体,其晶胞结构如图所示,设NA为阿伏加德罗常数的值。下列说法正确的是
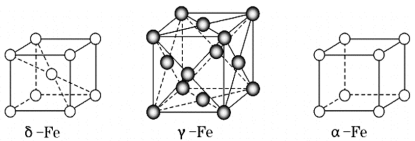
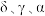 三种同素异形体,其晶胞结构如图所示,设NA为阿伏加德罗常数的值。下列说法正确的是
三种同素异形体,其晶胞结构如图所示,设NA为阿伏加德罗常数的值。下列说法正确的是
A.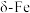 晶胞中含有2个铁原子,每个铁原子等距离且最近的铁原子有6个 晶胞中含有2个铁原子,每个铁原子等距离且最近的铁原子有6个 |
B.晶体的空间利用率: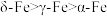 |
C.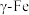 晶胞中的原子堆积方式为体心立方堆积 晶胞中的原子堆积方式为体心立方堆积 |
D.铁原子的半径为acm,则 晶胞的密度为 晶胞的密度为 |
您最近一年使用:0次
2022-04-22更新
|
345次组卷
|
7卷引用:河北省唐山市曹妃甸区第一中学2020-2021学年高二下学期6月月考化学试题
名校
解题方法
10 . 钠离子电池是被认为在基于电网的储能系统中最具发展前景,双金属硫化物 空心纳米棒将有助于提高钠离子电池性能。回答下列问题:
空心纳米棒将有助于提高钠离子电池性能。回答下列问题:
(1) 位于第五周期,与N同主族,基态
位于第五周期,与N同主族,基态 的价电子排布图(轨道表达式)为
的价电子排布图(轨道表达式)为___________ ,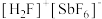 (氟酸锑)是一种超强酸,
(氟酸锑)是一种超强酸,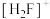 的空间构型为
的空间构型为___________ ,与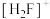 具有相同空间构型和键合形式的阴离子为
具有相同空间构型和键合形式的阴离子为___________ 。
(2) Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是___________ ,第一电离能由大到小的顺序是___________ 。
(3)与S同主族的元素有O、Se、Te等,它们氢化物的沸点大小为 ,其原因是
,其原因是___________ 。
(4)已知: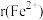 为
为 ,
, 为
为 。在隔绝空气条件下分别加热
。在隔绝空气条件下分别加热 和
和 ,实验测得
,实验测得 的分解温度低于
的分解温度低于 ,原因是
,原因是___________ 。
(5)某离子型铁的氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为___________ ;已知该晶体的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的晶胞参数
,则该晶体的晶胞参数
___________  (用含d和
(用含d和 的代数式表示)。
的代数式表示)。

 空心纳米棒将有助于提高钠离子电池性能。回答下列问题:
空心纳米棒将有助于提高钠离子电池性能。回答下列问题:(1)
 位于第五周期,与N同主族,基态
位于第五周期,与N同主族,基态 的价电子排布图(轨道表达式)为
的价电子排布图(轨道表达式)为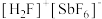 (氟酸锑)是一种超强酸,
(氟酸锑)是一种超强酸,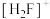 的空间构型为
的空间构型为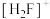 具有相同空间构型和键合形式的阴离子为
具有相同空间构型和键合形式的阴离子为(2) Si、P与S是同周期中相邻的元素,Si、P、S的电负性由大到小的顺序是
(3)与S同主族的元素有O、Se、Te等,它们氢化物的沸点大小为
 ,其原因是
,其原因是(4)已知:
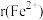 为
为 ,
, 为
为 。在隔绝空气条件下分别加热
。在隔绝空气条件下分别加热 和
和 ,实验测得
,实验测得 的分解温度低于
的分解温度低于 ,原因是
,原因是(5)某离子型铁的氧化物晶胞如图所示,它由X、Y组成,则该氧化物的化学式为
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则该晶体的晶胞参数
,则该晶体的晶胞参数
 (用含d和
(用含d和 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2021-12-31更新
|
1187次组卷
|
4卷引用:八省八校(T8联考)2021-2022学年高三上学期第一次联考化学试题(石家庄二中)
八省八校(T8联考)2021-2022学年高三上学期第一次联考化学试题(石家庄二中)(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)2022年全国甲卷高考真题变式题(非选择题)吉林省双辽市一中、大安市一中、通榆县一中等重点高中2021-2022学年高三上学期期末联考理科综合化学试题



