真题
名校
1 . 硅是重要的半导体材料,构成了现代电子工业的基础。请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为_______ ,该能层具有的原子轨道数为________ 、电子数为___________ 。
(2)硅主要以硅酸盐、___________ 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以___________ 相结合,其晶胞中共有8个原子,其中在面心位置贡献__________ 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为___________________________________ 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是______ 。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是___________________________ 。
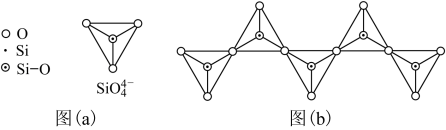
(6)在硅酸盐中,SiO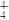 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为______ ,Si与O的原子数之比为_________ ,化学式为__________________ 。
(1)基态Si原子中,电子占据的最高能层符号为
(2)硅主要以硅酸盐、
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 | C—C | C—H | C—O | Si—Si | Si—H | Si—O |
| 键能/(kJ•mol-1 | 356 | 413 | 336 | 226 | 318 | 452 |
②SiH4的稳定性小于CH4,更易生成氧化物,原因是
(6)在硅酸盐中,SiO
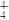 四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
四面体(如下图(a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b)为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为
您最近一年使用:0次
2019-01-30更新
|
3759次组卷
|
9卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅰ卷)
真题
名校
2 . [化学——选修3:物质结构与性质]碳及其化合物广泛存在于自然界中,回答下列问题:
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态原子中,核外存在______ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是_____________ 。
(3)CS2分子中,共价键的类型有_____________ ,C原子的杂化轨道类型是_______ ,写出两个与CS2具有相同空间构型和键合形式的分子或离子_______________ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于_____ 晶体。
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接_____ 个六元环,每个六元环占有___ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接________ 个六元环,六元环中最多有________ 个C原子在同一平面。
(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次
2016-12-09更新
|
5123次组卷
|
12卷引用:2015年全国普通高等学校招生统一考试化学(新课标I卷)
2015年全国普通高等学校招生统一考试化学(新课标I卷)2016届广东省深圳第二外国语学校高三上学期第二次教学质检化学试卷2016届黑龙江省哈尔滨一中高三上学期12月月考化学试卷重庆市垫江县2018届高三上学期模底考试理综化学试题宁夏石嘴山市第三中学2018届高三9月月考化学试题百所名校联考-物质结构与性质云南省曲靖市第一中学2020届高三化学仿真模拟考试理科综合化学试题云南省曲靖一中2020届高考化学仿真试卷河北省石家庄市第二中学2020届高中毕业班四月份教学质量监测卷理科综合化学部分安徽省马鞍山市2020届高考第二次模拟理综化学试题辽宁省沈阳东北育才中学2020年高中毕业班教学质量监测卷理科综合化学试题四川省宜宾市第四中学2021届高三上学期开学考试理综化学试题
真题
名校
3 . 氟在自然界中常以CaF2的形式存在。
(1)下列关于CaF2的表述正确的是_______ 。
a.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
b.Ca2+与F-间仅存在静电吸引作用
c.阴阳离子比为2:1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是__________________________ (用离子方程式表示)。 已知AlF63-在溶液中可稳定存在。
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为___________ ,其中氧原子的杂化方式为_________ 。
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) △H=-313kJ·mol-1,F-F键键能为159kJ·mol-1,Cl-Cl键键能为242kJ·mol-1,则ClF3中Cl-F键的平均键能为_________ kJ·mol-1。ClF3的熔、沸点比BrF3的________ (填“高”或“低”)。
(1)下列关于CaF2的表述正确的是
a.F-的离子半径小于Cl-,则CaF2的熔点高于CaCl2
b.Ca2+与F-间仅存在静电吸引作用
c.阴阳离子比为2:1的物质,均与CaF2晶体构型相同
d.CaF2中的化学键为离子键,因此CaF2在熔融状态下能导电
(2)CaF2难溶于水,但可溶于含Al3+的溶液中,原因是
(3)F2通入稀NaOH溶液中可生成OF2,OF2分子构型为
(4)F2与其他卤素单质反应可以形成卤素互化物,例如ClF3、BrF3等。已知反应Cl2(g)+3F2(g)=2ClF3(g) △H=-313kJ·mol-1,F-F键键能为159kJ·mol-1,Cl-Cl键键能为242kJ·mol-1,则ClF3中Cl-F键的平均键能为
您最近一年使用:0次
2016-12-09更新
|
1638次组卷
|
10卷引用:2015年全国普通高等学校招生统一考试化学(山东卷)
2015年全国普通高等学校招生统一考试化学(山东卷)河北省馆陶县第一中学2016-2017学年高二下学期期中考试化学试题山西省原平市范亭中学2016-2017学年高二下学期期末考试化学试题(已下线)二轮复习 专题17 物质结构与性质 押题专练河北省邢台市第二中学2017-2018学年高二化学选修三课时训练:3.4 离子晶体吉林省长春市东北师大附中2020届高中毕业班二月份网络教学质量监测卷理科综合化学部分贵州省贵阳市第一中学2020届高三教学质量监测理科综合化学试题福建省莆田第一中学2019-2020学年高二下学期期中考试化学试题安徽省蚌埠第三中学2019-2020学年高二下学期期末考试化学试题四川省巴中市平昌县驷马中学2020-2021学年高二上学期 十一月月考化学试题
真题
4 . X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。请回答下列问题:
(1)Y基态原子的电子排布式是________ ;Z所在周期中第一电离能最大的主族元素是_____ 。
(2)XY2-离子的立体构型是_______ ;R2+的水合离子中,提供孤电子对的是原子是______ 。
(3)Z与某元素形成的化合物的晶胞如右图所示,晶胞中阴离子与阳离子的个数之比是___________ 。

(4)将R单质的粉末加入XH3的浓溶液中,通入Y2,充分反应后溶液呈深蓝色,该反应的离子方程式是____________ 。
(1)Y基态原子的电子排布式是
(2)XY2-离子的立体构型是
(3)Z与某元素形成的化合物的晶胞如右图所示,晶胞中阴离子与阳离子的个数之比是

(4)将R单质的粉末加入XH3的浓溶液中,通入Y2,充分反应后溶液呈深蓝色,该反应的离子方程式是
您最近一年使用:0次
2016-12-09更新
|
2750次组卷
|
5卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(四川卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(四川卷)(已下线)2015届江苏省海安中学、常州一中、沭阳中学高三联合调研化学试卷2014-2015云南德宏州芒市第一中学高二下学期期中化学试卷陕西省黄陵中学2016-2017学年高二(重点班)下学期第四学月考试化学试题人教版化学选修三第3章《晶体结构与性质》测试题
真题
名校
5 . 石墨烯(如图甲)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图乙).
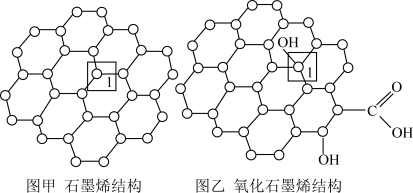

(1)图甲中,1号C与相邻C形成σ键的个数为___________ .
(2)图乙中,1号C的杂化方式是___________ ,该C与相邻C形成的键角___________ (填“>”“<”或“=”)图甲中1号C与相邻C形成的键角.
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有___________ (填元素符号).
(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为___________ ,该材料的化学式为___________ 。


(1)图甲中,1号C与相邻C形成σ键的个数为
(2)图乙中,1号C的杂化方式是
(3)若将图乙所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有
(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图丙所示,M原子位于晶胞的棱上与内部,该晶胞中M原子的个数为
您最近一年使用:0次
2016-12-09更新
|
2007次组卷
|
8卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(山东卷)
真题
6 . 胃舒平主要成分是氢氧化铝,同时含有三硅酸镁( )等化合物。
)等化合物。
(1)三硅酸镁的氧化物形式为_______ ,某元素与镁元素不同周期但在相邻一族,且性质和镁元素十分相似,该元素原子核外电子排布式为_______ 。
(2)铝元素的原子核外共有_______ 种不同运动状态的电子、_______ 种不同能级的电子。
(3)某元素与铝元素同周期且原子半径比镁原子半径大,该元素离子半径比铝离子半径_______ (填“大”或“小”),该元素与铝元素的最高价氧化物的水化物之间发生反应的离子方程式为:_______
(4) 、MgO和
、MgO和 都可以制耐火材料, 其原因是
都可以制耐火材料, 其原因是_______ 。
a. 、MgO和
、MgO和 都不溶于水
都不溶于水
b. 、MgO和
、MgO和 都是白色固体
都是白色固体
c. 、MgO和
、MgO和 都是氧化物
都是氧化物
d. 、MgO和
、MgO和 都有很高的熔点
都有很高的熔点
 )等化合物。
)等化合物。(1)三硅酸镁的氧化物形式为
(2)铝元素的原子核外共有
(3)某元素与铝元素同周期且原子半径比镁原子半径大,该元素离子半径比铝离子半径
(4)
 、MgO和
、MgO和 都可以制耐火材料, 其原因是
都可以制耐火材料, 其原因是a.
 、MgO和
、MgO和 都不溶于水
都不溶于水b.
 、MgO和
、MgO和 都是白色固体
都是白色固体 c.
 、MgO和
、MgO和 都是氧化物
都是氧化物 d.
 、MgO和
、MgO和 都有很高的熔点
都有很高的熔点
您最近一年使用:0次
真题
解题方法
7 . 胃舒平主要成分是氢氧化铝,同时含有三硅酸镁( )等化合物。
)等化合物。
1)三硅酸镁的氧化物形式为_______ ,某元素与镁元素不同周期但在相邻一族,且性质和镁元素十分相似,该元素原子核外电子排布式为_______ 。
2)铝元素的原子核外共有________ 种不同运动状态的电子、_______ 种不同能级的电子。
3)某元素与铝元素同周期且原子半径比镁原子半径大,该元素离子半径比铝离子半径____ (填“大”或“小”),该元素与铝元素的最高价氧化物的水化物之间发生反应的离子方程式为:______
4)Al2O3、MgO和SiO2都可以制耐火材料, 其原因是______ 。
a.Al2O3、MgO和SiO2都不溶于水
b.Al2O3、MgO和SiO2都是白色固体
c.Al2O3、MgO和SiO2都是氧化物
d.Al2O3、MgO和SiO2都有很高的熔点
 )等化合物。
)等化合物。1)三硅酸镁的氧化物形式为
2)铝元素的原子核外共有
3)某元素与铝元素同周期且原子半径比镁原子半径大,该元素离子半径比铝离子半径
4)Al2O3、MgO和SiO2都可以制耐火材料, 其原因是
a.Al2O3、MgO和SiO2都不溶于水
b.Al2O3、MgO和SiO2都是白色固体
c.Al2O3、MgO和SiO2都是氧化物
d.Al2O3、MgO和SiO2都有很高的熔点
您最近一年使用:0次
真题
名校
8 . 在2008年初我国南方遭遇的冰雪灾害中,使用了一种融雪剂,其主要成分的化学式为XY2,X、Y为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 molXY2含有54 mol电子。
(1)该融雪剂的化学式是_______ ;X与氢元素形成的化合物的电子式是_______ 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是_______ ;D与E能形成一种非极性分子,该分子的结构式为_______ ;D所在族元素的氢化物中,沸点最低的是_______ 。
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是_______ 。
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为_______ 。
(1)该融雪剂的化学式是
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
(3)元素W与Y同周期,其单质是原子晶体;元素Z的单质分子Z2中有3个共价键;W与Z能形成一种新型无机非金属材料,其化学式是
(4)元素R与Y同主族,其氢化物能用于刻蚀玻璃,R2与NaOH溶液反应的产物之一是OR2,该反应的离子方程式为
您最近一年使用:0次
2016-12-09更新
|
903次组卷
|
4卷引用:2008年普通高等学校招生统一考试理综试题化学部分(重庆卷)
2008年普通高等学校招生统一考试理综试题化学部分(重庆卷)(已下线)2011届嘉禾一中高三第一次摸底考试化学卷(已下线)2012届陕西省师大附中高三10月份月考化学试卷安徽省郎溪中学、泾县中学2020-2021学年高一下学期3月联考化学试题
真题
9 . Na、Cu、O、Si、S、Cl是常见的六种元素。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
(1)Na位于元素周期表第 周期第 族;S的基态原子核外有 个未成对电子;Si的基态原子核外电子排布式为 。
(2)用“>”或“<”填空:
| 第一电离能 | 离子半径 | 熔点 | 酸性 |
| Si S | O2- Na+ | NaCl Si | H2SO4 HClO4 |
(3)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101KPa下,已知该反应每消耗1 mol CuCl2(s),放热44.4KJ,该反应的热化学方程式是 。
(4)ClO2是常用于水的净化,工业上可用Cl2氧化NaClO2溶液制取ClO2。写出该反应的离子方程式,并标出电子转移的方向和数目 。
您最近一年使用:0次
2014-06-20更新
|
3035次组卷
|
6卷引用:2014年全国普通高等学校招生统一考试理科综合能力测试化学(安徽卷)
2014年全国普通高等学校招生统一考试理科综合能力测试化学(安徽卷)(已下线)2015届安徽省黄山市徽州一中高三第一次月考化学试卷2016届四川省攀枝花十二中高三下学期第一次月考化学试卷(已下线)2019高考备考二轮复习精品资料-专题3 氧化还原反应(教学案)(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)2021年天津高考化学试题变式题13-16
真题
10 . 金属镍在电池、合金、催化剂等方面应用广泛.
(1)下列关于金属及金属键的说法正确的是_____ .
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是____ .
(3)过滤金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=___ .CO与N2结构相似,CO分子内σ键与π键个数之比为______ .
(4)甲醛(H2C═O)在Ni催化作用下加氢可得甲醇(CH3OH).甲醇分子内C原子的杂化方式为_____ ,甲醇分子内的O﹣C﹣H键角____ (填“大于”“等于”或“小于”)甲醛分子内的O﹣C﹣H键角.
(1)下列关于金属及金属键的说法正确的是
a.金属键具有方向性与饱和性
b.金属键是金属阳离子与自由电子间的相互作用
c.金属导电是因为在外加电场作用下产生自由电子
d.金属具有光泽是因为金属阳离子吸收并放出可见光
(2)Ni是元素周期表中第28号元素,第二周期基态原子未成对电子数与Ni相同且电负性最小的元素是
(3)过滤金属配合物Ni(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=
(4)甲醛(H2C═O)在Ni催化作用下加氢可得甲醇(CH3OH).甲醇分子内C原子的杂化方式为
您最近一年使用:0次
2014-06-05更新
|
1800次组卷
|
3卷引用:2012年普通高等学校招生全国统一考试化学(山东卷)



