解题方法
1 . 红蓝宝石、祖母绿、金绿猫眼、钻石为举世公认的珍贵宝石。
(1)红宝石是刚玉的一种,主要成分为氧化铝( ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为_______ 。
(2)祖母绿主要成分的化学式为 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)_______ I(Al)。Be能与NaOH溶液反应,请简单说明判断依据:_______ 。
(3)金绿猫眼主要成分的化学式为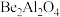 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为_______ 。 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式并解释其形成原因:
的结构式并解释其形成原因:_______ 。
(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为_______ 。金刚石晶胞结构如图所示,与晶胞面心处碳原子距离最近且等距离的碳原子数为_______ 。

(1)红宝石是刚玉的一种,主要成分为氧化铝(
 ),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为
),因含微量杂质元素铬(Cr)而呈红色。基态铬原子的简化电子排布式为(2)祖母绿主要成分的化学式为
 ,Be与Al的第一电离能大小关系为:I(Be)
,Be与Al的第一电离能大小关系为:I(Be)(3)金绿猫眼主要成分的化学式为
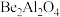 ,经碱熔酸浸可得到
,经碱熔酸浸可得到 和
和 ,
, 分子的空间构型为
分子的空间构型为 常以二聚分子
常以二聚分子 的形式存在,分子中所有原子均达到8稳定结构,请画出
的形式存在,分子中所有原子均达到8稳定结构,请画出 的结构式并解释其形成原因:
的结构式并解释其形成原因:(4)钻石是经过琢磨的金刚石,金刚石熔点高于晶体硅,原因为

您最近一年使用:0次
2 . 钛是20世纪50年代发展起来的一种重要的结构金属,钛合金因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。回答下列问题:
(1)钛元素在元素周期表中的位置___________ 。
(2)二氧化钛与 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
① 的空间构型为
的空间构型为___________ , 中σ键和π键的数目比为
中σ键和π键的数目比为___________ 。
② 是
是___________ 分子。(填“极性”或“非极性”)
(3)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示:
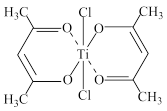
①碳原子的杂化类型有___________ 种。
②该配合物中存在的化学键有___________ (填字母)。
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中与N原子距离最近且相等的Ti原子有________ 个;若该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中Ti原子与N原子的最近距离为
,则晶胞中Ti原子与N原子的最近距离为_________ pm。(用含ρ、 的代数式表示)
的代数式表示)

(1)钛元素在元素周期表中的位置
(2)二氧化钛与
 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。①
 的空间构型为
的空间构型为 中σ键和π键的数目比为
中σ键和π键的数目比为②
 是
是(3)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示:

①碳原子的杂化类型有
②该配合物中存在的化学键有
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中与N原子距离最近且相等的Ti原子有
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中Ti原子与N原子的最近距离为
,则晶胞中Ti原子与N原子的最近距离为 的代数式表示)
的代数式表示)
您最近一年使用:0次
2022-11-16更新
|
1264次组卷
|
4卷引用:北京市海淀区2022届高三一模(结构与性质)
(已下线)北京市海淀区2022届高三一模(结构与性质)辽宁省六校2022-2023学年高三上学期期中联考化学试题山东省曹县第一中学2023届高三上学期12月月考化学试题(已下线)期中模拟预测卷01(测试范围:选择性必修2)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)
名校
解题方法
3 . C和Si元素在化学中占有极其重要的地位。
(1)写出Si的基态原子核外最外层电子排布式_______ ,C、O、Si三种元素的电负性由大到小的顺序为_______ 。
(2)干冰是分子晶体,其密度比冰大的原因是_______ 。SiC晶体的结构与晶体硅的相似,其中C原子的杂化方式为_______ 。
(3)氧化物XO的电子总数与SiC的相等,则X为_______ (填元素符号),XO是优良的耐高温材料,其熔点比CaO高的原因是_______ 。
(4)向盛有硫酸铜水溶液的试管中加氨水,先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解的原因是:_______ 。
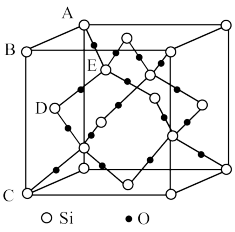
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含_______ 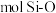 键。如果该立方体的边长为
键。如果该立方体的边长为 ,用
,用 表示阿伏加德罗常数,则SiO2晶体的密度表达式为
表示阿伏加德罗常数,则SiO2晶体的密度表达式为_______  。
。
(1)写出Si的基态原子核外最外层电子排布式
(2)干冰是分子晶体,其密度比冰大的原因是
(3)氧化物XO的电子总数与SiC的相等,则X为
(4)向盛有硫酸铜水溶液的试管中加氨水,先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液。在这个过程中先生成蓝色沉淀,后沉淀溶解的原因是:
(5)下图表示的是SiO2的晶胞结构(白圈代表硅原子,黑点代表氧原子),判断在30g二氧化硅晶体中含
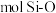 键。如果该立方体的边长为
键。如果该立方体的边长为 ,用
,用 表示阿伏加德罗常数,则SiO2晶体的密度表达式为
表示阿伏加德罗常数,则SiO2晶体的密度表达式为 。
。
您最近一年使用:0次
2022-10-30更新
|
1740次组卷
|
3卷引用:北京市海淀区2022届高三一模(结构与性质)
4 . 锶(Sr)为碱土金属,与钙、钡在周期表的同一列,三者原子的最外层电子数相同均为2,性质相似,锶的金属活性也与钙和钡接近,并介于二者之间。其氧化物和氢氧化物都有重要的工业用途。氧化锶是白色粉末,用于制造烟火、颜料,并用于医药等。氢氧化锶被用作聚乙烯塑料(PE)的稳定剂;也用于改进干性油和油漆的干燥性。
(1)氧化锶(SrO)在空气中极易吸收空气中的二氧化碳,反应方程式为:___________
(2)氢氧化锶属于___________ 类化合物,性质与___________ 相似,写出下列反应的方程式:
①Sr(OH)2与Cu(NO3)2反应:___________ 。
②H2SO4与氢氧化锶溶液反应可生成沉淀,反应方程式为:___________ 。
(3)某兴趣小组的同学向盛有一定体积氢氧化锶溶液的烧杯中逐渐通入 气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。
气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。

曲线AB段导电能力不断减弱的原因是:___________ 。
(1)氧化锶(SrO)在空气中极易吸收空气中的二氧化碳,反应方程式为:
(2)氢氧化锶属于
①Sr(OH)2与Cu(NO3)2反应:
②H2SO4与氢氧化锶溶液反应可生成沉淀,反应方程式为:
(3)某兴趣小组的同学向盛有一定体积氢氧化锶溶液的烧杯中逐渐通入
 气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。
气体,并测得所得体系的导电能力随通入CO2体积变化的曲线如图所示。
曲线AB段导电能力不断减弱的原因是:
您最近一年使用:0次
名校
解题方法
5 . 铜的配合物在自然界中广泛存在,请回答下列问题:
(1)基态29Cu的核外电子排布式为____ 。
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子____ (填化学式),配体中提供孤电子对的原子是____ (填元素符号)。
②H2O、SO 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为____ 、____ 。
(3)同学甲设计如图制备铜的配合物的实验:

已知:铜离子的配位数通常为4。
①结合化学平衡原理解释试管c中浑浊液转变为深蓝色溶液的原因____ 。
②由上述实验可得出以下结论:结论1:配合物的形成与____ 、____ 有关。
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:____>____(填化学式)。____
(1)基态29Cu的核外电子排布式为
(2)硫酸铜溶液中存在多种微粒:
①硫酸铜溶液呈蓝色的原因是其中存在配离子
②H2O、SO
 中心原子的杂化轨道类型分别为
中心原子的杂化轨道类型分别为(3)同学甲设计如图制备铜的配合物的实验:

已知:铜离子的配位数通常为4。
①结合化学平衡原理解释试管c中浑浊液转变为深蓝色溶液的原因
②由上述实验可得出以下结论:结论1:配合物的形成与
结论2:试管b、c中深蓝色配离子的稳定性强弱顺序为:____>____(填化学式)。
您最近一年使用:0次



