名校
1 .
铁和钴是重要的过渡元素。
(l)钴位于元素周期表中第_____ 族,其基态原子中未成对电子的个数为______ .
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为___________ ;尿素分子中N原子的杂化方式是_____ ,所含非金属元素的电负性由大到小的顺序是___________ 。
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀.
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为_______ 。
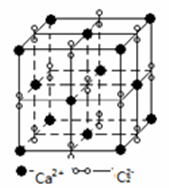
(4)离子化合物CaC2的一种晶体结构如图。从钙离子看,属于_____ 堆积,其配位数是_____ ;一个晶胞含有的σ键平均有______ 个。
(5)科学研究结果表明.碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH。其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是______ .
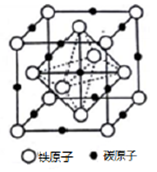
(6)奥氏体是碳溶解在γ—Fe中形成的一种间隙固溶体,无磁性,其晶胞如右图所示,则该物质的化学式为________ ,若晶体密度为dg/cm3,则晶胞中最近的两个碳原子的距离为____ pm。(阿伏伽德罗常数的值用NA表示,写出简化后的计算式即可)。
铁和钴是重要的过渡元素。
(l)钴位于元素周期表中第
(2)[Fe(H2NCONH2)6](NO3)3的名称是三硝酸六尿素合铁(Ⅲ),是一种重要的配合物。该化合物中中心离子Fe3+的核外价电子排布式为
(3)Co(NH3)5BrSO4可形成两种结构的钴的配合物,已知Co3+的配位数是6,为确定钴的配合物的结构,现对两种配合物进行如下实验:
在第一种配合物溶液中加硝酸银溶液产生白色沉淀.
在第二种配合物溶液中加入硝酸银溶液产生淡黄色沉淀,则第二种配合物的配体为
(4)离子化合物CaC2的一种晶体结构如图。从钙离子看,属于
(5)科学研究结果表明.碳的氧化物CO2能够与H2O借助于太阳能制备HCOOH。其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中σ键和π键的个数比是
(6)奥氏体是碳溶解在γ—Fe中形成的一种间隙固溶体,无磁性,其晶胞如右图所示,则该物质的化学式为
您最近一年使用:0次
名校
解题方法
2 . 短周期元素Q、R、T、W在周期表中的位置如图所示,其中,T所处周期序数与主族序数相等,则下列说法正确的是

| A.元素R的最高价氧化物对应的水化物是高沸点酸 |
| B.元素T和W各自形成的简单离子都能促进水的电离 |
| C.简单离子半径:W>T>R |
| D.常温下,T的单质能完全溶于R的最高价氧化物的水化物的浓溶液中 |
您最近一年使用:0次
2017-05-27更新
|
538次组卷
|
2卷引用:宁夏石嘴山市第三中学2017届高三下学期第四次模拟考试理综化学试题
3 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W的原子核外只有6个电子,X+和Y3+的电子层结构相同,Z-的电子数比Y3+多8个,下列叙述正确的是
| A.W在自然界只有一种核素 | B.半径大小:X+>Y3+>Z- |
| C.Y与Z形成的化合物的水溶液呈弱酸性 | D.X的最高价氧化物对应的水化物为弱碱 |
您最近一年使用:0次
2017-05-25更新
|
1002次组卷
|
4卷引用:福建省宁德市2017届高三毕业班第三次质量检查化学试题
名校
4 . X、Y、Z、M、W、N六种元素的原子序数依次增大,其中X、Y、Z、M、W为五种短周期元素。X元素的某种核素无中子,W原子核外电子数是M原子最外层电子数的2倍,Y、Z、M、W在周期表中的相对位置如图所示,N是用量最多的金属元素。下列说法不正确 的是
| Y | Z | M | ||
| W |
| A.原子半径:W>Y>Z>M>X |
| B.N的一种氧化物可用作油漆和涂料 |
| C.氢化物的沸点:Z小于M |
| D.工业上制备W单质的方法为电解熔融的W的氧化物 |
您最近一年使用:0次
2017-05-25更新
|
1560次组卷
|
4卷引用:辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题
辽宁省鞍山市第一中学2017届高三下学期最后一次模拟考试理科综合化学试题【全国百强校】云南省曲靖市第一中学2018-2019学年高一下学期期中考试化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题(已下线)专题16 元素周期律和元素周期表(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练
名校
5 . 中学常见的短周期主族元素R、X、Y、Z、M的原子序数依次增大,它们占据三个周期。Y和M位于同主族,Y原子最外层电子数是电子层数的3倍。这五种元素组成一种离子化合物Q。取一定量Q溶于蒸馏水得到溶液,向溶液中滴加稀氢氧化钠溶液,产生沉淀与氢氧化钠溶液体积如图所示。下列说法不正确的是
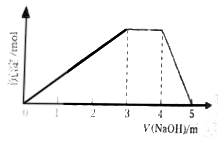
| A.简单的离子半径:M>Y>Z |
| B.气态氢化物的热稳定性:Y>X |
| C.由R、X、Y、M四种元素只组成一种盐 |
| D.最高价氧化物对应水化物的酸性:M>Z |
您最近一年使用:0次
2017-05-25更新
|
607次组卷
|
3卷引用:广东省汕头市2017届高三第三次模拟考试理科综合化学试题
名校
6 . 2017年1月26日,美国《科学》杂志刊发论文称发现了一种新材料——金属氢,证实了一百多年前提出的存在金属氢的假说。下列事实不能说明氢可能具有金属性的是
| A.可以把H写入金属活动性顺序表 | B.H与Na、K等碱金属元素同属于第IA族 |
| C.H存在H- | D.H与非金属反应,产物中H通常显正价 |
您最近一年使用:0次
2017-05-24更新
|
626次组卷
|
2卷引用:河北省石家庄市第二中学2017届高三5月联考理科综合化学试题
7 . 短周期主族元素X、Y、Z、W、M的原子序数依次增大,其中X与其它元素均不位于同一主族,Y和W的原子序数相差8,Y、Z、W三种原子的最外层电子数之和为16,X、Z的最高正价和最低负价的代数和均为0。下列说法正确的是
| A.M的氢化物的水溶液能与W的钠盐溶液,反应得到W的氢化物,说明非金属性M>W |
| B.X和Y形成的原子个数比为1∶1的分子中极性键和非极性键个数之比为2∶1 |
| C.Z元素在自然界中存在游离态 |
| D.原子半径的大小顺序:r(W)>r(Z)>r(Y) |
您最近一年使用:0次
名校
8 . 短周期主族元素X、Y、Z、W的原子序数依次增大。X、W在同一主族,Z+与Y3-具有相同的电子层结构,X原子的最外层电子数是其内层电子数的2倍。下列说法正确的是
| A.粒子半径的大小顺序:r(W)>r(X)> r(Z+)> r(Y3-) |
| B.X的最高价氧化物对应水化物的酸性比Y的强 |
| C.W的气态简单氢化物的热稳定性比X的强 |
| D.工业上可用X的单质与W的氧化物反应制备W的单质 |
您最近一年使用:0次
解题方法
9 . 原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期。自然界存在多种A的化合物,B原子核外电子由6种不同的运动状态,B与C可形成正四面体形分子,D的M能层没有空轨道且只有2个未成对电子。请回答下列问题:
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为________ 。
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有________ 个六元环;图2位在元素周期表中与B相邻的元素位置关系,B、G形成的晶胞结构如图3所示(其中“●”为B元素原子,“〇”为G元素原子),图中“●”点构成的堆积方式与图4中_____ (填序号)所表示的堆积方式相同;图3的结构中,设晶胞边长为a cm,B原子直径为bcm,G原子直径为c cm,则该晶胞的空间利用率为_______ (用含a、b、c的式子表示)。

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式_____ (用化学式表示)。
(4)元素C的含氧酸中,酸性最强的是_________ (写化学式),该酸根离子的立体构型为________ 。
(5)基态D原子的核外电子排布式为[Ar]_______ ;D形成的配合物D(CO)n的中心原子价电子数与配体提供电子总数之和为18,则n=______ ;由D一铝合金为原料可制得一种历史悠久、应用广泛的催化剂,其催化的i实例为: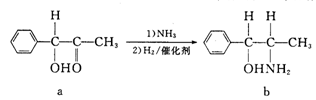 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有__________ (填元素符号)。
(1)A与B元素形成的B2A2种含有的σ键、π键数目之比为
(2)B元素的一种单质晶体结构如图1所示,理论上12g该晶体中有

(3)请说出E的氟化物(EF3)和F的氢化物(FH3)能发生反应的原因,并写出反应的化学方程式
(4)元素C的含氧酸中,酸性最强的是
(5)基态D原子的核外电子排布式为[Ar]
 化合物b中进行sp3杂化的原子有
化合物b中进行sp3杂化的原子有
您最近一年使用:0次
名校
10 . 短周期元素X、Y、Z、W、Q的原子序数依次增大,X与Q同主族,X的最外层电子数是次外层电子数的2倍,W的最外层电子数等于其电子层数,Y与Z的核外电子数之和等于X与Q的核外电子数之和,下列说法正确的是
| A.Z、W、Q、X、Y原子半径依次减小 |
| B.W最高价氧化物对应水化物一定能溶于Z最高价氧化物对应水化物的溶液中 |
| C.Y与Q形成化合物在常温下一定为气态 |
| D.Z、Q元素的单质都可以将X元素的单质从其氧化物中置换出来 |
您最近一年使用:0次
2017-05-07更新
|
1270次组卷
|
5卷引用:黑龙江省哈尔滨师范大学附属中学2017届高三第三次模拟考试化学试题



