名校
解题方法
1 . 填空题
(一)某同学欲验证 与
与 的金属性强弱,设计实验如下:
的金属性强弱,设计实验如下:
依据上述实验设计,回答下列问题:
(1)铝元素在周期表中的位置为第______ 周期______ 族;
(2)上述实验试管 中的实验现象为
中的实验现象为_________________________ ;
(3)写出试管 中白色沉淀溶解的离子反应方程式
中白色沉淀溶解的离子反应方程式______________________ ;
(4)上述实验现象证明碱性:
______  (填“>”“<”或“=”)
(填“>”“<”或“=”)
(二)某同学欲验证 、
、 、
、 的氧化性强弱,实验操作如下:
的氧化性强弱,实验操作如下:
Ⅰ.向盛有 和
和 混合液的试管
混合液的试管 中通入少量氯气,振荡观察;
中通入少量氯气,振荡观察;
Ⅱ.向盛有淀粉 混合液的试管
混合液的试管 中加入少量
中加入少量 溶液,振荡观察;
溶液,振荡观察;
(5) 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为____________
(6)试管 中通入少量氯气后的实验现象是
中通入少量氯气后的实验现象是______________________________
(7)写出试管 中发生的离子反应
中发生的离子反应______________________________
(一)某同学欲验证
 与
与 的金属性强弱,设计实验如下:
的金属性强弱,设计实验如下:实验操作 | 实验现象 | 反应或结论 |
Ⅰ.向试管 | ① |
|
Ⅱ.向试管 | 试管中先出现白色沉淀,后白色沉淀溶解 | ② |
(1)铝元素在周期表中的位置为第
(2)上述实验试管
 中的实验现象为
中的实验现象为(3)写出试管
 中白色沉淀溶解的离子反应方程式
中白色沉淀溶解的离子反应方程式(4)上述实验现象证明碱性:

 (填“>”“<”或“=”)
(填“>”“<”或“=”) (二)某同学欲验证
 、
、 、
、 的氧化性强弱,实验操作如下:
的氧化性强弱,实验操作如下:Ⅰ.向盛有
 和
和 混合液的试管
混合液的试管 中通入少量氯气,振荡观察;
中通入少量氯气,振荡观察;Ⅱ.向盛有淀粉
 混合液的试管
混合液的试管 中加入少量
中加入少量 溶液,振荡观察;
溶液,振荡观察;(5)
 、
、 、
、 的氧化性由强到弱的顺序为
的氧化性由强到弱的顺序为(6)试管
 中通入少量氯气后的实验现象是
中通入少量氯气后的实验现象是(7)写出试管
 中发生的离子反应
中发生的离子反应
您最近一年使用:0次
名校
2 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系,下图是元素周期表的一部分,回答下列问题:
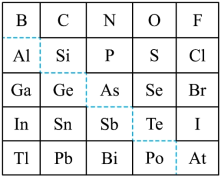
(1)元素Ga在元素周期表中的位置为:______ ;
(2)Sn的最高正价为______ ,C1的最高价氧化物对应水化物的化学式为______ ;
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是______ (写化学式),其电子式为______ 。
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4______ H2SeO4(填“>”、<”、“=”或“无法比较”);
③氢化物的还原性:H2O______ H2S(填“>”、“<”、“=”或“无法比较”)。
④原子半径比较:N______ Si(填“>”、“<”、“=”或“无法比较”)。

(1)元素Ga在元素周期表中的位置为:
(2)Sn的最高正价为
(3)根据元素周期律,推断
①表中元素形成的氢化物中热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱为:H3AsO4
③氢化物的还原性:H2O
④原子半径比较:N
您最近一年使用:0次
名校
3 . 据报道,我国首次将星载铷(Rb)钟应用于海洋二号卫星,已知Rb的原子序数为37。回答下列有关问题:
(1)Rb的原子结构示意图中共有______ 个电子层,最外层电子数为______ 。
(2)Rb在元素周期表中的位置是______ 。
(3)取少量铷单质加入水中,可观察到其剧烈反应,涉及反应的离子方程式为____________ 。
(1)Rb的原子结构示意图中共有
(2)Rb在元素周期表中的位置是
(3)取少量铷单质加入水中,可观察到其剧烈反应,涉及反应的离子方程式为
您最近一年使用:0次
23-24高二下·全国·课后作业
4 . 1869年俄国科学家门捷列夫绘制出了第一张元素周期表,成为化学史上的里程碑之一,且大大地促进了化学学科的快速发展。下表是现代元素周期表的一部分,请据表回答下列问题:
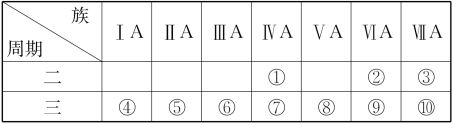
(1)元素③的名称是___________ ,金属性最强的元素是___________ (填元素符号)。
(2)①②⑤三种元素原子半径由大到小的顺序为___________ (填序号)。
(3)元素⑦的单质的一种用途是___________ (填写“制造玻璃”或“制造计算机芯片”)。
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是___________ (填化学式)。

(1)元素③的名称是
(2)①②⑤三种元素原子半径由大到小的顺序为
(3)元素⑦的单质的一种用途是
(4)元素⑧⑨⑩最高价氧化物的水化物中酸性最强的是
您最近一年使用:0次
名校
5 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的元素周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位、构。性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
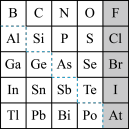
(1) 的结构示意图是
的结构示意图是___________ 。
(2)元素In在元素周期表中的位置是___________ 。
(3)P的最高价氧化物的化学式为___________ ,Al元素的最高价氧化物对应的水化物与S元素的最高价氧化物对应的水化物发生反应的离子方程式是___________ 。
(4) 的中子数与电子数的差值是
的中子数与电子数的差值是___________ ;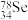 和
和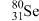 的物理性质
的物理性质___________ (填“相同”或“不同”),化学性质___________ (填“相同”或“不同”)。
(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是___________ 。
A.
B.
C.
②氢化物的还原性:
___________  (填“>”或“<”)。
(填“>”或“<”)。

(1)
 的结构示意图是
的结构示意图是(2)元素In在元素周期表中的位置是
(3)P的最高价氧化物的化学式为
(4)
 的中子数与电子数的差值是
的中子数与电子数的差值是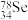 和
和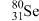 的物理性质
的物理性质(5)根据元素周期律及事实推断:
①在溶液中下列反应能发生的是
A.

B.

C.

②氢化物的还原性:

 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次
名校
6 . 结合下图所示元素周期表,回答下列问题:___________ (填字母,下同);属于主族元素的有___________ 。
(2)f元素位于第___________ 周期第___________ 族。g元素位于第___________ 周期第___________ 族,i元素位于第___________ 周期第___________ 族。
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应。请写出反应的离子方程式:___________ 、___________ 、___________ 。

(2)f元素位于第
(3)b、c、e三种元素最高价氧化物的水化物两两之间能发生反应。请写出反应的离子方程式:
您最近一年使用:0次
7 . 核外电子排布与元素周期系的基本结构
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有_______ 种元素。其余各周期总是从ns能级开始,以np结束,而从ns能级开始以np结束递增的核电荷数(或电子数)就_______ 每个周期里的元素数。
②周期、能级组、元素种类的对应关系
①根据构造原理得出的核外电子排布可以解释元素周期系中每个周期的元素数。第一周期从1s1开始,以1s2结束,只有
②周期、能级组、元素种类的对应关系
| 周期 | 对应能级组 | 对应能级组最多所能容纳的电子数 | 周期中所含元素种类 |
| 1 | 1s | 2 | 2 |
| 2 | 8 | ||
| 3 | 3s、3p | 8 | 8 |
| 4 | 18 | ||
| 5 | 5s、4d、5p | 18 | 18 |
| 6 | 32 | ||
| 7 | 7s、5f、6d、7p | 32 | 32 |
您最近一年使用:0次
8 . 元素在周期表中的位置与元素原子的结构、性质间的关系
(1)在元素周期表中,同族元素价层电子数_______ ,是同族元素性质_______ 的结构基础。
(2)长周期比短周期多出的元素,其原子的最外层电子数_______ 2(Pd除外),所以它们全部是_______ 。
(1)在元素周期表中,同族元素价层电子数
(2)长周期比短周期多出的元素,其原子的最外层电子数
您最近一年使用:0次
9 . 核外电子排布与元素周期表的分区
按电子排布式中最后填入电子的_______ 可将元素周期表分为s、p、d、f4个区,而IB、IIB族这2个纵行的元素的核外电子可理解为先填满了_______ 能级而后再填充_______ 能级而得名ds区。5个区的位置关系如下图所示:
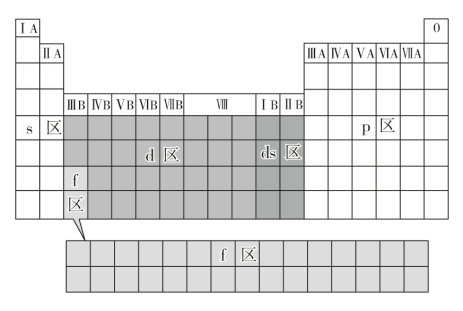
按电子排布式中最后填入电子的

您最近一年使用:0次

 溶液,再逐滴滴入
溶液,再逐滴滴入 溶液至过量,边滴边振荡
溶液至过量,边滴边振荡 溶液,再逐滴滴入
溶液,再逐滴滴入

