1 . 科技创新是引领发展的第一动力。下列说法错误的是
| A.我国“问天”实验舱采用了砷化镓太阳能电池,砷化镓所含的元素都位于p区 |
| B.绚烂焰火的产生是电子由基态跃迁到激发态时,能量以光的形式释放引起的 |
| C.我国发现了月球新矿物——“嫦娥石”,可以采用X射线衍射法分析其晶体结构 |
| D.C919飞机采用了碳纤维和玻璃纤维,二者均属于无机非金属材料 |
您最近一年使用:0次
2 . 元素周期表揭示了元素间的内在联系和规律性,下列说法正确的是
| A.某短周期元素的原子最外层只有一个电子,则该元素一定是碱金属元素 |
| B.元素周期表中有7个横行,共七个周期;18个纵列,共18个族 |
| C.在元素周期表中包含元素种类最多的是第IIIB族 |
| D.卤素单质及碱金属单质的熔沸点均随着原子序数的递增而升高 |
您最近一年使用:0次
名校
3 . 下列说法中错误的是
| A.元素周期表中有7个横行,18个纵列 |
| B.稀有气体元素原子的最外层电子数均为8 |
| C.氢是原子半径最小的元素 |
| D.氧元素位于第2周期ⅥA族 |
您最近一年使用:0次
名校
解题方法
4 . 如表是同周期三种主族元素X、Y、Z的电离能数据(单位:kJ•mol-1)。下列判断错误的是
| 元素代号 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 578 | 1817 | 2745 | 11575 |
| Z | 738 | 1451 | 7733 | 10540 |
| A.X为第IA族元素 |
B.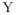 的价电子排布式为ns 2np 1 的价电子排布式为ns 2np 1 |
| C.Z位于元素周期表s区 |
| D.金属性:X>Y>Z |
您最近一年使用:0次
2023-10-24更新
|
542次组卷
|
7卷引用:陕西省西安市陕西师范大学附属中学渭北中学2022-2023学年高二下学期5月月考化学试题
5 . 某短周期元素的最外层电子数与 层电子数相等,关于该元素的说法错误的是
层电子数相等,关于该元素的说法错误的是
 层电子数相等,关于该元素的说法错误的是
层电子数相等,关于该元素的说法错误的是| A.可能是第ⅠA族元素 | B.可能是金属元素 |
C.最高化合价可能为 价 价 | D.符合该条件的元素有3种 |
您最近一年使用:0次
名校
6 . 元素周期表和周期律体现了对元素的科学分类方法,以及结构决定性质的化学观念,下列说法正确的是
| A.门捷列夫编制的第一张元素周期表是按原子序数递增的顺序编排的 |
| B.在金属与非金属分界线附近可以寻找优良催化剂和耐高温的合金材料 |
| C.某元素的原子最外层只有一个电子,它跟卤素原子结合时,所形成的化学键一定是离子键 |
| D.化学键是相邻离子或原子间的一种强作用力,既包括静电吸引力,又包括静电排斥力 |
您最近一年使用:0次
7 . 元素周期表从左到右共18列,第1列为碱金属元素(氢元素除外),第18列为稀有气体元素,则下列说法正确的是
| A.第11、12列为d区元素 |
| B.第15列元素原子的最外层电子排布式是ns2np5 |
| C.最外层电子排布式为ns1的元素一定在主族 |
| D.第9列元素中没有非金属元素 |
您最近一年使用:0次
8 . C、N、O、F等元素的化合物在航天、美容、食品等多领域中有广泛的用途,请回答:
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为______ ;N、O、F的第一电离能由大到小的顺序为_____ (用元素符号表示)。
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为______ 晶体(填晶体类型)。
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第______ 周期第______ 族。
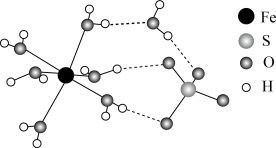
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO 的作用类型分别是
的作用类型分别是______ 、______ 。
A.离子键 B.配位键 C.氢键 D.金属键 中键角的大小并解释原因:
中键角的大小并解释原因:______ 。
(1)OF2主要用于火箭工程液体助燃剂,该分子的空间结构为
(2)XeF2是一种选择性很好的氟化试剂,但在室温下易升华,推测XeF2为
(3)FeSO4是一种重要的食品和饲料添加剂:
①Fe在周期表中位于第
②FeSO4·7H2O的结构示意图如图所示,H2O与Fe2+、SO
 的作用类型分别是
的作用类型分别是A.离子键 B.配位键 C.氢键 D.金属键
 中键角的大小并解释原因:
中键角的大小并解释原因:
您最近一年使用:0次
2023-04-20更新
|
187次组卷
|
2卷引用:陕西省西安市2023-2024学年高二下学期4月期中联考化学试题
解题方法
9 . 下列关于元素周期表和元素周期律的说法正确的是
| A.透明陶瓷材料硒化锌是由主族元素和副族元素形成的化合物 |
| B.元素的性质随着相对原子质量的增加而呈周期性变化 |
| C.同一主族元素的原子,最外层电子数相同,化学性质也完全相同 |
| D.第二周期元素从Li到F,非金属性逐渐减弱 |
您最近一年使用:0次
解题方法
10 . 如图是元素周期表的一部分,回答下列问题:
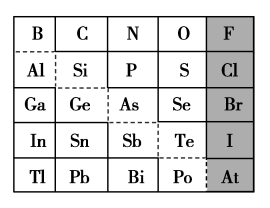
(1)元素Ga在元素周期表中的位置为:第_______ 周期第_______ 族。
(2)Sn的最高正价为_______ ,Cl的最高价氧化物对应的水化物的化学式为_______ ,Bi的最高价氧化物的化学式为_______ 。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是_______ (填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4_______ H2SeO4(填“>”或“<”下同)。
③氢化物的还原性:H2O_______ H2S。

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次



