1 . X、Y、Z、M为前两周期元素,是构成生命体的基本元素,其原子序数依次增大,下列说法正确的是
| A.四种元素中离子半径最大的为M |
| B.四种元素最多可形成两种盐 |
| C.Y、Z、M的氢化物中,M的氢化物沸点最高 |
| D.由四种元素中的两种形成的相对分子质量最小的有机物,不能发生加成反应 |
您最近一年使用:0次
名校
2 . 短周期主族元素W、X、Y、Z原子序数依次增大,其中只有X、Y处于同一周期,且相邻;Y是地壳中含量最多的元素;Z是短周期中金属性最强的元素。下列说法正确的是( )
| A.离子半径:r(Z)<r(X)<r(Y) |
| B.X的单质的氧化性比Y的强 |
| C.化合物Z2Y2中阴、阳离子个数比为1∶1 |
| D.W、X、Y三种元素可以组成共价化合物和离子化合物 |
您最近一年使用:0次
2020-06-15更新
|
421次组卷
|
4卷引用:天津市河北区2020届高三总复习质量检测(二)化学试题
天津市河北区2020届高三总复习质量检测(二)化学试题江西省临川一中暨临川一中实验学校2020-2021学年高二上学期期中考试化学试题吉林省榆树市第一高级中学2021届高三上学期第三次模拟考试化学试题(已下线)专题04 物质结构与元素周期律—2022年高考化学二轮复习讲练测(全国版)-练习
名校
解题方法
3 . 下列叙述能说明X的非金属性比Y强的是
| A.X的气态氢化物比Y的气态氢化物稳定 |
| B.X原子的电子层数比Y原子的电子层数多 |
| C.Y的单质能将X从NaX的溶液中置换出来 |
| D.Y在暗处可与H2反应,X在加热条件下才能与H2反应 |
您最近一年使用:0次
2020-04-16更新
|
346次组卷
|
6卷引用:天津市河北区2021-2022学年高一上学期期末质量检测化学试题
4 . I.A〜G七种元素中,除F外其他均为短周期主族元素,它们的原子结构或性质如下表所示:
请回答下列问题:
(1)A在元素周期表中的位置是_______ ;F的原子结构示意图是_____________ 。
(2)下列事实能证明C和E的非金属性强弱的是_____ 。(填序号)
①常温下,C的单质呈气态,E的单质呈固态②C的气态氢化物的温定性强于E的气态氢化物的温定性③C与E形成的化合物中,E呈正价④E的氢化物的沸点高于于C的氢化物的沸点
(3)由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是______ (填化学式),它与足量NaOH溶液在加热时反应的离子方程式为:_______ 。
(4)A的氢化物有多种,1 molA的某种氢化物分子中含有14mol电子,请写出该氢化物的电子式:______ 。已知在25℃、101kPa下,1g该氢化物在足量氧气中完全燃烧生成液态水时放出的热量为40kJ,写出该氢化物燃烧热:_________ 。
Ⅱ.甲、乙、丙,丁均为上述元素所形成的物质,甲是单质。它们之间有如下的反应关系:
(5)若乙为淡黄色固体,②③反应均用到同一种液态氢化物,丁物质常用于食品工业。乙所含化学键的类型是________ 。写出乙→丙的化学方程式:__________ 。
(6)若丁物成质具有两性,②③反应均要用强碱溶液,④反应是通入过量的—种引起温室效应的主要气体。写出丙→丁的离子方程式:__________ 。室温下,若由丁物质形成的水溶液中甲离子浓度为1.3×10-6mol·L-1,则该溶液的pH为______ 。
(丁的Ksp为1.3×10-33)
| 元素 | 原子结构或性质 |
| A | 其形成的一种同位素原子在考古中可推测化石的年代 |
| B | 与A同周期,其最高价氧化物的水化物无论浓、稀溶液均有强氧化性 |
| C | 地壳中含量最多的元素 |
| D | D原子的最外层电子数与其电子层数相同,是地壳中含量多的金属元素 |
| E | 其单质主要存在于火山口附近 |
| F | 生活中常见的金属,它的某种氧化物具有磁性 |
| G | G原子与D原子同周期,且原子半径是同周期元素中最大的 |
(1)A在元素周期表中的位置是
(2)下列事实能证明C和E的非金属性强弱的是
①常温下,C的单质呈气态,E的单质呈固态②C的气态氢化物的温定性强于E的气态氢化物的温定性③C与E形成的化合物中,E呈正价④E的氢化物的沸点高于于C的氢化物的沸点
(3)由A、B、C和氢元素四种元素所形成的阴、阳离子数目之比为1:1的离子化合物是
(4)A的氢化物有多种,1 molA的某种氢化物分子中含有14mol电子,请写出该氢化物的电子式:
Ⅱ.甲、乙、丙,丁均为上述元素所形成的物质,甲是单质。它们之间有如下的反应关系:
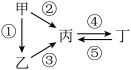
(5)若乙为淡黄色固体,②③反应均用到同一种液态氢化物,丁物质常用于食品工业。乙所含化学键的类型是
(6)若丁物成质具有两性,②③反应均要用强碱溶液,④反应是通入过量的—种引起温室效应的主要气体。写出丙→丁的离子方程式:
(丁的Ksp为1.3×10-33)
您最近一年使用:0次
解题方法
5 . A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中B与C同周期,D与E和F同周期,A与D同主族,C与F同主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的主族元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题。
(1)元素D在周期表中的位置________ 。
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)____ 。
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有________ 。用电子式表示当C、D按1:1所组成化合物的形成过程________ 。
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:________________________________________________________________________ 。
(5)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:_______________________________________________________ 。
(1)元素D在周期表中的位置
(2)C、D、F三种元素形成的简单离子的半径由大到小的顺序是(用离子符号表示)
(3)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有
(4)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:
(5)若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:
您最近一年使用:0次



