1 . 回答下列问题:
(1)氟原子激发态的电子排布式有______ ,其中能量较高的是______ 。(填标号)
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的______ 区,写出该基态原子电子排布式为______ 。
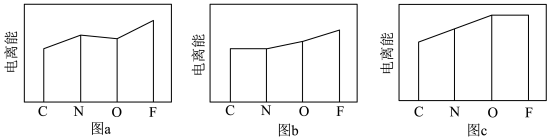
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是______ (填标号),判断的根据是______ ;第三电离能的变化图是______ (填标号)。
(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
①元素的电负性:Z______ W(填“大于”“小于”或“等于”)。
②简单离子半径:W______ Y(填“大于”“小于”或“等于”)。
③氢化物的稳定性:X______ Z(填“大于”“小于”或“等于”)。
(1)氟原子激发态的电子排布式有
a.1s22s22p43s1 b.1s22s22p43d2 c.1s22s12p5 d.1s22s22p33p2
(2)某元素原子的位于周期表的第四周期,元素原子的最外层只有一个电子,其次外层内的所以轨道电子均成对。该元素位于周期表的
(3)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(4)短周期元素X、Y、Z、W的原子序数依次增大。根据表中信息完成下列空白。
| 元素 | X | Y | Z | W |
| 最高价氧化物的水化物 | H3ZO4 | |||
| 0.1 mol∙L−1溶液对应的pH(25℃) | 1.00 | 13.00 | 1.57 | 0.70 |
②简单离子半径:W
③氢化物的稳定性:X
您最近一年使用:0次
2023-01-03更新
|
426次组卷
|
2卷引用:天津市和平区2022-2023学年高二上学期期末质量调查化学试卷
名校
2 . 短周期主族元素 、
、 、
、 、
、 原子序数依次增大,
原子序数依次增大, 元素的单质在自然界存在硬度很大的矿石,
元素的单质在自然界存在硬度很大的矿石, 原子最外层有
原子最外层有 个电子,
个电子, 元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质,
元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质, 与
与 同主族。下列叙述正确的是
同主族。下列叙述正确的是
 、
、 、
、 、
、 原子序数依次增大,
原子序数依次增大, 元素的单质在自然界存在硬度很大的矿石,
元素的单质在自然界存在硬度很大的矿石, 原子最外层有
原子最外层有 个电子,
个电子, 元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质,
元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质, 与
与 同主族。下列叙述正确的是
同主族。下列叙述正确的是A.原子最外层电子数由少到多的顺序: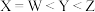 |
B.原子半径由大到小的顺序: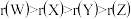 |
C.元素电负性由强到弱的顺序: |
D.元素的最简单气态氢化物的稳定性由强到弱的顺序: 、 、 、 、 |
您最近一年使用:0次
2022-03-10更新
|
225次组卷
|
2卷引用:天津市耀华中学2022届高三第二次模拟考化学试题
名校
3 . (一)如图是部分短周期主族元素的原子序数与其最高或最低化合价的关系图(用原子序数代表所对应的元素),已知a为元素周期表中相对原子质量最小的元素,请回答下列问题:
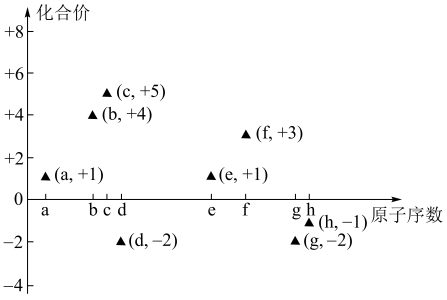
(1)a与c、d分别都可以形成有18个电子的分子甲和乙,甲分子的电子式_____ ,乙分子类型属于____ 分子(填“极性”或“非极性”)。
(2)b元素的一种单质丙可与g元素的最高价含氧酸丁的溶液反应,该反应的化学方程式为_____ ,如果一次性取样分别检验上述反应的生成物,按照最简单的操作顺序写出所用试剂的名称_____ 。
(3)f元素的单质可与e元素的最高价氧化物对应水化物反应放出氢气,该反应的化学方程式为_____ ,f元素的两种盐溶液也可以反应得到f元素最高价氧化物对应的水化物,该反应的离子方程式为_____ 。
(二)过渡金属在社会生产、生活发展中具有重要作用。
(4)原子序数21~30的元素中,基态电子排布未成对电子最多的元素在周期表的位置_____ ,其价电子排布图为____ 。
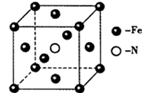
(5)铁单质和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,该反应的化学方程式为______ 。若该晶体的密度是ρg•cm-3,则两个最近的Fe原子间的距离为_____ cm。(用NA表示阿伏加德罗常数的值)
(6)铁的一种配合物的化学式为Fe[(Htrz)3](ClO4)2,其中Htrz为1,2,4—三氮唑()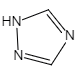 。
。
①配合物中阴离子的空间构型为_____ ,中心原子的杂化方式是_____ 。
② 分子中含σ键与π键个数比为
分子中含σ键与π键个数比为______ 。
③1摩尔1,2,4—三氮唑最多能与_____ molH+结合。
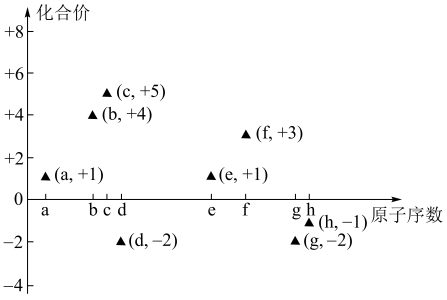
(1)a与c、d分别都可以形成有18个电子的分子甲和乙,甲分子的电子式
(2)b元素的一种单质丙可与g元素的最高价含氧酸丁的溶液反应,该反应的化学方程式为
(3)f元素的单质可与e元素的最高价氧化物对应水化物反应放出氢气,该反应的化学方程式为
(二)过渡金属在社会生产、生活发展中具有重要作用。
(4)原子序数21~30的元素中,基态电子排布未成对电子最多的元素在周期表的位置
(5)铁单质和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,该反应的化学方程式为

(6)铁的一种配合物的化学式为Fe[(Htrz)3](ClO4)2,其中Htrz为1,2,4—三氮唑()
 。
。①配合物中阴离子的空间构型为
②
 分子中含σ键与π键个数比为
分子中含σ键与π键个数比为③1摩尔1,2,4—三氮唑最多能与
您最近一年使用:0次
2022-01-13更新
|
163次组卷
|
2卷引用:天津市耀华中学2021-2022学年高三上学期第二次月考化学试题
名校
4 . 一种高效电解质的结构如图所示,W、Y、X、Z、Q均为短周期元素,且原子序数依次增大,X与Q同族,Y和Z的原子序数之和与Q相等。下列说法正确的是

| A.原子半径的顺序为Q>Y>X>Z>W |
| B.简单氢化物沸点的顺序为Q>Z>X |
| C.阴离子中所有原子均满足8电子稳定结构 |
| D.化合物QX2、YX2均能与NaOH溶液反应 |
您最近一年使用:0次
2021-10-24更新
|
647次组卷
|
8卷引用:天津市耀华中学2021-2022学年高三上学期第二次月考化学试题
5 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W的简单氢化物可用作制冷剂,Y的原子半径是所有短周期主族元素中最大的。由X、Y和Z三种元素形成的一种盐溶于水后,加入稀盐酸,有黄色沉淀析出,同时有刺激性气体产生。下列说法不正确的是
| A.X的简单氢化物的热稳定性比W的强 |
| B.Y与X的简单离子具有相同的电子层结构 |
| C.Y与Z形成的化合物的水溶液可使蓝色石蕊试纸变红 |
| D.Z与X属于同一主族,与Y属于同一周期 |
您最近一年使用:0次
2021-07-28更新
|
4303次组卷
|
73卷引用:【全国区级联考】天津市和平区2018届高三下学期第二次质量调查化学试题
【全国区级联考】天津市和平区2018届高三下学期第二次质量调查化学试题山西省康杰中学2016-2017学年高二下学期期末考试化学试题河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题河北省安平中学2016-2017学年高二下学期期末考试化学试题2017年全国普通高等学校招生统一考试理综化学(新课标Ⅰ卷精编版)山东省淄博市淄川中学2018届高三上学期开学考试化学试题广西灵山县第二中学2018届高三上学期开学考试化学试题陕西省西安中学2018届高三上学期第一次摸底考试化学试题新疆阿克苏市农一师中学2018届高三上学期第二次月考化学试题2018届广东省揭阳市高三上学期第一次月考化学试题浙江省嘉兴市第一中学2018届高三上学期期末考试化学试题浙江省嘉兴市第一中学2017-2018学年高二上学期期末考试化学试题(已下线)狂刷05 元素周期表和元素周期律的应用—《小题狂刷》2017-2018学年高一化学人教必修2重庆市第二中学2018届高三3月测试化学试题(已下线)《考前20天终极攻略》-5月19日 物质结构 元素周期律(已下线)解密07 物质结构和元素周期律(教师版)——备战2018年高考化学之高频考点解密【全国市级联考】河南省周口市2017-2018学年高二下学期期末考试化学试题河北省磁县滏滨中学2017-2018学年高二下学期期末考试化学试题山东省淄博市淄川中学2019届高三上学期10月月考化学试题河南省辉县市第一高级中学2019届高三上学期第二次月考化学试题河北省隆化县存瑞中学2019届高三上学期期中考试化学试题【全国百强校】辽宁省大连市辽宁师范大学附属中学2019届高三上学期第一次考试化学试题【市级联考】广东省化州市2019年高三上学期第二次模拟考试理科综合化学试题(已下线)2019高考备考二轮复习精品资料-专题7 物质结构与元素周期律(教学案)【全国百强校】广西河池市高级中学2018-2019学年高二下学期第一次月考理综-化学试题(已下线)考点07 元素周期律和元素周期表——备战2019年浙江新高考化学考点福建省泉州市泉港区第一中学2018-2019学年高二下学期第二次月考化学试题重庆市璧山大路中学校2018-2019学年高一下学期4月月考化学试题苏教版高二化学选修三单元测试题:2.2 元素性质的递变规律广东省北京师范大学东莞石竹附属学校2018-2019学年高一下学期期中考试化学试题(已下线)2019年6月26日《每日一题》选修3—— 元素推断技巧重庆市南岸区2018-2019学年高一下学期期末质量调研抽测化学试题百所名校联考-物质结构 元素周期律湖南省邵阳市邵东县第十中学2020届高三9月月考(读论班)化学试题(已下线)【新东方】高中化学5001广东省揭阳市第三中学2020届高三上学期第三次月考理综化学试题河北省张家口市第一中学2019-2020学年高二12月月考化学试题辽宁省滨海实验中学2019-2020学年高一上学期期末化学试题山东省烟台第二中学2019-2020学年高二上学期12月月考化学试题第1章原子结构与元素周期律 挑战区 模拟高考第1章 原子结构——C挑战区 模拟高考(鲁科版选修3)(已下线)专题八 物质结构与元素周期律(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训云南省大理白族自治州祥云县第一中学2020届高三下学期4月月考理综化学试题安徽省黄山市屯溪第一中学2019-2020学年高一下学期入学考试化学试题河北省衡水中学2020届高三四月份质量监测理综化学试题河北省衡水中学2020年高中毕业班教学质量监测卷理科综合化学试题湖南省株洲市2020年高中毕业班教学质量监测卷理科综合化学试题四川省内江市市中区天立学校2019-2020学年高一下学期第二次月考化学试题(已下线)专题5.2 元素周期律和元素周期表(讲)——2020年高考化学一轮复习讲练测(已下线)专题5.2 元素周期律和元素周期表(练)——2020年高考化学一轮复习讲练测黑龙江省哈尔滨师范大学青冈实验中学校2020届高三10月月考化学试题四川省宜宾市第四中学2019-2020学年高一下学期期末模拟考试化学试题四川省成都艺术高级中学2020-2021学年高三上学期开学考试化学试题江苏省启东中学2020-2021学年高二上学期期初考试化学试题安徽省定远县育才学校2021届高三上学期第二次月考化学试题浙江省金丽衢十二校2021届高三上学期第一次联考化学试题(已下线)练习12 原子核外电子的排布-2020-2021学年【补习教材·寒假作业】高一化学(人教版)专题5 第一单元综合拔高练-高中化学苏教2019版必修第一册(人教版2019)选择性必修2 第一章 原子结构与性质 章末总结(鲁科版2019)必修第二册 第1章 原子结构 元素周期律 学科素养提升(已下线)第一单元 原子结构(基础过关)-2020-2021学年高二化学单元测试定心卷(鲁科版选修3)(已下线)小题15 元素周期表、律(根据物质性质角度的元素推断)——备战2021年高考化学经典小题考前必刷(全国通用)(已下线)【浙江新东方】高中化学20210513-044【2021】【高二下】安徽省蚌埠第三中学2020-2021学年高一下学期5月教学质量检测化学试题江西省宜春市丰城市第九中学2020-2021学年高一下学期月考化学试题(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点07 元素周期律和元素周期表-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题讲座(三)“位-构-性”综合推断题的解题方法(练) — 2022年高考化学一轮复习讲练测(新教材新高考)黑龙江省大庆实验中学2022届高三10月月考化学试题吉林省梅河口市第五中学2022届高三上学期第一次月考化学试题黑龙江省七台河市勃利县高级中学2021-2022学年高三上学期期中考试化学试题安徽省合肥市肥东县综合高中2021-2022学年高二下学期期中考试化学试题(已下线)专题突破卷05?物质结构 元素周期律?-2024年高考化学一轮复习考点通关卷(新教材新高考)
2021高三·全国·专题练习
名校
解题方法
6 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W的一种核素没有中子,Y原子中L层电子数是K层电子数三倍。a、b、c、d均是由以上四种元素中的两种组成的二元化合物,且d是淡黄色固体;25℃时,0.1mol/Le的水溶液pH=13.上述物质的转化关系如图所示。
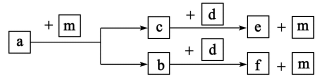
下列说法正确的是

下列说法正确的是
| A.沸点:a>c |
| B.元素的非金属性:X>W |
C.f溶液中存在c(H+)+c(HCO )+c(H2CO3)=c(OH-) )+c(H2CO3)=c(OH-) |
| D.简单阴离子的还原性:Y>W |
您最近一年使用:0次
名校
7 . 现有下列短周期元素性质的有关数据:
(1)根据元素周期律确定a至h8种元素在周期表中的位置,将它们的元素编号填入下表相应的空格内_______ 。
(2)上述元素形成的常见氢化物中,分子间存在氢键的有(填氢化物的化学式)_______ 。
(3)氢化铝锂( )是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式
)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式_______ 。写出该物质受热分解的反应方程式_______ 。
(4)在元素周期表中,相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除 外,还有
外,还有 ;碳元素的氢化物除
;碳元素的氢化物除 外,还有
外,还有 等;与之相似的氮元素的氢化物除
等;与之相似的氮元素的氢化物除 外,还有
外,还有_______ (填化学式),其沸点比液氨_______ (填“高”或“低”),稳定性比氨_______ (填“好”或“差”),该氢化物与足量盐酸反应的化学方程式为_______ 。
| 元素编号 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最底 |  |  |  |  |  |  |  |  |
(1)根据元素周期律确定a至h8种元素在周期表中的位置,将它们的元素编号填入下表相应的空格内
| Ⅰ族 | Ⅱ族 | Ⅲ族 | Ⅳ族 | Ⅴ族 | Ⅵ族 | Ⅶ族 | Ⅷ族 | |
| 第一周期 | ||||||||
| 第二周期 | ||||||||
| 第三周期 |
(2)上述元素形成的常见氢化物中,分子间存在氢键的有(填氢化物的化学式)
(3)氢化铝锂(
 )是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式
)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式(4)在元素周期表中,相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、氮、氧、氟都可以形成氢化物,氧元素的氢化物除
 外,还有
外,还有 ;碳元素的氢化物除
;碳元素的氢化物除 外,还有
外,还有 等;与之相似的氮元素的氢化物除
等;与之相似的氮元素的氢化物除 外,还有
外,还有
您最近一年使用:0次
名校
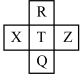
8 . 元素R、X、T、Z、Q在元素周期表中的相对位置如图所示,其中R单质在暗处与H2剧烈化合并发生爆炸,T元素的一种核素的质量数为37,则下列判断不正确的是

| A.T元素中质量数为37的这种核素含有20个中子 |
| B.R与Q的电子数相差26 |
| C.气态氢化物的稳定性:R<T<Q |
| D.T的单质通入Q的钠盐溶液中能发生置换反应 |
您最近一年使用:0次
2021-05-18更新
|
246次组卷
|
3卷引用:天津市耀华中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
9 . 已知短周期元素W、X、Y、Z的原子序数依次增大,W的阴离子的核外电子数与X、Y、Z元素原子的最内层电子数相同;X的一种核素常用来鉴定一些文物的年代;工业上采用液态空气分馏法来生产Y的单质,该单质是常见氧化剂;Z的单质为单原子分子。下列说法正确的是
| A.原子半径:W<X<Y<Z |
| B.X的电负性大于Y的电负性 |
| C.XY2分子中σ键与π键的个数之比是2:1 |
| D.W与Y形成的分子的空间构型可能是V形 |
您最近一年使用:0次
2021-04-11更新
|
330次组卷
|
3卷引用:天津市耀华中学2020-2021学年高二下学期期中检测化学试题
名校
10 . 化合物甲是一种常见无机物,其结构如图所示(图中的“-”可表示单键或双键),其中 W、X、Y、Z 为元素周期表中的短周期主族元素,且原子序数依次增大,W 和 Y、X和 Z 分别为同主族元素,这四种元素原子的最外层电子数之和为14,甲的水溶液显酸性。下列叙述不正确的是


| A.W 与 X、W 与 Z 均可形成 18 电子分子 |
| B.X、Y 形成的离子化合物中可能含共价键 |
| C.X、Y、Z 三种元素的简单离子半径大小顺序为 Z X Y |
D.甲的水溶液中 W2ZX3的浓度大于 ZX 的浓度 的浓度 |
您最近一年使用:0次



