1 . 短周期主族元素X、Y、Z、U、V、W在元素周期表中的相对位置如图所示。已知:常温常压下,W的单质为黄绿色气体。下列说法错误的是
| Y | Z | U | ||
| X | V | W |
A.简单离子半径: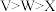 |
B.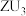 分子中所有原子均达到了8电子稳定结构 分子中所有原子均达到了8电子稳定结构 |
C.最高价氧化物对应水化物的酸性: |
| D.Z的最简单氢化物的水溶液呈酸性 |
您最近半年使用:0次
2023-07-14更新
|
48次组卷
|
2卷引用:甘肃省陇南市2022-2023学年高一下学期期末考试化学试题
解题方法
2 . 六种主族元素A、B、C、D、X、Y的原子序数依次增大,且均小于54。常温下A2B呈液态,高纯度的单质C具有良好的半导体性能。D、X、Y原子核外最外层电子数均为7,过渡元素Z与B可形成多种化合物,其中红棕色粉末Z2B3常用作外墙涂料。请完成下列空白。
(1)将D2水溶液滴入浅绿色的ZD2溶液中,发生反应的离子方程式为___ 。
①甲认为X2和Y2都可能将Z2+氧化为Z3+,他推理的依据是___ 。
②乙认为X2和Y2都不能将Z2+氧化为Z3+;丙认为X2能将Z2+氧化为Z3+而Y2不能。乙、丙推理的依据是__ 。
(2)A与B可形成既含极性键又含非极性键的化合物W。W的水溶液呈弱酸性,常用作无公害的消毒杀菌剂等。W的电子式为__ 。
(3)铅(Pb)、锡(Sn)、锗(Ge)与元素C位于同主族,原子核外电子层数均小于7;常温下,锡、锗在空气中不反应,而铅表面会生成一层氧化铅。锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为__ ;
②它们+4价氢氧化物的碱性由强到弱顺序为__ (填化学式)。
(1)将D2水溶液滴入浅绿色的ZD2溶液中,发生反应的离子方程式为
①甲认为X2和Y2都可能将Z2+氧化为Z3+,他推理的依据是
②乙认为X2和Y2都不能将Z2+氧化为Z3+;丙认为X2能将Z2+氧化为Z3+而Y2不能。乙、丙推理的依据是
(2)A与B可形成既含极性键又含非极性键的化合物W。W的水溶液呈弱酸性,常用作无公害的消毒杀菌剂等。W的电子式为
(3)铅(Pb)、锡(Sn)、锗(Ge)与元素C位于同主族,原子核外电子层数均小于7;常温下,锡、锗在空气中不反应,而铅表面会生成一层氧化铅。锗与盐酸不反应,而锡与盐酸反应。由此可得出以下结论:
①锗的原子序数为
②它们+4价氢氧化物的碱性由强到弱顺序为
您最近半年使用:0次
解题方法
3 . 现有部分短周期元素的性质或原子结构如下表:
(1)元素X的一种同位素可测定文物年代,这种同位素的符号是___ 。
(2)元素Y与氢元素形成一种离子YH ,写出该微粒的化学式:
,写出该微粒的化学式:___ (用元素符号表示).
(3)元素Z与元素T相比,非金属性较强的是___ (用元素符号表示),下列表述中能证明这一事实的是___ 。
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是___ (填化学式),理由是_____ ;Z的最高价氧化物对应的水化物与W的最高价氧化物对应的水化物反应的离子方程式为___ 。
| 元素编号 | 元素性质或原子结构 |
| T | M层上有6个电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
| W | 其单质既能跟酸反应,又能跟碱反应,都产生H2 |
(2)元素Y与氢元素形成一种离子YH
 ,写出该微粒的化学式:
,写出该微粒的化学式:(3)元素Z与元素T相比,非金属性较强的是
①常温下Z的单质和T的单质状态不同
②Z的氢化物比T的氢化物稳定
③一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种的是
您最近半年使用:0次
2020-07-02更新
|
43次组卷
|
2卷引用:甘肃省陇南市徽县二中2020-2021学年高一下学期第一次月考化学试题
解题方法
4 . 短周期主族元素 W、X、Y、Z 的原子序数依次增大,W、Y 同主族,Y的次外层电子数与W的质子数相同。X的简单离子半径是 X 所处周期中最小的,Z元素是最重要的“成盐元素” 下列说法正确的是
| A.原子半径由大到小的 顺序:Z> Y> X |
| B.Y2Z2 中含极性共价键和非极性共价链 |
| C.Z的氧化物对应的水化物一定是强酸 |
| D.氢化物沸点由高到低的顺序:W> Z> Y |
您最近半年使用:0次



