名校
1 . 短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上用Y的简单氢化物作制冷剂,W、Z同族。下列说法中正确的是
| A.Y的氢化物与的最高价氧化物对应水化物可能生成盐 |
| B.这些元素的原子半径大小顺序为Z<X<Y<W |
| C.由Y与Z组成的化合物中都只含有离子键 |
| D.Y与W只形成含极性共价键化合物 |
您最近半年使用:0次
2022-03-24更新
|
61次组卷
|
2卷引用:甘肃省临洮县第二中学2022-2023学年高二下学期第一次月考化学试题
2 . 现有下列短周期元素性质的数据,试回答下列问题:
(1)上述元素中处于ⅤA族的有:_____ (用编号表示)。
(2)处于第二周期的元素有:______ (用编号表示)。
(3)写出②、⑤的元素符号:______ 、______ 。
(4)能形成两性氢氧化物和两性氧化物的元素为______ (用编号表示)。
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.73 | 1.30 | 1.24 | 1.06 | 0.99 | 1.54 | 0.75 | 1.18 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)上述元素中处于ⅤA族的有:
(2)处于第二周期的元素有:
(3)写出②、⑤的元素符号:
(4)能形成两性氢氧化物和两性氧化物的元素为
您最近半年使用:0次
名校
3 . 短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期且相邻,Y是地壳中含量最多的元素,Z是短周期中原子半径最大的主族元素,W的单质常温下是一种淡黄色固体。下列叙述正确的是
A.元素的非金属性: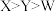 |
B.Z的单质在空气中燃烧生成阴、阳离子个数比为 的氧化物 的氧化物 |
| C.Y的简单气态氢化物的稳定性强于W的 |
| D.工业上一般采用电解对应盐的水溶液制Z单质 |
您最近半年使用:0次
2020-06-17更新
|
58次组卷
|
4卷引用:甘肃省临洮中学2021-2022学年高二下学期期中考试化学试题
解题方法
4 . 有A、B、C、D四种短周期元素,它们的原子序数由A到D依次增大,已知A和B原子有相同的电子层数,且A的L层电子数是K层电子数的两倍,C燃烧时呈现黄色火焰,C的单质在点燃条件下与B的单质充分反应,可以得到与D的单质颜色相同的淡黄色固态化合物。
试根据以上叙述回答:
(1)写出AB2的电子式:___________ ;
(2)用电子式表示C2B的形成过程:____________ 。
(3)写出C单质点燃时与B单质充分反应的化学方程式:___________ 。
(4)写出淡黄色固态化合物与水反应的化学方程式:___________ 。
(5)请设计简单实验,比较元素B、D的金属性(或非金属性)强弱:___________ 。
试根据以上叙述回答:
(1)写出AB2的电子式:
(2)用电子式表示C2B的形成过程:
(3)写出C单质点燃时与B单质充分反应的化学方程式:
(4)写出淡黄色固态化合物与水反应的化学方程式:
(5)请设计简单实验,比较元素B、D的金属性(或非金属性)强弱:
您最近半年使用:0次
解题方法
5 . 已知由短周期常见元素形成的纯净物A、B、C、D转化关系如图l所示,物质A与物质B之间的反应不在溶液中进行。
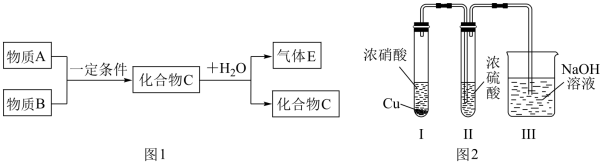
请回答下列问题:
(1)若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是__________________ ;(填化学式)
②化合物C的电子式为__________ ;化合物D中所含化学键的类型是_________ 。
(2)若A为非金属单质,B是化合物,C是红棕色气体,D是一元强酸.
①B为_________________ (填化学式)。
②化合物C与水反应时的化学方程式为________________ ,其氧化剂与还原剂的质量比为_______________ 。
(3)某同学用图2装置完成有关探究实验。
I.试管中(试管中的药品分别为浓硝酸,铜片)发生反应的离子方程式为:_________________________ 。
II.试管中观察到_______________________ 的实验现象时,说明NO2能溶于浓硫酸中,浓硫酸不能干燥NO2。Ⅲ.装置Ⅲ的用途是:____________________________

请回答下列问题:
(1)若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是
②化合物C的电子式为
(2)若A为非金属单质,B是化合物,C是红棕色气体,D是一元强酸.
①B为
②化合物C与水反应时的化学方程式为
(3)某同学用图2装置完成有关探究实验。
I.试管中(试管中的药品分别为浓硝酸,铜片)发生反应的离子方程式为:
II.试管中观察到
您最近半年使用:0次
6 . A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A元素是所有原子中半径最小的原子;B元素的最高价氧化物对应水化物与其氢化物生成一种盐X;D与A同主族,且与E同周期;E元素的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素中,每一种都能与C元素形成原子个数比不相同的化合物。
请回答下列问题:
(1)A、C两元素形成的原子个数比为1:1的化合物,该化合物电子式为_______________ 。
(2)B元素的氢化物在催化剂存在的情况下与C元素单质反应的化学方程式为__________ 。
(3)X的水溶液显__________ (填酸性、碱性或中性),原因是__________ (用离子方程式表示)。
(4)C和E两元素相比较,非金属性较强的是____________ (填“元素名称”),可以验证该结论的是________ (填“序号”)。
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的单质在常温下的状态
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(5)C、D两元素形成的原子个数比为1:1的化合物,E、C两元素形成的原子个数比为1:2的化合物,这两种化合物反应的化学方程式为_______________ 。
(6)A与C、A与E可分别形成甲、乙两种负一价双原子离子,且甲有10个电子,乙有18个电子,则甲与乙反应的离子方程式为____________________ 。
请回答下列问题:
(1)A、C两元素形成的原子个数比为1:1的化合物,该化合物电子式为
(2)B元素的氢化物在催化剂存在的情况下与C元素单质反应的化学方程式为
(3)X的水溶液显
(4)C和E两元素相比较,非金属性较强的是
A.比较这两种元素的气态氢化物的沸点
B.比较这两种元素的单质在常温下的状态
C.比较这两种元素的气态氢化物的稳定性
D.比较这两种元素的单质与氢气化合的难易
(5)C、D两元素形成的原子个数比为1:1的化合物,E、C两元素形成的原子个数比为1:2的化合物,这两种化合物反应的化学方程式为
(6)A与C、A与E可分别形成甲、乙两种负一价双原子离子,且甲有10个电子,乙有18个电子,则甲与乙反应的离子方程式为
您最近半年使用:0次



