2021高三·全国·专题练习
1 . 常温下,W、X、Y、Z四种短周期元素的最高价氧化物对应的水化物溶液(浓度均为0.01mol·L-1)的pH和原子半径、原子序数的关系如图所示。下列说法错误的是
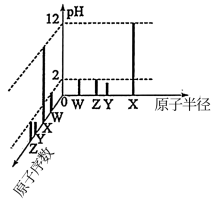

| A.非金属性:Z>W>Y>X |
| B.简单离子的半径:Y>Z>W>X |
| C.W的氢化物空间构型不一定是三角锥形 |
| D.Z的单质具有强氧化性和漂白性 |
您最近一年使用:0次
名校
2 . A、B、C、D、E、 F、G、H是周期表中前四周期的七种元素,有关性质或结构信息如下表:
(1) B元素符号为________ ,A与C以原子个数比为1:1形成的化合物的电子式为_______ ,用电子式表示C与E形成化合物的过程________ 。
(2) A、C、E所形成简单离子半径由大到小的顺序是____________ ,H的最高价氧化物对应水化物的化学式为_________ ,A、D、H的氢化物的沸点由高到低的顺序为____________________ 。
(3) 非金属性D_________ E(填“大于”或“小于”)。下列事实能证明这一结论的是________ (选填字母序号)。
a.E的熔点低于D
b.氢化物的还原性:D > E
c.最高价氧化物对应的水化物酸性:E > D
d.氢化物的酸性:E >D
| 元素 | 有关性质或结构信息 |
| A | 地壳中含量最多的元素 |
| B | B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
| C | C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
| D | D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
| E | E与D同周期,且在该周期中原子半径最小 |
| F | F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
| G | G是形成化合物种类最多的元素 |
| H | H是与D相邻的同主族元素,且原子半径:H>D |
(1) B元素符号为
(2) A、C、E所形成简单离子半径由大到小的顺序是
(3) 非金属性D
a.E的熔点低于D
b.氢化物的还原性:D > E
c.最高价氧化物对应的水化物酸性:E > D
d.氢化物的酸性:E >D
您最近一年使用:0次
3 . 下图为元素周期表的一部分。根据元素①~⑦在周期表中的位置,按要求回答下列问题。
(1)元素①~⑦的单质中氧化性最强的是___________ 。(填化学式)
(2)元素③⑤⑥的原子的半径从大到小的顺序是___________ 。(用元素符号表示)
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是___________ 。
(4)元素②④⑦按原子数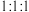 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是___________ 。
(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式___________ 。
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中 最大的是
最大的是___________ 。(填化学式)
(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| ② | ③ | |||||||
| ④ | ⑤ | ⑥ | ⑦ |
(2)元素③⑤⑥的原子的半径从大到小的顺序是
(3)元素②的简单气态氢化物的沸点高于元素⑥的,原因是
(4)元素②④⑦按原子数
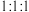 组成化合物甲,甲中所含化学键的类型是
组成化合物甲,甲中所含化学键的类型是(5)元素①与④组成的化合物可与水反应,写出反应的化学方程式
(6)元款④⑥⑦的最高价氧化物对应的水化物分别为A、B、C.相同条件下。相同物质的量浓度的A、B、C的水溶液中
 最大的是
最大的是(7)元素①与⑦组成的化合物为乙。用电子式表示乙的形成过程
您最近一年使用:0次
4 . W、X、Y、Z为元素周期表中原子序数依次增大的四种短周期元素,W的单原子阳离子的水溶液中能使紫色石蕊试液显红色,X的最外层电子数为次外层电子数的三倍,Y的单质遇水剧烈反应生成H2,Z位于第三周期VIIA族。下列说法正确的是
| A.Y的单质在空气中燃烧后的产物中阳离子和阴离子的个数比为1:1 |
| B.Al在YXW的水溶液中不反应 |
| C.Z的单质具有强氧化性,可以和KSCN溶液一起用于检测Fe2+ |
| D.检验水溶液中Z的单原子阴离子的方法是在溶液中滴加AgNO3,看是否产生白色沉淀 |
您最近一年使用:0次
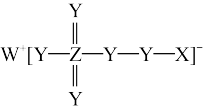
5 . 一种由前20号主族元素组成的化合物的结构如图所示, 、
、 、
、 、
、 原子序数依次增大且总和为44,其中
原子序数依次增大且总和为44,其中 原子最外层
原子最外层 轨道上有1对成对电子。下列叙述错误的是
轨道上有1对成对电子。下列叙述错误的是
 、
、 、
、 、
、 原子序数依次增大且总和为44,其中
原子序数依次增大且总和为44,其中 原子最外层
原子最外层 轨道上有1对成对电子。下列叙述错误的是
轨道上有1对成对电子。下列叙述错误的是
A.该化合物中 元素价态不同 元素价态不同 |
B.简单离子半径: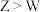 |
C. 因其强氧化性而使品红溶液褪色 因其强氧化性而使品红溶液褪色 |
D.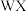 与 与 反应能生成 反应能生成 |
您最近一年使用:0次
名校
6 . 有W、X、Y、Z四种原子序数依次增大的元素。已知:
①W与X或Y形成的化合物的焰色反应均呈黄色;
②X原子次外层电子数为核外电子总数的一半
③X离子、Y离子均与Y的气态氢化物具有相同电子数
④Z可与Y组成常见化合物ZY2和ZY3;请回答:
(1)X的原子结构示意图___ ,
(2)写出工业上电解熔融WY的方法制取W,其化学方程式:__ 当电极上通过0.2mol电子时,生成的气体在标准状况下体积是__ L。
(3)将ZY饱和溶液滴入沸水可得到红褐色液体,此液体的分散系类型是___ 。
a.溶液 b.胶体 c.乳浊液
(4)写出一个能够证明Y单质的氧化性比X单质的氧化性强的化学方程式___ 。
①W与X或Y形成的化合物的焰色反应均呈黄色;
②X原子次外层电子数为核外电子总数的一半
③X离子、Y离子均与Y的气态氢化物具有相同电子数
④Z可与Y组成常见化合物ZY2和ZY3;请回答:
(1)X的原子结构示意图
(2)写出工业上电解熔融WY的方法制取W,其化学方程式:
(3)将ZY饱和溶液滴入沸水可得到红褐色液体,此液体的分散系类型是
a.溶液 b.胶体 c.乳浊液
(4)写出一个能够证明Y单质的氧化性比X单质的氧化性强的化学方程式
您最近一年使用:0次
名校
解题方法
7 . 前四周期主族元素V、W、X和Y,原子序数依次增大且最外层电子数之和为11,元素V的一种核素可用于文物断代,W的气态氢化物和其最高价氧化物的水化物能形成离子化合物,X是短周期原子半径最大的原子。下列说法正确的是:
| A.简单离子半径大小:r(W) < r(X ) < r(Y) |
| B.X与氧能形成两种只含离子键的化合物 |
| C.最高价氧化物对应水化物碱性:X > Y |
| D.简单氢化物的稳定性:W > V |
您最近一年使用:0次
20-21高二·全国·单元测试
解题方法
8 . 短周期主族元素W、X、Y、Z的原子序数依次增大。工业上以金红石(主要成分是TiO2)为原料制备金属钛的步骤:①在高温下,向金红石与W的单质组成的混合物中通入黄绿色气体单质Z,得到化合物甲和化学式为WX的气体乙,气体乙会与血红蛋白结合导致人体中毒;②金属Y形成的淡黄色氧化物可用于呼吸面具。在稀有气体环境和加热条件下,用Y的金属单质与甲反应可得钛。下列说法不正确的是
| A.W的氢化物的沸点一定小于X的氢化物 |
| B.简单离子半径:Z>Y>X |
| C.W与Z形成的化合物可用做工业上的重要有机溶剂 |
| D.含Z元素的某种盐具有强氧化性,可用于饮用水消毒 |
您最近一年使用:0次
名校
解题方法
9 . 根据给出的信息提示,填写下列空白。
(1)元素①的氢化物可以用来雕刻玻璃。写出其在元素周期表中的位置_______ 。
(2)在第三周期的主族元素中,元素②的原子半径最大,写出元素②的单质在空气中燃烧后主要产物的电子式_______ 。
(3)元素③的氢化物的水溶液能够与元素③的最高价氧化物的水溶液发生反应,试写出该反应的离子反应方程式_______ 。
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为金属锂和石墨,离子导体(电解质溶液)是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2↑。组装该电池必须在无水条件下进行,原因是_______ (用化学方程式表示)。
(5)用方程式解释陶瓷坩埚不能用来灼烧氢氧化钠固体的原因_______ 。
(6)常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
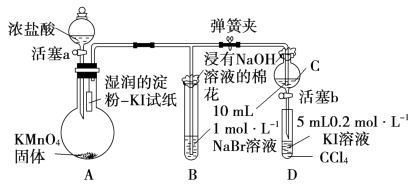
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.打开活塞b,使C中溶液滴入试管D中
V.关闭活塞b,取下试管D,振荡、静置
①验证氯气的氧化性强于碘的实验现象是_______ 。
②B中溶液发生反应的离子方程式是_______ 。
③该实验_______ (填“能”或“不能”)证明溴的氧化性强于碘,原因是_______ 。
(1)元素①的氢化物可以用来雕刻玻璃。写出其在元素周期表中的位置
(2)在第三周期的主族元素中,元素②的原子半径最大,写出元素②的单质在空气中燃烧后主要产物的电子式
(3)元素③的氢化物的水溶液能够与元素③的最高价氧化物的水溶液发生反应,试写出该反应的离子反应方程式
(4)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为金属锂和石墨,离子导体(电解质溶液)是LiAlCl4-SOCl2。电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2↑。组装该电池必须在无水条件下进行,原因是
(5)用方程式解释陶瓷坩埚不能用来灼烧氢氧化钠固体的原因
(6)常温下,KMnO4固体和浓盐酸反应产生氯气。为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.打开活塞b,使C中溶液滴入试管D中
V.关闭活塞b,取下试管D,振荡、静置
①验证氯气的氧化性强于碘的实验现象是
②B中溶液发生反应的离子方程式是
③该实验
您最近一年使用:0次
名校
10 . X、Y、Z、W是原子序数依次增大的短周期主族元素,原子序数之和为48,Y是金属元素,Y的单质能与强碱溶液反应放出气体,其余三种均为非金属元素。下列判断正确的是
| A.原子半径:W>Z>Y>X |
| B.Z的单质可用于生产太阳能电池 |
| C.W的简单气态氢化物具有较强的氧化性 |
| D.X的最高价氧化物对应的水化物为强酸 |
您最近一年使用:0次
2021-04-24更新
|
112次组卷
|
2卷引用:河南省天一大联考2020-2021学年高一下学期期中考试化学试题



