1 . X、Y为第三周期元素、Y最高正价与最低负价的代数和为6,二者形成的一种化合物能以[XY4]+[XY6]-的形式存在。下列说法错误的是
| A.原子半径:X>Y | B.简单氢化物的还原性:X>Y |
| C.同周期元素形成的单质中Y氧化性最强 | D.同周期中第一电离能小于X的元素有4种 |
您最近一年使用:0次
2021-06-29更新
|
13006次组卷
|
35卷引用:2021年新高考山东化学高考真题
2021年新高考山东化学高考真题(已下线)课时25 原子结构-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第36讲 原子结构与性质(精练)-2022年一轮复习讲练测(已下线)专题06 物质结构 元素周期律-备战2022年高考化学真题及地市好题专项集训【山东专用】江苏省如皋中学2021-2022学年高三上学期第一次阶段考试化学试题辽宁省渤海大学附属高级中学2021-2022学年高三上学期第二次月考化学试题辽宁省沈阳市第一二〇中学2021-2022学年高二上学期期中考试化学试题2021年湖北高考化学试题变式题11-192021年山东高考化学试题变式题1-10福建省福州第三中学2021-2022学年高三上学期第五次质量检测化学试题(已下线)查补易混易错点06 物质结构 元素周期律-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)浙江省温州新力量联盟2021-2022学年高二下学期期末联考化学试题(已下线)考点46 原子结构与性质-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第14讲 元素周期律和元素周期表(练)-2023年高考化学一轮复习讲练测(新教材新高考)北京市清华大学附属中学2022-2023学年高三9月月考化学试题四川省遂宁市射洪中学2022-2023学年高二上学期第一次月考(10月)化学试题湖南省长沙市卓华高级中学2021-2022学年高二下学期期末考试化学试题四川省内江市第六中学2022-2023学年高二上学期期中考试化学试题四川省遂宁中学校2022-2023学年高二上学期期中考试化学试题山东省济宁市邹城市孟子湖中学2021-2022学年高三下学期开学考试化学试题(已下线)专题九 物质结构与性质-实战高考·二轮复习核心突破天津市第四十七中学2022—2023学年高三上学期期末 阶段性学习检测化学试题天津市第四十七中学2022-2023学年高三上学期期末考试化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第五章 物质结构与性质 元素周期律 第27讲 元素周期表和元素周期律湖北省武汉市洪山高级中学2022-2023学年高二下学期2月考试化学试题安徽省安庆市第一中学2022-2023学年高二下学期第一次月考化学试题黑龙江省哈尔滨市第三中学2022-2023学年高二下学期第一次验收考试化学试题(已下线)江苏省南京市盐城市2023届高三3月第二次模拟考试化学试题变式题(选择题1-5)(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
解题方法
2 . 短周期主族元素X、Y、Z、W的原子序数依次增大,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法错误的是( )
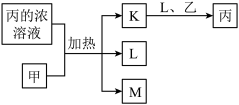

A.X、Y、Z三种元素的第一电离能: |
| B.X分别与Y、Z、W形成的分子中均可能含有非极性共价键 |
| C.Z元素的最高价含氧酸的酸性在同周期和同主族元素中均最强 |
D.若固体 是由直线形的 是由直线形的 和平面三角形的 和平面三角形的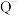 组成,则 组成,则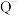 与丙溶液中的溶质阴离子相同 与丙溶液中的溶质阴离子相同 |
您最近一年使用:0次
2020-06-11更新
|
873次组卷
|
3卷引用:山东省日照市2020届高三校际联合考试(二模)化学试题
13-14高三·浙江温州·开学考试
解题方法
3 . 现有A、B、C、D四种短周期元素,它们之间的关系如下:
Ⅰ.原子半径:A < C < B < D Ⅱ.原子的最外层电子数:A + C =" B" + D = 8
Ⅲ.原子的核外电子层数:B =" C" = 2A Ⅳ.B元素的主要化合价:最高正价 + 最低负价 = 2
请回答:
(1)由A、B两种元素组成的常见气体,其电子式为_____ ;只有A和B两种元素组成的属于离子晶体的化合物可能为________ (用化学式表示)。
(2)由D元素形成的氢氧化物,与强碱溶液反应的离子方程式为______ 。
(3)由B、C元素组成的化合物BC3,该化合物具有强氧化性,与水反应生成两种酸和一种无色气体,该气体常温下遇空气变红棕色,写出该化合物与水反应的化学方程式______ 。
(4)由A、B和C三种元素组成的盐,常温下其水溶液显酸性,则0.1 mol·L-1该盐溶液中浓度最大的离子为___ (写离子符号)。
(5)由A、B、C和D四种元素组成的配位化合物己,写出己的化学式______ ;写出检验化合物己中所含阳离子的实验方法________ 。
Ⅰ.原子半径:A < C < B < D Ⅱ.原子的最外层电子数:A + C =" B" + D = 8
Ⅲ.原子的核外电子层数:B =" C" = 2A Ⅳ.B元素的主要化合价:最高正价 + 最低负价 = 2
请回答:
(1)由A、B两种元素组成的常见气体,其电子式为
(2)由D元素形成的氢氧化物,与强碱溶液反应的离子方程式为
(3)由B、C元素组成的化合物BC3,该化合物具有强氧化性,与水反应生成两种酸和一种无色气体,该气体常温下遇空气变红棕色,写出该化合物与水反应的化学方程式
(4)由A、B和C三种元素组成的盐,常温下其水溶液显酸性,则0.1 mol·L-1该盐溶液中浓度最大的离子为
(5)由A、B、C和D四种元素组成的配位化合物己,写出己的化学式
您最近一年使用:0次
名校
4 . 短周期主族元素X、Y、Z和W的原子序数依次增大,X、Y、W位于不同周期,Y、Z、W的原子最外层电子数之和为14,Z的原子半径在短周期主族元素中最大。下列说法错误的是( )
| A.简单离子半径:W>Z>X |
| B.W的最高价氧化物对应的水化物为强酸 |
| C.Y与Z形成的化合物溶于水所得溶液呈碱性 |
| D.与X形成的简单化合物的还原性:Y>Z>W |
您最近一年使用:0次
2020-04-03更新
|
2672次组卷
|
4卷引用:福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题
福建省泉州市2020届高三下学期3月适应性线上测试卷理综化学试题解题达人.化学选择题(2021全国卷)提升小卷16(已下线)押新高考卷06题 元素周期表元素周期律-备战2022年高考化学临考题号押题(新高考通版)江西省安义中学2022-2023学年高三上学期中考试化学试题
解题方法
5 . 元素周期表与元素周期律在学习、研究中有很重要的作用。下表所示为某5种元素的相关信息,已知W、X都位于第三周期。
请回答:
(1)W在元素周期表中的位置为_______ ,Q、W、X形成的简单离子半径的由大到小顺序是_______ (用离子符号表示)。
(2)用电子式表示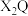 的形成过程:
的形成过程:_______ 。
(3)写出Y的单质与Q最简单氢化物反应的化学方程式_______ 。根据元素周期律可知金属性:Y>X,用原子结构解释原因:_______ 。
(4)下列对于Z及其化合物的推断中正确的是_______(填字母)。
(5)将X元素的单质在Q元素的单质中点燃生成M,预测将M投入硫酸亚铁溶液中,主要的反应现象是_______ 。
(6)原子序数为Q的2倍的元素,与Q组成的气体化合物具有漂白性,请设计简单实验方案验证其漂白性_______ 。
| 元素 | 相关信息 |
| Q | 最外层电子数是次外层电子数的3倍 |
| W | 最高化合价为 |
| X | 最高价氧化物对应的水化物在本周期中碱性最强 |
| Y | 焰色试验(透过蓝色钴玻璃)的火焰呈紫色 |
| Z | 与W同主族且其单质在 溶液中呈橙色 溶液中呈橙色 |
(1)W在元素周期表中的位置为
(2)用电子式表示
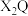 的形成过程:
的形成过程:(3)写出Y的单质与Q最简单氢化物反应的化学方程式
(4)下列对于Z及其化合物的推断中正确的是_______(填字母)。
A.Z的化合价中有 和 和 |
| B.Z的最高价氧化物对应水化物的酸性强于W的最高价氧化物对应水化物的酸性 |
| C.Z简单气态氢化物的稳定性弱于W简单气态氢化物的稳定性 |
| D.Z单质可以从含有W的盐溶液中置换出W |
(6)原子序数为Q的2倍的元素,与Q组成的气体化合物具有漂白性,请设计简单实验方案验证其漂白性
您最近一年使用:0次
名校
6 . A、B、C、D是四种短周期元素,E是过渡元素。A、B、C同周期,C、D同主族,A原子M层电子数是L层的一半,B是同周期第一电离能最小的元素,C在同周期中未成对电子数最多,E的外围电子排布式为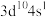 。回答下列问题:
。回答下列问题:
(1)A的基态原子中的电子有_______ 种不同的能量状态,B的基态原子中有_______ 种不同运动状态的电子。
(2)上述元素中最高价氧化物对应水化物酸性最弱的与碱性最强的物质发生反应的方程式是_______ 。
(3)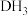 分子的
分子的 模型为
模型为_______ ,E元素在周期表的位置是_______ 。
(4)C与D的简单氢化物熔点相比后者的高,解释原因_______ ,A与碳形成的某晶体可用作打磨砂轮原料,1mol该晶体含有的共价键为_______ 个。
(5)C可形成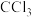 、
、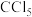 ,D只能形成
,D只能形成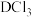 解释原因
解释原因_______ 。
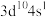 。回答下列问题:
。回答下列问题:(1)A的基态原子中的电子有
(2)上述元素中最高价氧化物对应水化物酸性最弱的与碱性最强的物质发生反应的方程式是
(3)
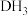 分子的
分子的 模型为
模型为(4)C与D的简单氢化物熔点相比后者的高,解释原因
(5)C可形成
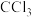 、
、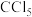 ,D只能形成
,D只能形成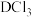 解释原因
解释原因
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、W是原子序数依次增大的短周期元素。W与X位于同一主族; X、 Y、Z三种元素形成的化合物具有强氧化性,能灭活新冠病毒,其结构如图所示。下列叙述不正确的是
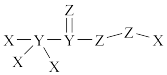
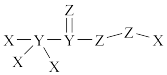
| A.该化合物含极性键和非极性键 |
| B.该化合物中各元素原子均达稳定结构 |
| C.Z、W形成的简单离子半径,Z大于W |
| D.由X、Y、Z、W四种元素形成的化合物一定能与X、Z、W形成的化合物反应 |
您最近一年使用:0次
2021-05-31更新
|
1158次组卷
|
4卷引用:四川省达州市普通高中2021届高三第二次诊断性测试理科综合化学试题
解题方法
8 . X、Y、Z 为不同短周期非金属元素的气态单质。在一定条件下能发生如下反应:
Y+X → 甲(g),Y+Z → 乙(g)。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。
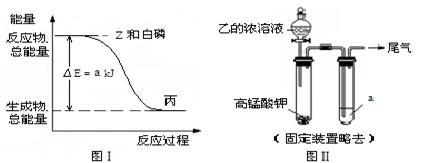
(1)X 的电子式是__________ 。
(2)白磷(P4)在 Z 气体中燃烧可生成液态丙分子,也可生成固态丁分子。已知丙分子中各原子最外层均是 8 电子结构,丙的结构式是__________ 。 白磷固体和 Z 气体反应,生成 1 mol 液态丙时,能量变化如图Ⅰ所示,写出该反应的热化学方程式: _____________________________ 。已知 1 mol 白磷固体和 Z 气体反应,生成固态丁时,放热 b kJ,则 1 mol 固态丁转化为液态丙时的反应热△H =____________________ 。
(3)某同学拟用图Ⅱ所示装置证明氧化性Z>I2,已知高锰酸钾与乙的浓溶液反应生成Z,则 a____ 的水溶液。若仅将 a 换为甲的浓溶液,实验时会产生大量白烟并有气体单质生成,该反应的化学方程式是____________________ 。
(4)向一定浓度的 BaCl2溶液中通入 SO2气体,未见沉淀生成,若在通入 SO2气体的同时加入由 X、 Y、Z 中的一种或几种元素组成的某纯净物,即可生成白色沉淀,该纯净物可能是__________ 。
Y+X → 甲(g),Y+Z → 乙(g)。甲、乙可化合生成离子化合物,甲的相对分子质量小于乙。

(1)X 的电子式是
(2)白磷(P4)在 Z 气体中燃烧可生成液态丙分子,也可生成固态丁分子。已知丙分子中各原子最外层均是 8 电子结构,丙的结构式是
(3)某同学拟用图Ⅱ所示装置证明氧化性Z>I2,已知高锰酸钾与乙的浓溶液反应生成Z,则 a
(4)向一定浓度的 BaCl2溶液中通入 SO2气体,未见沉淀生成,若在通入 SO2气体的同时加入由 X、 Y、Z 中的一种或几种元素组成的某纯净物,即可生成白色沉淀,该纯净物可能是
您最近一年使用:0次
10-11高三·河北衡水·阶段练习
9 . 下表中列出五种短周期元素A、B、C、D、E的信息,请推断后作答:
(1)画出B的离子结构示意图______ ;写出D元素最高价氧化物的水化物电子式_________
(2)盐X水溶液显____ (填“酸”“碱”“中”)性,用离子方程式解释其原因________________
(3)D2CA3的溶液与B的单质能发生反应,其反应的离子方程式为________
(4)已知E元素的某种氢化物Y与A2的摩尔质量相同。Y与空气组成的燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。该燃料电池放电时,正极的电极反应式是________________________________
(5)如右图是一个电解过程示意图。
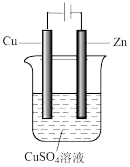
假设使用Y-空气燃料电池作为本过程的电源,铜片质量变化128g,则Y一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)_______________ L
| 元素 | 有关信息 |
| A | 元素主要化合价为—2,原子半径为0.074 n m |
| B | 所在主族序数与所在周期序数之差为4 |
| C | 原子半径为0.102 n m,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物的水化物,能按1∶1电离出电子数相等的阴、阳离子 |
| E | 原子半径为0.075 n m,最高价氧化物的水化物与其氢化物组成一种盐X |
(2)盐X水溶液显
(3)D2CA3的溶液与B的单质能发生反应,其反应的离子方程式为
(4)已知E元素的某种氢化物Y与A2的摩尔质量相同。Y与空气组成的燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。该燃料电池放电时,正极的电极反应式是
(5)如右图是一个电解过程示意图。

假设使用Y-空气燃料电池作为本过程的电源,铜片质量变化128g,则Y一空气燃料电池理论上消耗标准状况下的空气(设空气中氧气的体积含量为20%)
您最近一年使用:0次
名校
10 . 短周期主族元素X、Y、Z、Q、R的原子序数依次增大,其中X的单质是密度最小的气体,Z是同周期中原子半径最大的元素,Y与Q同主族,且Q的原子序数是Y的两倍。回答下列问题:
(1)Z的原子结构示意图为__________ ,R在元素周期表中的位置是______________ 。
(2)Z的最高价氧化物对应水化物所含化学键类型是_______________ 。Q、R的最高价氧化物对应的水化物酸性较强的是__________ (填化学式)。
(3)由X和Y可以形成一种液态化合物T,T分子含18个电子,则其电子式为_______ 。将Q的低价氧化物通入T可以生成一种强酸,反应的化学方程式为___________________ 。
(4)氮元素的一种氢化物M,M分子含18个电子,用惰性电极,M、氧气和Z的最高价氧化物对应水化物的溶液设计一个燃料电池,则M发生的电极反应式为______________________ 。
(5)在2 L密闭容器中分别充入4 mol A气体和6 mol B气体,在一定条件下发生反应:4A(g)+5B(g) 4C(g)+xD(g),5 min后达到平衡状态,经测定B的转化率为75%,D的浓度为2.7 mol·L-1。则x=
4C(g)+xD(g),5 min后达到平衡状态,经测定B的转化率为75%,D的浓度为2.7 mol·L-1。则x=_______ ;A在平衡混合物中的体积分数为________ ;从反应开始至平衡时,以C的浓度变化表示该反应的平均速率v(C)=_____________ 。
(1)Z的原子结构示意图为
(2)Z的最高价氧化物对应水化物所含化学键类型是
(3)由X和Y可以形成一种液态化合物T,T分子含18个电子,则其电子式为
(4)氮元素的一种氢化物M,M分子含18个电子,用惰性电极,M、氧气和Z的最高价氧化物对应水化物的溶液设计一个燃料电池,则M发生的电极反应式为
(5)在2 L密闭容器中分别充入4 mol A气体和6 mol B气体,在一定条件下发生反应:4A(g)+5B(g)
 4C(g)+xD(g),5 min后达到平衡状态,经测定B的转化率为75%,D的浓度为2.7 mol·L-1。则x=
4C(g)+xD(g),5 min后达到平衡状态,经测定B的转化率为75%,D的浓度为2.7 mol·L-1。则x=
您最近一年使用:0次



