名校
1 . 短周期主族元素A、B、C、D的原子序数依次增大,A元素与C元素同主族,B的单质可以在A的单质中燃烧,生成一种具有强氧化性的物质,C元素与D元素相邻,D元素最高价氧化物对应的水化物和氢化物溶于水都能完全电离。下列说法错误的是
| A.元素A与元素B形成的两种化合物中,阴、阳离子个数比都是1:2 |
| B.D的氢化物酸性强于C的氢化物酸性,可证明非金属性:D>C |
| C.可用CS2清洗试管内壁附着的C单质 |
| D.简单离子半径:C>D>A>B |
您最近半年使用:0次
2 . 中国地质科学院地质研究所对嫦娥五号带回的月球玄武岩开展了分析,证明月球在19.6亿年前仍存在岩浆活动。A、B、C、D、E是月球玄武岩中含有的五种元素,均为前20号元素,原子序数依次增大;A、D同族,D的单质常在地球火山口附近沉积,B、D、E最高价氧化物对应的水化物可以两两反应,C是地壳中含量第二位的元素,含E物质的焰色透过蓝色钴玻璃片为紫色。下列说法错误的是
| A.简单氢化物的沸点:A<D |
| B.原子半径:E>B>D |
C.B、E最高价氧化物的对应水化物反应的离子方程式为: |
| D.单质C广泛应用于信息技术和新能源技术等领域 |
您最近半年使用:0次
名校
3 . 中国地质科学院地质研究所对嫦娥五号月球玄武岩开展了年代学、元素、同位素分析,证明月球在19.6亿年前仍存在岩浆活动。A、B、C、D、E是月核中含有的五种原子序数依次增大的前20号元素,A、D同族,D的单质常在地球火山口附近沉积,B、D、E最高价氧化物的水化物可以两两反应,C是地壳中含量第二的元素。下列说法错误的是
| A.简单离子半径:E>D>B |
| B.简单氢化物的稳定性:A>D |
| C.A与C形成的化合物是制备玻璃的原料之一 |
| D.单质C广泛应用于信息技术和新能源技术等领域 |
您最近半年使用:0次
2023-05-15更新
|
341次组卷
|
3卷引用:湖北省荆荆襄宜四地七校考试联盟2022-2023学年高一下学期期中联考化学试题
名校
4 . 如表是元素周期表主族元素的一部分,请参照元素①~⑥在表中的位置,回答下列问题:

(1)②在周期表中的位置______ 。
(2)①的简单氢化物的电子式______ 。
(3)③④⑤形成的简单离子半径由大到小的排序是______ (用离子符号表示)。
(4)用电子式表示③和⑥形成的化合物的过程______ 。
(5)写出⑤单质与③的最高价氧化物对应水化物反应的离子方程式______ 。
(6)③和④中金属性强的是______ (填“元素符号”),以下说法能证明该结论的是______ 。
a.③容易失去1个e-,而④容易失去2个e-
b.③与冷水剧烈反应,而④与冷水反应缓慢
c.③和④的最高价氧化物对应水化物的碱性:③>④
(7)硒(Se)位于第四周期,与②同主族。下列推断不正确 的是______ 。
a.Se最低价为-2价
b.Se单质常温下也呈气态,只有氧化性
c.沸点:H2Se<H2O

(1)②在周期表中的位置
(2)①的简单氢化物的电子式
(3)③④⑤形成的简单离子半径由大到小的排序是
(4)用电子式表示③和⑥形成的化合物的过程
(5)写出⑤单质与③的最高价氧化物对应水化物反应的离子方程式
(6)③和④中金属性强的是
a.③容易失去1个e-,而④容易失去2个e-
b.③与冷水剧烈反应,而④与冷水反应缓慢
c.③和④的最高价氧化物对应水化物的碱性:③>④
(7)硒(Se)位于第四周期,与②同主族。下列推断
a.Se最低价为-2价
b.Se单质常温下也呈气态,只有氧化性
c.沸点:H2Se<H2O
您最近半年使用:0次
2023-04-23更新
|
166次组卷
|
2卷引用:广西壮族自治区玉林市2022-2023学年高一上学期1月期末考试化学试题
名校
解题方法
5 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4,请回答下列问题:
(1)用电子式表示 的形成过程
的形成过程______ 。
(2)W在周期表中的位置是______ 。
(3)ZYX的电子式为______ , 的结构式为
的结构式为______ , 中含有的化学键类型为
中含有的化学键类型为______ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是______ (用元素的离子符号表示)。
(5)下列说法能证明非金属性Q强于R的是______ (填字母)。
a.简单阴离子的还原性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性:
(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是______ 。
(7)处于周期表中对角线位置(左上方和右下方)的元素,其性质具有相似性,称为“对角线规则”,写出 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式______ 。
(1)用电子式表示
 的形成过程
的形成过程(2)W在周期表中的位置是
(3)ZYX的电子式为
 的结构式为
的结构式为 中含有的化学键类型为
中含有的化学键类型为(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:

b.简单氢化物热稳定性:

c.氧化物对应的水化物的酸性:

(6)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
(7)处于周期表中对角线位置(左上方和右下方)的元素,其性质具有相似性,称为“对角线规则”,写出
 与氢氧化钠溶液反应的化学方程式
与氢氧化钠溶液反应的化学方程式
您最近半年使用:0次
名校
6 . 下图是元素周期表的一部分。按要求填写下列空白:

(1)元素⑦在周期表中的位置为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物中所含的化学键为_______ ;③的氢化物的电子式为_______ 。
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素⑦在周期表中的位置为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物中所含的化学键为
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近半年使用:0次
2023-01-31更新
|
189次组卷
|
2卷引用:湖南省永州市第一中学2022-2023学年高一上学期期末阶段性考试化学试题
解题方法
7 . 化合物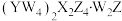 为无色柱状晶体,受热易分解,已知
为无色柱状晶体,受热易分解,已知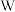 、
、 、
、 、
、 的原子序数依次增大,其和为22,
的原子序数依次增大,其和为22, 、
、 、
、 为同一周期相邻元素。可利用下图装置检验该化合物分解出的相同元素组成的不同产物。
为同一周期相邻元素。可利用下图装置检验该化合物分解出的相同元素组成的不同产物。
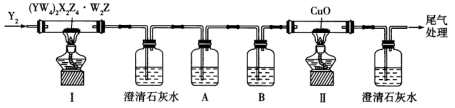
下列说法错误的是
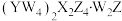 为无色柱状晶体,受热易分解,已知
为无色柱状晶体,受热易分解,已知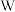 、
、 、
、 、
、 的原子序数依次增大,其和为22,
的原子序数依次增大,其和为22, 、
、 、
、 为同一周期相邻元素。可利用下图装置检验该化合物分解出的相同元素组成的不同产物。
为同一周期相邻元素。可利用下图装置检验该化合物分解出的相同元素组成的不同产物。
下列说法错误的是
A.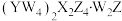 属于含有共价键的离子化合物 属于含有共价键的离子化合物 |
B. 、 、 两种元素的简单氢化物的稳定性: 两种元素的简单氢化物的稳定性: |
C.反应开始前通入 ,可以避免装置中的空气干扰产物的检验 ,可以避免装置中的空气干扰产物的检验 |
D.装置中两处澄清石灰水都变浑浊,证明分解产物中含有两种由 、 、 组成的物质 组成的物质 |
您最近半年使用:0次
8 . A、B、X、D、E、Y为短周期元素,原子序数依次增大,有关信息如表中所示:
(1)六种元素中原子半径最大的是_______ ( 填元素符号)。
(2)A在周期表中的位置是_______ 。
(3)A和B的最简单氢化物中较稳定的是_______ (填化学式)。
(4)B、X以原子个数比为1:1组成的化合物W,常用于呼吸面具中做供氧剂。写出W的电子式_______ ,其所含化学键的类型为_______ 。
(5)D的氧化物与X的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(6)Y的最高价氧化物对应的水化物的化学式为_______ 。
(7)下列说法中能证明Y的非金属性强于E的是_______( 填字母)。
| A | 一种同位素常用于文物年代的测定 |
| B | 最外层电子数是电子层数的3倍 |
| X | M层有1个电子,单质需保存在煤油中 |
| D | 地壳中含量最多的金属元素 |
| E | 与B可形成EB2和EB3两种物质,EB2是形成酸雨的主要物质 |
| Y | 单质可用于生产漂白液、漂白粉 |
(2)A在周期表中的位置是
(3)A和B的最简单氢化物中较稳定的是
(4)B、X以原子个数比为1:1组成的化合物W,常用于呼吸面具中做供氧剂。写出W的电子式
(5)D的氧化物与X的最高价氧化物对应的水化物反应的离子方程式是
(6)Y的最高价氧化物对应的水化物的化学式为
(7)下列说法中能证明Y的非金属性强于E的是_______( 填字母)。
| A.E的单质在常温下为固体而Y的单质为气体 |
| B.与Fe反应时,Y的单质能生成高价铁化合物,E的单质只能生成低价铁化合物 |
| C.简单气态氢化物的稳定性:Y>E |
| D.H2EO3的酸性弱于HYO3 |
您最近半年使用:0次
解题方法
9 . 在短周期元素中有部分元素的原子具有核外电子排布有2个未成对电子的特点。具有这样特点的元素中:
(1)A元素原子的半径最大,写出A在元素周期表中的位置___________ ,其原子核外电子排布式为___________ ,A与上述元素中原子半径最小的元素B形成的化合物晶体类型为___________ 。
(2)C元素的单质能溶解于C与D形成的化合物中,写出该化合物的分子式___________ ,推断该化合物___________ (难、微、易)溶于水。
(3)C、D元素均可与B元素形成化合物,此2种化合物都可与水反应形成对应的酸,2种酸的分子式相似,写出2种酸的分子式___________ ,简述证明2种酸酸性相对强弱的方法___________ 。
Cu2S和CuS均可被KMnO4酸性溶液氧化,在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
① + Cu2S +
+ Cu2S + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)
② + CuS +
+ CuS + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)
(4)下列关于反应①的说法中错误的是___________ (选填编号)。
a.还原性的强弱关系是: > Cu2S
> Cu2S
b.氧化剂与还原剂的物质的量之比为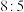
c.生成2.24L(标况下)SO2,转移电子的物质的量是0.8mol
d.被氧化的元素是正一价的Cu和负二价的S
(4)写出反应②中反应物配平后的系数并标出电子转移方向和数目:___________
___________ +___________CuS +___________
+___________CuS +___________
已知:KMnO4在稀硫酸存在下能将H2O2氧化为O2,KMnO4被还原为 ;H2O2在前面反应生成
;H2O2在前面反应生成 的催化下能发生分解反应生成H2O和O2。
的催化下能发生分解反应生成H2O和O2。
(5)稀硫酸中,某KMnO4和H2O2发生氧化还原反应方程式如下:
2KMnO4 + 7H2O2 + 3H2SO4 → K2SO4 + 2MnSO4 + 6O2↑ + 10H2O,反应中1mol KMnO4氧化H2O2的物质的量是___________ mol, 反应中的氧化剂是___________ ,氧化剂与还原剂的物质的量比为___________ 。
(1)A元素原子的半径最大,写出A在元素周期表中的位置
(2)C元素的单质能溶解于C与D形成的化合物中,写出该化合物的分子式
(3)C、D元素均可与B元素形成化合物,此2种化合物都可与水反应形成对应的酸,2种酸的分子式相似,写出2种酸的分子式
Cu2S和CuS均可被KMnO4酸性溶液氧化,在用KMnO4酸性溶液处理Cu2S和CuS的混合物时,发生的反应如下:
①
 + Cu2S +
+ Cu2S + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)②
 + CuS +
+ CuS + →
→ + SO2↑ +
+ SO2↑ + + H2O(未配平)
+ H2O(未配平)(4)下列关于反应①的说法中错误的是
a.还原性的强弱关系是:
 > Cu2S
> Cu2Sb.氧化剂与还原剂的物质的量之比为
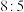
c.生成2.24L(标况下)SO2,转移电子的物质的量是0.8mol
d.被氧化的元素是正一价的Cu和负二价的S
(4)写出反应②中反应物配平后的系数并标出电子转移方向和数目:
___________
 +___________CuS +___________
+___________CuS +___________
已知:KMnO4在稀硫酸存在下能将H2O2氧化为O2,KMnO4被还原为
 ;H2O2在前面反应生成
;H2O2在前面反应生成 的催化下能发生分解反应生成H2O和O2。
的催化下能发生分解反应生成H2O和O2。(5)稀硫酸中,某KMnO4和H2O2发生氧化还原反应方程式如下:
2KMnO4 + 7H2O2 + 3H2SO4 → K2SO4 + 2MnSO4 + 6O2↑ + 10H2O,反应中1mol KMnO4氧化H2O2的物质的量是
您最近半年使用:0次
名校
解题方法
10 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。请回答下列问题:
(1)Y的元素名称是______ 。
(2)W在周期表中的位置是______ 。
(3)写出化合物Z2R的电子式______ 。
(4)写出化合物X2Y2的结构式______ 。
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是______ (用元素的离子符号表示)。
(6)下列说法能证明非金属性Q强于R的是______ (填序号)。
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是______ 。
(1)Y的元素名称是
(2)W在周期表中的位置是
(3)写出化合物Z2R的电子式
(4)写出化合物X2Y2的结构式
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(6)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
您最近半年使用:0次
2021-01-19更新
|
588次组卷
|
5卷引用:辽宁省锦州市2020-2021学年高一上学期期末考试化学试题



