1 . 元素的“价类二维图”体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如下图所示。

回答下列问题:
(1)写出物质R的电子式。_______ 。
(2)下列有关图中所示含N、S物质的叙述,正确的是_______ (填标号)。
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物
e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将 的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是_______ 。
(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析, 晶体中所含化学键的类型有
晶体中所含化学键的类型有_______ ,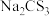 水溶液显
水溶液显_______ (填“酸性”、“碱性”或“中性”)。
(5) (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: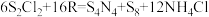 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有_______ ,该反应每生成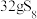 转移电子
转移电子_______  。其中被氧化的元素是
。其中被氧化的元素是_______ (填元素符号)。

回答下列问题:
(1)写出物质R的电子式。
(2)下列有关图中所示含N、S物质的叙述,正确的是
a.在催化剂的作用下,R可将Y、Z还原为X
b.图中所示的物质中,只有W、D、E属于电解质
c.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生
d.Z、C、F均能与
 溶液反应,都是酸性氧化物
溶液反应,都是酸性氧化物e.制备焦亚硫酸钠(Na2S2O5),从氧化还原反应的角度分析,可选择B和D反应
(3)将
 的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是
的物质W的稀溶液加入物质D的溶液中,可生成物质E,该反应的离子方程式是(4)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析,
 晶体中所含化学键的类型有
晶体中所含化学键的类型有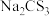 水溶液显
水溶液显(5)
 (S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入
(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质R通入 的
的 溶液中,可制得该物质:
溶液中,可制得该物质: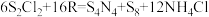 ,上述反应中,物质R体现的性质有
,上述反应中,物质R体现的性质有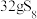 转移电子
转移电子 。其中被氧化的元素是
。其中被氧化的元素是
您最近半年使用:0次
名校
2 . 短周期主族元素X、Y、Z、W、M的原子半径依次增大,与元素有关的信息如表所示:
回答下列问题:
(1) 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为___________ ,写出其简单氢化物的一种用途:___________ 。
(2)由 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为___________ 。
(3)上述元素对应的简单离子中半径最大的为___________ (填离子符号)。
(4) 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为___________ 。
(5) 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程___________ 。
(6) 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为___________ 。
(7)下列关于 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。
| 元素 | 相关信息 |
 | 简单氢化物的水溶液可以刻蚀玻璃 |
 | 最外层电子数比次外层多3 |
 | 最高正价和最低负价的代数和为4 |
 | 地壳中含量最高的金属元素 |
 | 最高价氧化物对应水化物属于强碱 |
(1)
 的一种核素含有8个中子,其核素符号为
的一种核素含有8个中子,其核素符号为(2)由
 与
与 组成的化合物含有的化学键类型为
组成的化合物含有的化学键类型为(3)上述元素对应的简单离子中半径最大的为
(4)
 单质与
单质与 的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为
的最高价氧化物对应水化物混合使用,可用于疏通地下管道,其发生反应的离子方程式为(5)
 与
与 形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程
形成的一种化合物中,所有原子均满足8电子稳定结构,用电子式表示该化合物的形成过程(6)
 的简单氢化物的沸点比
的简单氢化物的沸点比 的简单氢化物的沸点高,从结构角度分析其原因为
的简单氢化物的沸点高,从结构角度分析其原因为(7)下列关于
 及
及 同主族元素的说法错误的是___________。
同主族元素的说法错误的是___________。A.将 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 的单质通入其同族元素与钠形成的钠盐溶液中,可置换出同族元素的单质 |
| B.随着原子序数递增,该主族元素对应单质的沸点逐渐升高 |
C.该主族元素中最高价氧化物对应水化物酸性最强的元素为 |
D. 的简单氢化物可与强碱溶液反应 的简单氢化物可与强碱溶液反应 |
您最近半年使用:0次
名校
3 . A、B、C、D、E、F是原子序数依次增大的元素,其相关信息如下。
回答下列问题:
(1)元素A和E形成的化合物的电子式为___________ ,该化合物含有的化学键类型是___________ 。
(2)元素B在元素周期表中的位置为___________ ,其原子结构示意图为___________ 。
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为___________ ;元素D形成的单质久置于空气中最终得到的化合物的化学式为___________ 。
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
| 元素 | 特征 | 元素 | 特征 |
| A | 该元素的某种原子不含中子 | B | 简单氢化物的分子结构模型为 |
| C | 在人体中含量最多 | D | 该元素形成的化合物灼烧时火焰呈现黄色 |
| E | 该元素形成的单质常温下是黄绿色的有毒气体 | F | 由该元素形成的合金是目前我国用途最广的合金 |
(1)元素A和E形成的化合物的电子式为
(2)元素B在元素周期表中的位置为
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
A.酸性: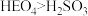 | B. 通入 通入 溶液能产生黄色沉淀 溶液能产生黄色沉淀 |
C.氢化物稳定性: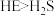 | D.常温下,E的单质为气态,S的单质为固态 |
您最近半年使用:0次
名校
解题方法
4 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量含氧橄榄石矿物(ZxW2-xRX4)。已知前四周期元素X、Y、Z、R、W的原子序数依次增大,Y的氢化物常用于雕刻玻璃,R元素的一种氧化物可制作光导纤维,W的合金材料是生活中用途最广泛的金属材料,基态Z原子核外s,p能级上电子总数相等。下列叙述正确的是
| A.原子半径:Z>R>Y>X |
| B.X的第一电离能比同周期相邻元素小 |
| C.X的简单氢化物的热稳定性强于Y的简单氢化物 |
| D.熔点:ZY2>RX2 |
您最近半年使用:0次
2023-10-26更新
|
933次组卷
|
6卷引用:湖南省郴州市2024届高三上学期一模化学试题
湖南省郴州市2024届高三上学期一模化学试题湖南省邵阳市绥宁县世贤中学2023-2024学年高三上学期12月月考化学试题广西名校2023-2024学年高三上学期仿真卷(一)化学试题湖南省常德市 临澧县第一中学2023-2024学年高三上学期第五次阶段性考试化学试题(已下线)专题04 物质结构与性质 元素推断-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)2024届海南省海南中学高三下学期第一次模拟化学试题
名校
5 . 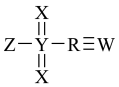 是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
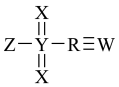 是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是A. 与 与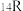 的中子数相同 的中子数相同 |
| B.第一电离能:X>W>R |
| C.简单氢化物还原性:Z>Y |
| D.R、W、X三种元素均能与氢元素形成含非极性键的二元化合物 |
您最近半年使用:0次
解题方法
6 . 已知:A、B、C、D是短周期主族元素,E、F为长周期元素,请根据下列信息回答有关问题。
(1)写出A元素的最高价氧化物的电子式:___________ ;C、D、E的简单离子半径由大到小的顺序为___________ (填离子符号)。
(2)写出E元素的氧化物(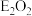 )与水反应的离子方程式:
)与水反应的离子方程式:___________ 。
(3)F元素的单质可以在C元素的单质中燃烧,其产物的饱和溶液与沸水反应可以得到能产生丁达尔效应的分散系,写出该产物的浓溶液与沸水反应的化学方程式:___________ 。
(4)C元素的最高价氧化物对应的水化物与E元素的最高价氧化物对应的水化物反应的离子方程式为___________ 。
(5)B元素与E元素形成的化合物属于___________ (填“离子”或“共价”)化合物,该化合物中所含的化学键为___________ (填“共价键”或“离子键”)。
| ① | A的一种氧化物可用于人工降雨 |
| ② | B元素的简单阳离子中没有电子 |
| ③ | C的单质为黄绿色气体 |
| ④ | D是地壳中含量最高的金属元素 |
| ⑤ | E位于元素周期表第ⅠA族,核外电子层数为4 |
| ⑥ | F是用途最广泛的金属,它的一种氧化物可以作磁性材料 |
(2)写出E元素的氧化物(
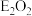 )与水反应的离子方程式:
)与水反应的离子方程式:(3)F元素的单质可以在C元素的单质中燃烧,其产物的饱和溶液与沸水反应可以得到能产生丁达尔效应的分散系,写出该产物的浓溶液与沸水反应的化学方程式:
(4)C元素的最高价氧化物对应的水化物与E元素的最高价氧化物对应的水化物反应的离子方程式为
(5)B元素与E元素形成的化合物属于
您最近半年使用:0次
解题方法
7 . 已知A为淡黄色固体,T、R为日常生活中两种常见的用途很广的金属单质,D是具有磁性的黑色晶体,C是无色无味的气体,H是白色沉淀,且在潮湿空气中迅速变为灰绿色,最终变为红褐色固体M。
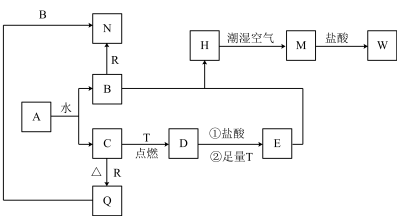
(1)写出下列物质的化学式:A:___________ ,D:___________ ,W:___________ 。
(2)按要求写出下列方程式:
①B和Q反应的离子方程式:___________ 。
②D和稀盐酸反应后的溶液与足量T反应的离子方程式:___________ 。
③H在潮湿空气中变成M的化学方程式:___________ 。
④检验W中阴离子的方法:___________ 。

(1)写出下列物质的化学式:A:
(2)按要求写出下列方程式:
①B和Q反应的离子方程式:
②D和稀盐酸反应后的溶液与足量T反应的离子方程式:
③H在潮湿空气中变成M的化学方程式:
④检验W中阴离子的方法:
您最近半年使用:0次
名校
8 . 如表为部分元素的特点
请回答下列问题:
(1)若火灾现场存放大量Y,需要用______ 灭火;化合物Y2X2中存在的化学键类型为______ 。
(2)向含+3价L离子的溶液中滴加KI溶液,再滴入淀粉溶液,溶液呈______ 色,说明还原性有:L2+______ I-(填“>”或“<”);
(3)混合物甲由两种常见化合物组成,每种化合物含X、Y、Z、Q四种元素中的至少三种元素,在向甲中逐滴滴加盐酸的过程中,产生的QX2气体的物质的量与滴加的盐酸体积关系如图所示:
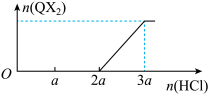
由此可知,混合物甲的组成为______ (填化学式),两者的物质的量之比为______ 。
(4)使用下列装置再添加合适的药品,可以证明R和Q两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸 ②稀硫酸 ③盐酸 ④Na2CO3固体 ⑤CaCO3⑥澄清石灰水 ⑦NaOH溶液
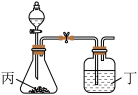
请选择装置丙、丁两处应该加入的药品代号:丙______ 、丁______ 。
| 特点 | 元素代号 |
| 地壳中含量最高的元素 | X |
| +1价阳离子L层充满电子 | Y |
| 原子半径最小的原子 | Z |
| 一种同位素可以用于考古 | Q |
| 与上述代号为Z的元素形成分子Z2R,其摩尔质量为34g/mol | R |
| 其合金用量最大,用途最广 | L |
(1)若火灾现场存放大量Y,需要用
(2)向含+3价L离子的溶液中滴加KI溶液,再滴入淀粉溶液,溶液呈
(3)混合物甲由两种常见化合物组成,每种化合物含X、Y、Z、Q四种元素中的至少三种元素,在向甲中逐滴滴加盐酸的过程中,产生的QX2气体的物质的量与滴加的盐酸体积关系如图所示:

由此可知,混合物甲的组成为
(4)使用下列装置再添加合适的药品,可以证明R和Q两种元素的非金属性强弱顺序,可供选择的药品为:①浓硫酸 ②稀硫酸 ③盐酸 ④Na2CO3固体 ⑤CaCO3⑥澄清石灰水 ⑦NaOH溶液

请选择装置丙、丁两处应该加入的药品代号:丙
您最近半年使用:0次
2023-03-09更新
|
266次组卷
|
2卷引用:辽宁省五校联考2022-2023学年高一上学期期末考试化学试题
9 . X、Y、Z、M、Q为前四周期元素,原子序数依次增大。X的族序数等于其周期数,Y和M同族,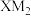 分子和
分子和 分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是
分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是
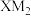 分子和
分子和 分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是
分子中X、Z均显最高价。Q是用途最广、用量最大的金属。下列说法正确的是A.一个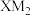 分子含1个 分子含1个 和2个 和2个 | B.X的氢氧化物能与NaOH溶液反应 |
| C.Y的气态氢化物沸点比M的气态氢化物低 | D.基态Q原子的价电子排布式为 |
您最近半年使用:0次
名校
10 . 短周期元素X、Y、Z、W、R原子序数依次增大,W原子次外层电子数比最外层电子数多2个,X与R同主族,其中部分元素的原子半径和主要化合价如下表所示:
请回答下列问题:
(1)W元素在元素周期表中的位置为_______ 。
(2)Y元素最高价氧化物水化物的溶液与Z的氧化物反应的离子方程式为_______ 。
(3)W、R元素最高价氧化物水化物的酸性较强的为_______ (用化学式表示);从原子结构角度解释原因_______ 。
(4)化合物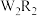 、
、 (所有原子均满足8电子结构)在工业生产中有广泛用途,
(所有原子均满足8电子结构)在工业生产中有广泛用途,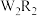 的结构式为
的结构式为_______ ;在一定条件下, 与
与 反应生成
反应生成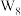 、
、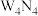 和一种仅由非金属元素组成的离子化合物,该离子化合物为
和一种仅由非金属元素组成的离子化合物,该离子化合物为_______ (填化学式)。
(5)化合物 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与
与 反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为_______ 。
| N | X | Y | Z | |
| 原子半径/pm | 75 | 71 | 186 | 143 |
| 主要化合价 | / | -1 | +1 | +3 |
(1)W元素在元素周期表中的位置为
(2)Y元素最高价氧化物水化物的溶液与Z的氧化物反应的离子方程式为
(3)W、R元素最高价氧化物水化物的酸性较强的为
(4)化合物
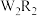 、
、 (所有原子均满足8电子结构)在工业生产中有广泛用途,
(所有原子均满足8电子结构)在工业生产中有广泛用途,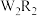 的结构式为
的结构式为 与
与 反应生成
反应生成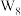 、
、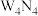 和一种仅由非金属元素组成的离子化合物,该离子化合物为
和一种仅由非金属元素组成的离子化合物,该离子化合物为(5)化合物
 可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。
可用作燃烧剂、推进剂中的氧化剂、高温金属的切割油等。 与
与 反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
反应生成两种单质(其中一种为黄绿色气体)和一种氢化物,则该反应的化学方程式为
您最近半年使用:0次



