名校
解题方法
1 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是_______ ,写出YM的电子式:_______ 。
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):_______ 。
(3)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是_______ 。
a.Ga位于元素周期表第四周期ⅣA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d.酸性:
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出 气体,同时生成
气体,同时生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为_______ 。
(4) 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
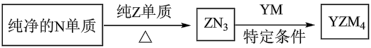
利用 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。
①其反应的化学方程式为_______ 。
②取样品a g,若实验测得氢气的体积为V mL(标准状态),则 样品纯度为
样品纯度为_______ (用代数式表示)。
(1)Y在周期表中的位置是
(2)N、X、Y、Z简单离子的半径由大到小的顺序(用对应离子符号表示):
(3)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温、耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是
a.Ga位于元素周期表第四周期ⅣA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
d.酸性:

②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出
 气体,同时生成
气体,同时生成 和
和 ,写出该反应的化学方程式为
,写出该反应的化学方程式为(4)
 是有机合成的重要还原剂,其合成路线如图所示。
是有机合成的重要还原剂,其合成路线如图所示。
利用
 遇水反应生成的氢气的体积测定
遇水反应生成的氢气的体积测定 样品纯度。
样品纯度。①其反应的化学方程式为
②取样品a g,若实验测得氢气的体积为V mL(标准状态),则
 样品纯度为
样品纯度为
您最近半年使用:0次
名校
2 . 已知短周期元素M、N、X、Y、Z分布在三个周期,N、X最外层电子数相同,Z原子序数大于X,其中Z的简单离子半径在同周期中最小,X单质极易与常见无色无味液态物质发生置换反应且做氧化剂,在短周期中Y的最高价氧化物对应水化物的碱性最强。回答下列问题:
(1)Y在周期表中的位置是_____ ;N的简单离子的核外电子排布示意图为_____ 。
(2)用电子式表示化合物YN的形成过程:_____ 。
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:_____ 。
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是_____ (填字母)。
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:_____ 。
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。
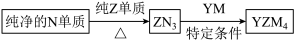
特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为_____ 。
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是_____ (填编号)。
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为_____ (用代数式表示)。
(1)Y在周期表中的位置是
(2)用电子式表示化合物YN的形成过程:
(3)在YZO2与YX的混合液中,通入足量CO2,是工业制取Y3ZX6的一种方法,写出该反应的化学方程式:
(4)镓(31Ga)的化合物氮化镓(GaN)和砷化镓(GaAs)作为第三代半导体材料,具有耐高温耐高电压等特性,随着5G技术的发展,它们的商用价值进入“快车道”。
①下列有关说法正确的是
a.Ga位于元素周期表第四周期IVA族
b.Ga为门捷列夫预言的“类铝”
c.Ga的最高价氧化物对应水化物的碱性比Z元素最高价氧化物对应水化物的碱性强
②废弃的含GaAs的半导体材料可以用浓硝酸溶解,放出NO2气体,同时生成H3AsO4和Ga(NO3)3,写出该反应的化学方程式:
(5)YZM4是有机合成的重要还原剂,其合成路线如图所示。

特定条件利用YZM4遇水反应生成的氢气的体积测定YZM4样品纯度。
①YZM4遇水反应的化学方程式为
②现设计如图四种装置测定YZM4样品的纯度(假设杂质不参与反应)。

从简约性、准确性考虑,最适宜的方案是
③取样品ag,若实验测得氢气的体积为VmL(标准状态),则YZM4样品纯度为
您最近半年使用:0次
解题方法
3 . X、Y、Z、M为原子序数依次增大的短周期主族元素,这四种元素原子的最外层电子数之和等于12。A~G是由上述四种元素组成的化合物,其转化关系如图所示,其中C是一种强碱,焰色试验呈黄色。

回答下列问题:
(1)元素Y在元素周期表中的位置是___________ 。
(2)Y、Z、M三种元素的原子半径由大到小的顺序为___________ (用元素符号表示)。
(3)能说明Z的非金属性强于Y的依据是___________ (写一点即可)。
(4)写出反应①的离子方程式___________ 。
(5)去除A溶液中混有的少量B的方法是___________ 。
(6)3.9g固体D与足量F反应转移的电子数目为___________ 。
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是___________ (填标号)。
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng

回答下列问题:
(1)元素Y在元素周期表中的位置是
(2)Y、Z、M三种元素的原子半径由大到小的顺序为
(3)能说明Z的非金属性强于Y的依据是
(4)写出反应①的离子方程式
(5)去除A溶液中混有的少量B的方法是
(6)3.9g固体D与足量F反应转移的电子数目为
(7)下列实验方案中,能测定出物质A和B的混合物中B的质量分数的是
a.取mg混合物充分加热,质量减少ng
b.取mg混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得到ng固体
c.取mg混合物与足量NaOH溶液充分反应,得到ng溶液
d.取mg混合物与足量稀硫酸充分反应,逸出气体经干燥后用碱石灰吸收,质量增加ng
您最近半年使用:0次
名校
解题方法
4 . a、b、c、d、e为五种短周期主族元素,原子序数依次递增。下图是a~e五种元素的单质及其化合物(或其溶液)的转化关系。已知A为金属单质,E为淡黄色固体,B、C、D是非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒,化合物F通常状况下呈气态。请回答下列问题:

(1)d在元素周期表中的位置位于___________ , 的电子式为
的电子式为___________ 。
(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(3) 可在呼吸面具中作为氧气来源,假设每人每分钟消耗
可在呼吸面具中作为氧气来源,假设每人每分钟消耗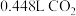 (标准状况),且所需的
(标准状况),且所需的 全部由
全部由 来提供,则某消防员工作1小时所需
来提供,则某消防员工作1小时所需 的质量为
的质量为___________ g。
(4)b、c、d元素中,原子半径由小到大的顺序是___________ (填元素符号);c、d、e元素分别形成的简单离子中离子半径最小的是___________ (填离子符号)。
(5)b和e两元素相比较,非金属性较强是___________ (填元素符号),可以证明该结论的是___________ 。
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价

(1)d在元素周期表中的位置位于
 的电子式为
的电子式为(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是
(3)
 可在呼吸面具中作为氧气来源,假设每人每分钟消耗
可在呼吸面具中作为氧气来源,假设每人每分钟消耗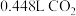 (标准状况),且所需的
(标准状况),且所需的 全部由
全部由 来提供,则某消防员工作1小时所需
来提供,则某消防员工作1小时所需 的质量为
的质量为(4)b、c、d元素中,原子半径由小到大的顺序是
(5)b和e两元素相比较,非金属性较强是
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价
您最近半年使用:0次
解题方法
5 . 下表是元素周期表中的一部分:
根据a~i在周期表中的位置,回答下列问题:
(1)a~i的单质中,化学性质最不活泼的是______ (填化学式,下同),氧化性最强的是_______ 。
(2)a与b形成的简单化合物的电子式是___________ 。
(3)最高价氧化物对应的水化物酸性最强的是___________ (填化学式);e、f的最高价氧化物对应的水化物之间反应的离子方程式为________________________ 。
(4)g的最高价氧化物对应水化物的浓溶液可与Cu在加热时反应,反应的化学方程式为___________________ ,该反应中氧化剂与还原剂的物质的量之比为_________ 。
(5)如图表示由c、g元素组成的两种气体分子在一定 条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______________________ 。
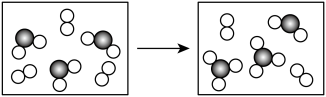
I A | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
| 第1周期 | a | |||||||
| 第2周期 | b | c | d | |||||
| 第3周期 | e | f | g | h | i | |||
(1)a~i的单质中,化学性质最不活泼的是
(2)a与b形成的简单化合物的电子式是
(3)最高价氧化物对应的水化物酸性最强的是
(4)g的最高价氧化物对应水化物的浓溶液可与Cu在加热时反应,反应的化学方程式为
(5)如图表示由c、g元素组成的两种气体分子在一定 条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

您最近半年使用:0次
解题方法
6 . 已知A、B、C、D、E、F是原子序数依次增大的六种短周期主族元素,A与B能形成 和
和 两种常见共价化合物,A与C位于相邻主族,B与E位于同一主族,D是同周期中简单离子半径最小的元素。回答下列问题:
两种常见共价化合物,A与C位于相邻主族,B与E位于同一主族,D是同周期中简单离子半径最小的元素。回答下列问题:
(1)C在元素周期表中的位置是_______ 。
(2)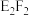 的电子式为
的电子式为_______ 。
(3)D的最高价氧化物对应的水化物与F的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(4) 和
和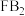 是市场上较好的消毒剂,等质量的
是市场上较好的消毒剂,等质量的 和
和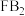 分别与足量二氧化硫反应时,消耗二氧化硫的质量之比为
分别与足量二氧化硫反应时,消耗二氧化硫的质量之比为_______ 。
(5)已知W、X、Y、Z四种物质中均含有上述元素中的某一种,M、X为单质,其余均为化合物,它们之间存在如图所示的转化关系(反应条件略)。
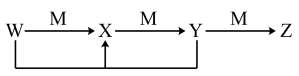
①Z的化学式为_______ 。
②上述五种物质所含的元素中,原子半径最大的是_______ (填元素符号)。
③C元素形成的单质与M在海水中可以形成原电池,其正极的电极反应式为_______ 。
 和
和 两种常见共价化合物,A与C位于相邻主族,B与E位于同一主族,D是同周期中简单离子半径最小的元素。回答下列问题:
两种常见共价化合物,A与C位于相邻主族,B与E位于同一主族,D是同周期中简单离子半径最小的元素。回答下列问题:(1)C在元素周期表中的位置是
(2)
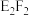 的电子式为
的电子式为(3)D的最高价氧化物对应的水化物与F的最高价氧化物对应的水化物反应的离子方程式为
(4)
 和
和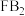 是市场上较好的消毒剂,等质量的
是市场上较好的消毒剂,等质量的 和
和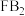 分别与足量二氧化硫反应时,消耗二氧化硫的质量之比为
分别与足量二氧化硫反应时,消耗二氧化硫的质量之比为(5)已知W、X、Y、Z四种物质中均含有上述元素中的某一种,M、X为单质,其余均为化合物,它们之间存在如图所示的转化关系(反应条件略)。

①Z的化学式为
②上述五种物质所含的元素中,原子半径最大的是
③C元素形成的单质与M在海水中可以形成原电池,其正极的电极反应式为
您最近半年使用:0次
名校
7 . 短周期元素W、X、Y、Z、Q、R的原子序数依次增大,c、d、e、f、h是由这些元素组成的二元化合物,自然界中硬度最大的单质和a都由X组成,b由W、Y、Q三种元素组成,d能使品红溶液褪色,是液体,上述物质的转化关系如下图所示(个别产物略去)。请回答下列问题:
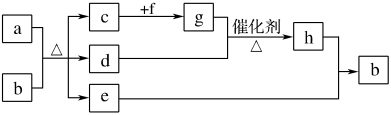
(1)R在元素周期表中的位置:_______ 。
(2)化合物f的电子式:_______ 该化合物存在的化学键种类是:_______ ;化合物c的结构式:_______ 。
(3)用电子式表示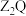 的形成过程为
的形成过程为_______ 。
(4)W、Y、Z、Q四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为_______ 、_______ ,这两种酸式盐相互反应的离子方程式为_______ 。
(5)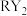 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过 和
和 在稀硫酸酸化的环境中反应制得气体
在稀硫酸酸化的环境中反应制得气体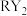 ,试写出该反应的离子反应方程式并配平:
,试写出该反应的离子反应方程式并配平:_______ 。
(6)在100mL 18mol/L b的浓溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解,产生的气体在标准状况下的体积可能是_______(填序号)。

(1)R在元素周期表中的位置:
(2)化合物f的电子式:
(3)用电子式表示
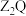 的形成过程为
的形成过程为(4)W、Y、Z、Q四种元素可以形成两种酸式盐(均由四种元素组成),这两种酸式盐的化学式分别为
(5)
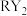 是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过
是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过 和
和 在稀硫酸酸化的环境中反应制得气体
在稀硫酸酸化的环境中反应制得气体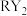 ,试写出该反应的离子反应方程式并配平:
,试写出该反应的离子反应方程式并配平:(6)在100mL 18mol/L b的浓溶液中加入过量的铜片,加热使之充分反应,铜片部分溶解,产生的气体在标准状况下的体积可能是_______(填序号)。
| A.7.32L | B.6.72L | C.20.16L | D.30.24L |
您最近半年使用:0次
解题方法
8 . X、Y、Z为短周期主族元素,且原子序数依次增大,Y、Z位于相邻主族,这三种元素形成的化合物甲为 ,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
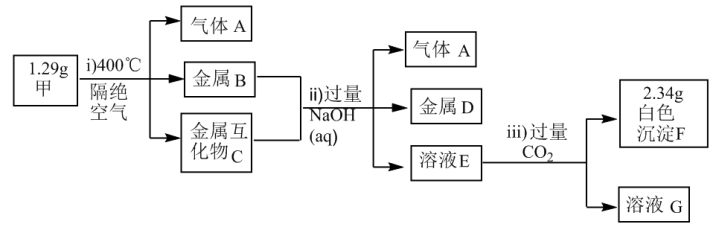
已知:金属互化物是由两种或两种以上的金属组成,其组成金属具有单质的性质。
回答下列问题:
(1)Y在元素周期表中的位置是___________ 。
(2)F受热分解生成两性氧化物,则F与烧碱溶液反应的离子方程式是___________ 。
(3)若溶液G中只有一种溶质,则该溶液中阴离子的浓度由大到小的顺序是___________ 。
(4)1.29g甲在隔绝空气的条件下,加热到400℃,完全分解产生的气体A的体积(标准状况)为___________ L。
 ,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
,化合物甲受热分解产生的物质及后续有关物质的转化关系如下图所示:
已知:金属互化物是由两种或两种以上的金属组成,其组成金属具有单质的性质。
回答下列问题:
(1)Y在元素周期表中的位置是
(2)F受热分解生成两性氧化物,则F与烧碱溶液反应的离子方程式是
(3)若溶液G中只有一种溶质,则该溶液中阴离子的浓度由大到小的顺序是
(4)1.29g甲在隔绝空气的条件下,加热到400℃,完全分解产生的气体A的体积(标准状况)为
您最近半年使用:0次
解题方法
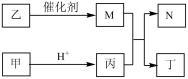
9 . X、Y、Z、W 是原子序数依次增大的短周期元素,Y 和W同主族,且X、Z原子序数之和是Y、W原子序数之和的 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
(1)W在元素周期表中的位置是_______________________ 。
(2)Y、Z、W的离子半径由大到小的顺序为__________ (用元素符号表示)。
(3)写出乙的电子式_____________ ,M 的结构式_____________________ 。
(4)丁与H2S相比沸点高的是_______ (用化学式表示);原因是_______________ 。
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理______________ (填“相同”或“不相同”);N使酸性KMnO4溶液褪色的离子方程式为 ________________________ 。
 。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
。甲、乙、丙、丁、N是由这些元素组成的二元化合物,M 是这四种元素中某种元素对应的单质,乙和丁的组成元素相同,且乙是一种“绿色氧化剂”,化合物N是具有漂白性的气体(常温下),能使品红溶液褪色。上述物质间的转化关系如图所示(部分反应物和生成物省略)。
(1)W在元素周期表中的位置是
(2)Y、Z、W的离子半径由大到小的顺序为
(3)写出乙的电子式
(4)丁与H2S相比沸点高的是
(5)N 与乙烯均能使酸性 KMnO4溶液褪色,原理
您最近半年使用:0次
名校
解题方法
10 . A~H均为短周期元素,A~F在元素周期表中的相对位置如图1所示,G与其他七种元素不在同一周期,H是短周期中原子半径最大的主族元素。由B、G构成的最简单化合物常作为氮肥工业和纯碱工业的原料。由上述某些元素组成的物质甲~戊的转化关系如图2所示。

已知图2中反应①是复分解反应,生成物中水已略去。请回答下列问题:
(1)上述元素组成的单质中,硬度最大的是_________________ (填该物质名称)。
(2)若戊是含有18电子的双原子分子,则丙的电子式为________________ ;在①中制取气体丙的化学方程式为_______________________________________________ 。
(3)若甲的水溶液呈碱性,丙的凝胶经干燥脱水后,常用作干燥剂,写出甲的一种用途:_____________________________ 。
(4)如果图2中反应①是置换反应,戊是单质,则戊不可能是_____________ 。 (填序母序号)
A、O2 B、Cl2 C、H2 D、N2

已知图2中反应①是复分解反应,生成物中水已略去。请回答下列问题:
(1)上述元素组成的单质中,硬度最大的是
(2)若戊是含有18电子的双原子分子,则丙的电子式为
(3)若甲的水溶液呈碱性,丙的凝胶经干燥脱水后,常用作干燥剂,写出甲的一种用途:
(4)如果图2中反应①是置换反应,戊是单质,则戊不可能是
A、O2 B、Cl2 C、H2 D、N2
您最近半年使用:0次



