1 . Ⅰ. 元素X、Y、Z、W、Q在元素周期表中的相对位置如下图所示。
(1)元素X在周期表中的位置是第_______ 周期,第_______ 族。
(2)五种元素中离子半径最小的是_______ 。
Ⅱ. 下图是部分短周期主族元素原子半径与原子序数的关系。

(3)X的元素符号:_______ 。
(4)Y与Z形成的是_______ 化合物。(填“离子”或“共价”)
(5)上述元素的最高价含氧酸中酸性最强的是_______ (填化学式)。
Ⅲ.(6)下列关于元素及其化合物性质的判断中,正确的是_______ (填序号)
A. 元素甲的氢氧化物只有碱性,而元素乙的氢氧化物具有两性,所以金属性:甲>乙
B. 元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
C. 金属元素 、
、 能分别形成+2、+3价离子,所以氧化性:
能分别形成+2、+3价离子,所以氧化性: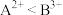
D. 因为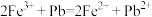 ,所以金属性:
,所以金属性:
E. 因为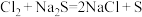 ,所以非金属性:
,所以非金属性:
F. 因为水溶液的酸性: ,所以非金属性:
,所以非金属性:
G. 是一元酸,而
是一元酸,而 是二元酸,所以酸性:
是二元酸,所以酸性: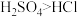
Ⅳ.(7)甲同学查阅资料知:氨气( )的分解温度在850℃以上,甲烷(
)的分解温度在850℃以上,甲烷( )的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
)的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):_______ 。
| X | Y | ||||
| Z | W | Q |
(2)五种元素中离子半径最小的是
Ⅱ. 下图是部分短周期主族元素原子半径与原子序数的关系。

(3)X的元素符号:
(4)Y与Z形成的是
(5)上述元素的最高价含氧酸中酸性最强的是
Ⅲ.(6)下列关于元素及其化合物性质的判断中,正确的是
A. 元素甲的氢氧化物只有碱性,而元素乙的氢氧化物具有两性,所以金属性:甲>乙
B. 元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
C. 金属元素
 、
、 能分别形成+2、+3价离子,所以氧化性:
能分别形成+2、+3价离子,所以氧化性: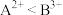
D. 因为
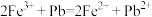 ,所以金属性:
,所以金属性:
E. 因为
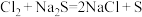 ,所以非金属性:
,所以非金属性:
F. 因为水溶液的酸性:
 ,所以非金属性:
,所以非金属性:
G.
 是一元酸,而
是一元酸,而 是二元酸,所以酸性:
是二元酸,所以酸性: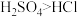
Ⅳ.(7)甲同学查阅资料知:氨气(
 )的分解温度在850℃以上,甲烷(
)的分解温度在850℃以上,甲烷( )的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
)的分解温度是655℃,据此得出结论:N元素的非金属性强于C元素。乙同学对此结论持怀疑态度,甲同学通过实验间接证明了自己的结论。你认为甲同学的实验方案是(请结合离子方程式简要说明):
您最近半年使用:0次
名校
2 . 有四种短周期元素,相关信息如下表。
请根据表中信息回答:
(1)A在周期表中位于第_______ 周期第_______ 族。
(2)用电子式表示B与C形成化合物的过程:_______ 。
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是_______ (填化学式)。
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是_______ 。
a.其单质在常温下呈固态
b. 既有氧化性又有还原性
既有氧化性又有还原性
c.最高价氧化物对应的水化物的化学式为
d.非金属性比Cl元素的强
| 元素 | 相关信息 |
| A | 气态氢化物极易溶于水,且其水溶液显碱性 |
| B | 单质在焰色试验中显黄色 |
| C | 单质是淡黄绿色气体,可用于自来水消毒 |
| D | -2价阴离子的电子层结构与Ar原子相同 |
(1)A在周期表中位于第
(2)用电子式表示B与C形成化合物的过程:
(3)在元素C与D的最高价氧化物对应的水化物中,酸性较强的是
(4)已知硒(Se)与D同主族,且位于D下一个周期,根据硒元素在元素周期表中的位置推测,硒可能具有的性质是
a.其单质在常温下呈固态
b.
 既有氧化性又有还原性
既有氧化性又有还原性c.最高价氧化物对应的水化物的化学式为

d.非金属性比Cl元素的强
您最近半年使用:0次
名校
3 . 元素周期表是学习化学的重要工具。回答下列问题:
(1)硅元素原子核外有______ 种能量不同的电子,有______ 种运动状态不同的电子,写出其最外层电子的电子排布式__________________ 。
(2) 的空间构型和
的空间构型和 相同,写出
相同,写出 的电子式:
的电子式:__________________ 。
(3)部分短周期元素化合价与原子序数的关系可用图示表示。

①元素X在元素周期表中的位置是__________________ 。
②写出元素Y和Z的最高价氧化物对应水化物反应的离子方程式:______________________________ 。
③第三周期主族元素中非金属性最强的两种元素是____________ 和____________ (填元素符号),用一个化学方程式说明这两种元素非金属性的相对强弱:______________________________ 。
(4)第三周期元素的原子所形成的简单离子中:还原性最弱的阴离子是____________ ;氧化性最强的阳离子是____________ 。
(5)写出两种W的含氧酸的化学式____________ 、____________ ,设计一种实验方案比较两种酸的酸性强弱,写出反应的化学方程式:________________________ 。
(1)硅元素原子核外有
(2)
 的空间构型和
的空间构型和 相同,写出
相同,写出 的电子式:
的电子式:(3)部分短周期元素化合价与原子序数的关系可用图示表示。

①元素X在元素周期表中的位置是
②写出元素Y和Z的最高价氧化物对应水化物反应的离子方程式:
③第三周期主族元素中非金属性最强的两种元素是
(4)第三周期元素的原子所形成的简单离子中:还原性最弱的阴离子是
(5)写出两种W的含氧酸的化学式
您最近半年使用:0次
解题方法
4 . 有A、B、C、D、E、F六种元素,试按下述所给条件推断:①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,原子半径A>B>C ②D、E、F是同主族非金属元素,它们与氢化合可生成气态氢化物HD、HE、HF,在室温时,E的单质是液体是液体,F的单质是固体;D是除氢外原子半径最小的元素。
(1)A的名称是_________ ,B、C的简单离子的氧化性强弱(用离子符号表示)___________ ,C 的原子结构示意图是_____________ 。
(2)气态氢化物HD、HE、HF的稳定性由强到弱是(用分子式表示)_________ ,D、E、F离子的还原性由强到弱是(用离子符号表示)____________ 。
(3)A元素与E元素形成化合物的化学式是___________ 。
(4)下列表述中能证明E的单质氧化性强于F单质的事实是________ 。
A.E单质的熔点小于F单质的熔点
B.E单质能将F从其可溶性盐中置换出来
c.一定条件下E和F的单质都能与A的单质反应
(5)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是______ (填物质化学式,下同),酸性最强的是________ ,气体氢化物最稳定的是__________ 。
(6)将C的最高价氧化物对应的水化物既能与A的最高价氧化物对应的水化物反应,也能与E的最高价氧化物对应的水化物反应。分别写出其反应的离子方程式是_______________ ;_______________ 。
(1)A的名称是
(2)气态氢化物HD、HE、HF的稳定性由强到弱是(用分子式表示)
(3)A元素与E元素形成化合物的化学式是
(4)下列表述中能证明E的单质氧化性强于F单质的事实是
A.E单质的熔点小于F单质的熔点
B.E单质能将F从其可溶性盐中置换出来
c.一定条件下E和F的单质都能与A的单质反应
(5)在上述七种元素中,最高价氧化物对应的水化物碱性最强的是
(6)将C的最高价氧化物对应的水化物既能与A的最高价氧化物对应的水化物反应,也能与E的最高价氧化物对应的水化物反应。分别写出其反应的离子方程式是
您最近半年使用:0次
名校
5 . X、Y、Z、W为原子序数依次增大的短周期主族元素。X分别与Y、Z、W结合形成质子数相同的甲、乙、丙三种分子。丁为无色气体,遇空气变红棕色;丙的水溶液可刻蚀玻璃。上述物质有如图转化关系如图所示。
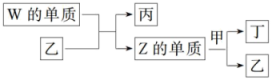
(1)Y、Z元素分别为_______ 、_______ (填元素符号)
(2)丙的水溶液刻蚀玻璃的化学反应方程式是_______
(3)X与Y还可以结合形成Y2X4分子,Y2X4的电子式为_______ ,Y的化合价为_______ 。实验室可用次氯酸钠溶液与甲反应制备Y2X4,反应的化学方程式为_______ 。
(4)下列关于元素及其化合物性质的判断中,正确的是_______ (填序号)
A.元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
B.金属元素A、B能分别形成+2、+3价离子,所以氧化性:A2+<B3+
C.因为 ,所以金属性:Pb>Fe
,所以金属性:Pb>Fe
D.因为 ,所以非金属性:Cl>S
,所以非金属性:Cl>S
E.因为水溶液的酸性:HmA>HnB,所以非金属性:A>B
F.HCl是一元酸,而H2SO4是二元酸,所以酸性:H2SO4>HCl
(5)某同学查阅资料知:甲的分解温度在850℃以上,甲烷(CH4)的分解温度是655℃,据此得出结论:Y元素的非金属性强于碳元素。该同学通过实验间接证明了自己的结论。你认为该同学的实验方案是(请结合离子方程式简要说明):_______ 。

(1)Y、Z元素分别为
(2)丙的水溶液刻蚀玻璃的化学反应方程式是
(3)X与Y还可以结合形成Y2X4分子,Y2X4的电子式为
(4)下列关于元素及其化合物性质的判断中,正确的是
A.元素甲最外层只有一个电子,而乙最外层有两个电子,所以金属性:甲>乙
B.金属元素A、B能分别形成+2、+3价离子,所以氧化性:A2+<B3+
C.因为
 ,所以金属性:Pb>Fe
,所以金属性:Pb>FeD.因为
 ,所以非金属性:Cl>S
,所以非金属性:Cl>SE.因为水溶液的酸性:HmA>HnB,所以非金属性:A>B
F.HCl是一元酸,而H2SO4是二元酸,所以酸性:H2SO4>HCl
(5)某同学查阅资料知:甲的分解温度在850℃以上,甲烷(CH4)的分解温度是655℃,据此得出结论:Y元素的非金属性强于碳元素。该同学通过实验间接证明了自己的结论。你认为该同学的实验方案是(请结合离子方程式简要说明):
您最近半年使用:0次
名校
解题方法
6 . 部分短周期主族元素的原子半径和主要化合价的关系如图所示,其中E、G、T位于同一周期。回答下列问题:

(1)B位于第_______ 周期第______ 族。
(2)FDB的电子式为_______ ;T的原子结构示意图为_______ 。
(3)设计简单实验证明D的非金属性比C的强:________ 。
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是_______ 。
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ;上述非金属元素的简单氢化物中,沸点最高的是_______ ,还原性最强的是_______ 。
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为_______ 。

(1)B位于第
(2)FDB的电子式为
(3)设计简单实验证明D的非金属性比C的强:
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为
您最近半年使用:0次
2023-10-27更新
|
166次组卷
|
2卷引用:湖南省炎德·英才·名校联考联合体2023-2024学年高三上学期第三次联考化学试题
7 . 现有原子序数依次增大的短周期主族元素P、Q、X、Y、Z、W。P元素的一种核素无中子,元素Q的最外层电子数是电子层数的2倍,Y原子是其所在周期中半径最大的原子,元素Z的最外层电子数是K层电子数的3倍,X能与Y可以形成一种淡黄色固体M。
(1)写出元素Q在元素周期表中的位置_______ 。
(2)写出元素P与元素X形成的18e-分子的电子式_______ 。
(3)研究发现M具有强氧化性,Z的一种氧化物具有较强的还原性,可相互反应。写出该反应的化学方程式:_______ 。
(4)为了证明非金属性W>Z,某小组设计如图装置探究元素非金属性的变化规律。C中装有Y2Z溶液,B中装有YWX3固体。A中试剂为_______ (填化学式)浓溶液,C中发生反应的离子方程式为_______ 。

(5)元素P与元素Q形成的一种物质Q2P4使溴水褪色,写出褪色过程中发生的化学反应方程式:_______ 。
(1)写出元素Q在元素周期表中的位置
(2)写出元素P与元素X形成的18e-分子的电子式
(3)研究发现M具有强氧化性,Z的一种氧化物具有较强的还原性,可相互反应。写出该反应的化学方程式:
(4)为了证明非金属性W>Z,某小组设计如图装置探究元素非金属性的变化规律。C中装有Y2Z溶液,B中装有YWX3固体。A中试剂为

(5)元素P与元素Q形成的一种物质Q2P4使溴水褪色,写出褪色过程中发生的化学反应方程式:
您最近半年使用:0次
名校
解题方法
8 . 已知A、B、C、D为原子序数依次增大的短周期元素,E为地壳中含量最高的过渡金属元素,A与D同主族,B与C同周期,且C与D的原子序数之和为20,C单质能与无色无味液体m反应置换出B单质,D单质也能与m反应置换出A单质,A、B、C均能与D形成离子化合物,下列说法不正确 的是
| A.B、E两元素的形成的化合物都为黑色固体 | B.B、D形成的离子化合物可能含有共价键 |
| C.D的单质只有还原性,没有氧化性 | D.A、B、C分别与D形成的化合物水溶液均显碱性 |
您最近半年使用:0次
2020-10-10更新
|
461次组卷
|
3卷引用:辽宁省实验中学东戴河校区2021届高三上学期第一次月考化学试题
名校
解题方法
9 . 短周期主族元素X、Y、Z、W的原子序数依次增大。在如图所示的物质转化关系中,p、q、m、n分别是元素W、X、Y、Z的气体单质,p和s均为有色气体,v的水溶液呈碱性。常温下,0.1mol·L-1t溶液与0.1mol·L−1u溶液的pH均为1。下列说法不正确的是( )
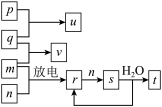

| A.Y、W的最高价氧化物对应的水化物均为强酸 |
| B.元素的非金属性:Z>Y>X,原子半径:X<Z<Y |
| C.s溶于水的反应中,氧化剂与还原剂的物质的量之比为1:2 |
| D.v只有还原性,r既有还原性又有氧化性 |
您最近半年使用:0次
10 . 短周期主族元素R、X、Y、Z的原子序数依次增大,其中,X的原子半径在短周期元素中最大,Y的单质常作制造半导体的材料,R的最高价氧化物对应的水化物具有强氧化性、不稳定性和挥发性,Z的游离态常出现在火山喷口处。下列说法正确的是
| A.简单氢化物的还原性:Y>R>Z |
| B.最高价氧化物对应水化物的酸性:Y>Z |
| C.X的单质能与水发生置换反应 |
| D.常温常压下R的氧化物都是无色气体 |
您最近半年使用:0次



