1 . X、Y、Z、W四种常见元素,其中X\、Y、Z为短周期元素,W为过渡元素,它们的相关信息如表:
回答下列问题:
(1)W在周期表的位置为_________ ,W(OH)2在空气中不稳定,极易被氧化反应的化学方程式为_________________________________________ 。
(2)X的简单阴离子的结构示意图为___________________ ;X的最高价氧化物对应水化物的水溶液与Y的氧化物反应的离子方程式为____________________________ 。
(3)Z的氧化物在通讯领域的用途是___________________ ,工业上制备Z的单质的化学反应方程式为 ___________________________________ 。
(4)YX3固体在熔融状态下不导电,则YX3固体中存在__________ 键;在50 mL l mol·L-1的YX3溶液中逐滴加入0.5 mol·L-1的NaOH溶液,得到1.56 g沉淀,则加入NaOH溶液的体积可能有________ 种情况。
| 原子或分子相关信息 | 单质及其化合物相关信息 | |
| X | ZX4分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种高温材料 |
| Z | Z原子的最外层电子数是次外层电子数的 | Z广泛存在于无机非金属材料中,其单质是制取大规模集成电路的主要原料 |
| W | W原子的最外层电子数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)W在周期表的位置为
(2)X的简单阴离子的结构示意图为
(3)Z的氧化物在通讯领域的用途是
(4)YX3固体在熔融状态下不导电,则YX3固体中存在
您最近半年使用:0次
解题方法
2 . 已知由短周期常见元素形成的纯净物A、B、C、D转化关系如图l所示,物质A与物质B之间的反应不在溶液中进行。
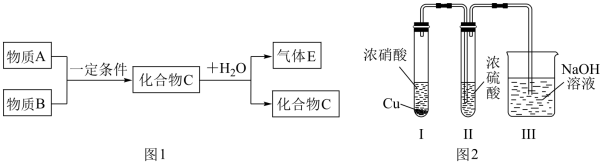
请回答下列问题:
(1)若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是__________________ ;(填化学式)
②化合物C的电子式为__________ ;化合物D中所含化学键的类型是_________ 。
(2)若A为非金属单质,B是化合物,C是红棕色气体,D是一元强酸.
①B为_________________ (填化学式)。
②化合物C与水反应时的化学方程式为________________ ,其氧化剂与还原剂的质量比为_______________ 。
(3)某同学用图2装置完成有关探究实验。
I.试管中(试管中的药品分别为浓硝酸,铜片)发生反应的离子方程式为:_________________________ 。
II.试管中观察到_______________________ 的实验现象时,说明NO2能溶于浓硫酸中,浓硫酸不能干燥NO2。Ⅲ.装置Ⅲ的用途是:____________________________

请回答下列问题:
(1)若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是
②化合物C的电子式为
(2)若A为非金属单质,B是化合物,C是红棕色气体,D是一元强酸.
①B为
②化合物C与水反应时的化学方程式为
(3)某同学用图2装置完成有关探究实验。
I.试管中(试管中的药品分别为浓硝酸,铜片)发生反应的离子方程式为:
II.试管中观察到
您最近半年使用:0次
名校
解题方法
3 . V、W、X、Y、Z是中学常见的五种化合物,其中V、W、X、Z均由两种元素组成,X是一种常见的大气污染性气体,V、Y、W都既能与酸反应,又能与强碱溶液反应。它们之间的反应关系如下图:
(1)写出W物质的一种用途:____________ 。
(2)制取固体V的一种方法(用化学方程式表示):___________ 。
(3)写出V与足量NaOH溶液反应的化学方程式:___________ 。
(4)写出X与Z反应生成M的化学方程式:_____________ 。

(1)写出W物质的一种用途:
(2)制取固体V的一种方法(用化学方程式表示):
(3)写出V与足量NaOH溶液反应的化学方程式:
(4)写出X与Z反应生成M的化学方程式:
您最近半年使用:0次
9-10高三·福建福州·阶段练习
4 . 已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6。M与其他物质的转化关系如下(部分产物已略去):
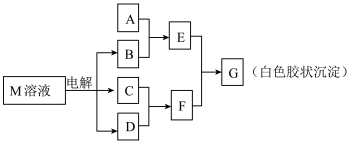
(1)工业电解M溶液的化学方程式为___________________________ 。
(2)若A是X、Y同周期的一种常见金属,则A元素在周期表中的位置是_________ ,写出A与B溶液反应的化学方程式是_____________________ 。
(3)若A是一种常见酸性氧化物,可用于制造光导纤维,则A元素原子结构示意图为______________ ,写出E与F反应的离子方程式是____________________ 。
(4)举例说明M物质的一种用途____________________ 。

(1)工业电解M溶液的化学方程式为
(2)若A是X、Y同周期的一种常见金属,则A元素在周期表中的位置是
(3)若A是一种常见酸性氧化物,可用于制造光导纤维,则A元素原子结构示意图为
(4)举例说明M物质的一种用途
您最近半年使用:0次
2010·山西太原·一模
5 . 有短周期元素A、B、C、D、E,已知:
①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜
② B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍
③ E与A同周期,C、D、E三种元素形成的单质或化合物可发生如下图所示的反应。
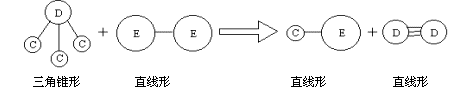
请用化学式或相应的符号回答下列问题:
(1)写出A元素最高价氧化物与NaOH溶液反应的离子方程式__________ ;
(2)B元素在元素周期表第_____ 周期第____ 族;
B的固态氧化物的晶体类型是_____ ;
(3)D元素的原子结构示意图是:_____________________ ;
(4)B元素与E元素的最高价氧化物的水化物的酸性强弱_____ >_______ ;
(5)请用化学方程式表示E元素的单质在工业上的一种重要用途:____ 。
①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜
② B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍
③ E与A同周期,C、D、E三种元素形成的单质或化合物可发生如下图所示的反应。

请用化学式或相应的符号回答下列问题:
(1)写出A元素最高价氧化物与NaOH溶液反应的离子方程式
(2)B元素在元素周期表第
B的固态氧化物的晶体类型是
(3)D元素的原子结构示意图是:
(4)B元素与E元素的最高价氧化物的水化物的酸性强弱
(5)请用化学方程式表示E元素的单质在工业上的一种重要用途:
您最近半年使用:0次
名校
解题方法
6 . 下图是部分短周期元素的常见化合价与原子序数的关系图:
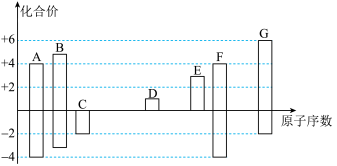
请回答下列问题:
(1)AB-离子与__________ 互为等电子体,lmolAB-离子含有___________ molπ键。
(2)用电子式表示D2G的形成过程________________________ 。
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器______________________________ ;
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时__________________________
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。
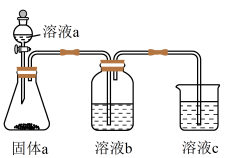
①溶液a和b分别为________________ ,________________ 。
②溶液c中的离子方程式为________________________________________________ 。
③请从原子结构的角度解释非金属性B>A的原因______________________________ 。

请回答下列问题:
(1)AB-离子与
(2)用电子式表示D2G的形成过程
(3)由C、E、G三种元素的某盐用途广泛,请用离子方程式表示下列过程:
①该盐可做泡沫灭火器
②向该盐溶液中加入Ba(OH) 2至沉淀物质的量最大时
(4)某同学设计实验证明A、B、F的非金属性强弱关系。(其中溶液b和溶液c均为足量)。

①溶液a和b分别为
②溶液c中的离子方程式为
③请从原子结构的角度解释非金属性B>A的原因
您最近半年使用:0次
解题方法
7 . 短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素电子层数之和是5。A、B两元素原子最外层电子数之和等于C元素原子最外层电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍,A与D可以形成原子个数比分别为1∶1和2∶1的两种液态化合物;E单质用于净化水质。请回答:
(1)E的原子结构示意图是__________________ 。
下列可以验证C与D两元素非金属性强弱的实验事实是___________ (填写编号)。
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
(2)由A、B两种元素组成的最简单的化合物,写出其电子式____ 。
(3)均由A、B、C、D四种元素组成的某无机化合物,既可以与盐酸反应又可以与NaOH溶液反应,其化学式为______________________ 。
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式____________________________________ 。
②上述反应生成的两种碱继续作用,得到Fe3O4。写出该反应的化学方程式_____________ 。
(1)E的原子结构示意图是
下列可以验证C与D两元素非金属性强弱的实验事实是
A.比较这两种元素的气态氢化物的沸点
B.比较只有这两种元素所形成的化合物中的化合价
C.比较这两种元素的气态氢化物的稳定性
(2)由A、B两种元素组成的最简单的化合物,写出其电子式
(3)均由A、B、C、D四种元素组成的某无机化合物,既可以与盐酸反应又可以与NaOH溶液反应,其化学式为
(4)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程可简单表示如下:
①将化合物CA3通入等物质的量的FeSO4、Fe2(SO4)3的混合溶液中,生成两种碱,写出该反应过程的总的离子方程式
②上述反应生成的两种碱继续作用,得到Fe3O4。写出该反应的化学方程式
您最近半年使用:0次
2017-09-06更新
|
421次组卷
|
2卷引用:浙江省名校协作体2017-2018学年高二上学期考试化学试题
解题方法
8 . 现有部分元素的性质、用途与原子(或分子)结构如表所示:
(1)元素Y在 周期表中的位置第
周期表中的位置第_______ ,元素T的简单离子结构示意图_______ 。
(2)W、X、Z、T中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式_______ 。
(3)元素W与元素X、T可以分别形成多种核外电子总数为10的微粒,其中有四种微粒可以发生反应:甲 + 乙 丙 + 丁,该反应为:
丙 + 丁,该反应为:_______ 。
(4)元素X与元素W以原子个数比1∶2化合形成常用于火箭燃料的化合物戊,元素T和元素W以原子个数比为1∶1化合形成化合物己,戊与己能发生氧化还原反应,生成X单质和另一种液体化合物,写出该反应的化学方程式_______ 。
| 元素编号 | 元素性质与原子(或分子)结构 |
W | 周期表中原子半径最小的元素 |
X | 氢化物可与其最高价氧化物的水化物反应生成盐 |
Y | 一种核素在考古时常用来鉴定一些文物的年代 |
Z | M层比K层少1个电子 |
T | 存在两种同素异形体,其中一种可吸收紫外线 |
 周期表中的位置第
周期表中的位置第(2)W、X、Z、T中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式
(3)元素W与元素X、T可以分别形成多种核外电子总数为10的微粒,其中有四种微粒可以发生反应:甲 + 乙
 丙 + 丁,该反应为:
丙 + 丁,该反应为:(4)元素X与元素W以原子个数比1∶2化合形成常用于火箭燃料的化合物戊,元素T和元素W以原子个数比为1∶1化合形成化合物己,戊与己能发生氧化还原反应,生成X单质和另一种液体化合物,写出该反应的化学方程式
您最近半年使用:0次
解题方法
9 . 现有几种元素的性质或原子结构如下表:
(1)工业制备X单质反应的化学方程式_______________________________ ;
(2)画出T的离子结构示意图__________ ;
(3)写出实验室利用浓盐酸和二氧化锰制取单质Z的离子方程式______________________ ;
(4)由T和Y两种元素组成的一种阴阳离子个数比为1:2的过氧化物,其电子式为___________ 。写出该物质的一种用途__________________________________
(5)T、Z的最高价氧化物对应的水化物相互反应的离子方程式为___________________ 。
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成Ne原子电子层结构 |
| X | 短周期非金属,其最外层电子数是次外层电子数的一半 |
| Y | 其单质之一是空气中主要成分,最常见的助燃剂 |
| Z | 形成双原子单质分子,黄绿色气体 |
(2)画出T的离子结构示意图
(3)写出实验室利用浓盐酸和二氧化锰制取单质Z的离子方程式
(4)由T和Y两种元素组成的一种阴阳离子个数比为1:2的过氧化物,其电子式为
(5)T、Z的最高价氧化物对应的水化物相互反应的离子方程式为
您最近半年使用:0次
10 . A、B、C、D、E均为元素周期表中短周期元素,其原子序数依次递增.请结合下表信息回答问题:

(1)元素B和E形成的化合物的电子式为_____ ,该化合物含有_____ (填“离子键”或“共价键”).
(2)B的单质在A的单质中燃烧的化学方程式为______________________
(3)元素D、E的最高价氧化物对应的水化物的酸性_____ 大于_____ (填化学式).
(4)请举出C单质的一种用途_____ .

(1)元素B和E形成的化合物的电子式为
(2)B的单质在A的单质中燃烧的化学方程式为
(3)元素D、E的最高价氧化物对应的水化物的酸性
(4)请举出C单质的一种用途
您最近半年使用:0次



