名校
1 . 现有四种短周期元素,其有关信息如表所示:
则甲、乙、丙、丁四种元素的原子序数从大到小的排列顺序为
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 第三周期简单离子半径最小的元素 | 工业上用电解法冶炼该金属 |
| 乙 | 原子最外层电子数是次外层电子数的一半 | 单质是重要的半导体材料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的单质 | 丁的一种单质与KI溶液反应生成丁的另一种单质 |
| A.乙、甲、丁、丙 | B.丁、甲、乙、丙 |
| C.丙、丁、甲、乙 | D.甲、乙、丙、丁 |
您最近半年使用:0次
名校
解题方法
2 . A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:____ 。
(2)D单质与C单质在加热条件下反应产物的电子式____ ,该物质与A的氧化物反应产生氧气,离子方程式为_____ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为____ 。
(4)G单质在一定条件下可以和A2C反应,方程式为_______ 。
(5)用电子式写出A2C的形成过程_______ 。
(1)E的原子结构示意图:
(2)D单质与C单质在加热条件下反应产物的电子式
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(4)G单质在一定条件下可以和A2C反应,方程式为
(5)用电子式写出A2C的形成过程
您最近半年使用:0次
解题方法
3 .  是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
 是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是
是一种用途广泛的有机合成试剂,R、W、X、Y、Z五种原子序数依次递增的短周期元素,R的最外层电子为内层电子的2倍,R与X形成的化合物可造成温室效应,下列叙述正确的是| A.14W与14R的中子数相同 |
| B.离子半径:Z>Y>X |
| C.W与X两元素之间可组成多种共价化合物且只含共价键 |
| D.氧化物对应水化物的酸性:Z>W>Y |
您最近半年使用:0次
名校
4 . Y、Z、U、W为四种短周期非金属元素,它们的原子半径与原子序数的关系如图所示,其中W的单质呈黄绿色。下列有关这四种元素的单质的用途说法不正确 的是
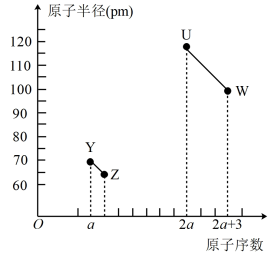

| A.W的单质可用于自来水消毒 |
| B.U的单质为光导纤维的主要成分 |
| C.Z的单质可用作氧化剂 |
| D.Y的单质可用作灯泡保护气 |
您最近半年使用:0次
2021-03-08更新
|
285次组卷
|
5卷引用:四川省雅安中学2020-2021学年高一下学期开学考试化学试题
名校
解题方法
5 . A、B、C、D、E、F的原子序数依次增大的短周期元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的离子结构示意图:___ 。
(2)D单质与C单质反应产物可能是___ ,其中有强氧化性的物质与A2C反应的离子方程式___ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为___ 。
(4)DA化合物与A2C化合物反应可以得到A的单质,则化学方程式___ 。
(5)E的最高价氧化物对应水合物的浓溶液加入G单质,下列说法不正确的是___ 。
A.常温下两者不发生反应
B.常温下无现象,G单质不溶解
C.受热能发生反应,开始放出氢气
D.受热能发生反应,开始放出是SO2
(1)E的离子结构示意图:
(2)D单质与C单质反应产物可能是
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为
(4)DA化合物与A2C化合物反应可以得到A的单质,则化学方程式
(5)E的最高价氧化物对应水合物的浓溶液加入G单质,下列说法不正确的是
A.常温下两者不发生反应
B.常温下无现象,G单质不溶解
C.受热能发生反应,开始放出氢气
D.受热能发生反应,开始放出是SO2
您最近半年使用:0次
名校
6 . 碳及其化合物在生产、生活中有广泛的用途。
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为___________ ,R的电子式为___________
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为___________ ,除去粗产品中少量钠的试剂为___________
(3)碳还原制取金刚砂SiC,其粗产品中杂质为Si和SiO2.先将20.0gSiC粗产品加入到过量NaOH溶液中充分反应,收集到标准状况下2.24 L的氢气,过滤后得SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为___________ ,硅酸盐的物质的量浓度为___________
(1)碳与同周期元素Q的单质化合仅能生成两种常见气态化合物,其中一种化合物R为非极性分子,则Q元素在周期表中的位置为
(2)一定条件下,Na还原CCl4可制备金刚石,反应结束冷却至室温后,回收CCl4的实验操作名称为
(3)碳还原制取金刚砂SiC,其粗产品中杂质为Si和SiO2.先将20.0gSiC粗产品加入到过量NaOH溶液中充分反应,收集到标准状况下2.24 L的氢气,过滤后得SiC固体11.4g,滤液稀释到1L。Si与NaOH溶液反应的离子方程式为
您最近半年使用:0次
7 .  、
、 、
、 、
、 、
、 、
、 六种短周期主族元素,其原子序数依次增大。
六种短周期主族元素,其原子序数依次增大。 是形成化合物种类最多的元素,
是形成化合物种类最多的元素, 、
、 能形成两种液态化合物
能形成两种液态化合物 和
和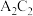 ,
, 、
、 同主族,
同主族, 元素的周期序数与主族序数相等。根据以上信息,回答下列问题:
元素的周期序数与主族序数相等。根据以上信息,回答下列问题:
(1) 元素在周期表中的位置为
元素在周期表中的位置为___________ , 、
、 、
、 三种元素的原子半径由大到小顺序为
三种元素的原子半径由大到小顺序为___________ (用原子符号表示)。
(2)化合物 、
、 性质比较:热稳定性:
性质比较:热稳定性:
___  ;沸点:
;沸点:
____  (填“
(填“ ”或“
”或“ ”)。
”)。
(3)物质 由
由 、
、 两种元素组成,
两种元素组成, 的产量可以用来衡量一个国家的石油化工发展水平,则
的产量可以用来衡量一个国家的石油化工发展水平,则 分子的电子式为:
分子的电子式为:___________ ,将 通入溴的四氧化碳溶液中,发生反应的化学方程式为
通入溴的四氧化碳溶液中,发生反应的化学方程式为___________ 。
(4) 的单质和化合物是一种用途很广的材料。写出
的单质和化合物是一种用途很广的材料。写出 单质与氧化铁高温加热制取铁的化学方程式:
单质与氧化铁高温加热制取铁的化学方程式:___________ 。
(5)向 溶液中通入适量的
溶液中通入适量的 单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:___________ 。
 、
、 、
、 、
、 、
、 、
、 六种短周期主族元素,其原子序数依次增大。
六种短周期主族元素,其原子序数依次增大。 是形成化合物种类最多的元素,
是形成化合物种类最多的元素, 、
、 能形成两种液态化合物
能形成两种液态化合物 和
和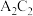 ,
, 、
、 同主族,
同主族, 元素的周期序数与主族序数相等。根据以上信息,回答下列问题:
元素的周期序数与主族序数相等。根据以上信息,回答下列问题:(1)
 元素在周期表中的位置为
元素在周期表中的位置为 、
、 、
、 三种元素的原子半径由大到小顺序为
三种元素的原子半径由大到小顺序为(2)化合物
 、
、 性质比较:热稳定性:
性质比较:热稳定性:
 ;沸点:
;沸点:
 (填“
(填“ ”或“
”或“ ”)。
”)。(3)物质
 由
由 、
、 两种元素组成,
两种元素组成, 的产量可以用来衡量一个国家的石油化工发展水平,则
的产量可以用来衡量一个国家的石油化工发展水平,则 分子的电子式为:
分子的电子式为: 通入溴的四氧化碳溶液中,发生反应的化学方程式为
通入溴的四氧化碳溶液中,发生反应的化学方程式为(4)
 的单质和化合物是一种用途很广的材料。写出
的单质和化合物是一种用途很广的材料。写出 单质与氧化铁高温加热制取铁的化学方程式:
单质与氧化铁高温加热制取铁的化学方程式:(5)向
 溶液中通入适量的
溶液中通入适量的 单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
单质后,取少量反应后的溶液,往其中滴加少许淀粉溶液,现象是:
您最近半年使用:0次
解题方法
8 . 部分中学化学常见元素原子结构及性质如下表所示。
(1)这五种元素的原子半径由大到小的顺序为_______________ (用元素符号表示)。
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为________ 。E与C组成的两种化合物M、N,所含电子数分别与X、Y相等,M中共用电子对对数为_______________ ,N的结构式为_______________ 。
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是_______________ 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
| 序号 | 元素 | 结构及性质 |
| ① | A | A为地壳中含量仅次于氧的非金属元素,其单质晶体结构与金刚石相似 |
| ② | B | B原子最外层电子数是内层电子总数的1/5 |
| ③ | C | C是常用化肥的主要元素,单质常温下呈气态 |
| ④ | D | 通常情况下,D在化合物中显负价,A、B、C都能与D形成中学常见化合物 |
| ⑤ | E | E是宇宙中最丰富的元素 |
(1)这五种元素的原子半径由大到小的顺序为
(2)E与D可以按原子个数比2:1、1:1形成两种化合物X、Y,区别X、Y这两种物质的实验方案为
(3)A与C可以形成一种新型陶瓷材料,机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备
B.在电子工业上制成耐高温的电的良导体
C.研发此种陶瓷的全陶发动机替代同类型金属发动机
D.此种陶瓷的开发受到资源的限制,没有发展前途
您最近半年使用:0次
解题方法
9 . 现有四种短周期元素的有关信息如表所示:
则甲、乙、丙、丁四种元素的原子序数从大到小的排列顺序为( )
| 元素 | 结构特点及在周期表中的位置 | 单质及化合物的部分性质与用途 |
| 甲 | 在元素周期表中,主族序数等于周期序数 | 工业上用电解法冶炼该金属 |
| 乙 | 原子最外层电子数是次外层电子数的一半 | 单质是重要的半导体材料 |
| 丙 | 原子最外层电子数是最内层电子数的2倍 | 单质存在多种同素异形体 |
| 丁 | 元素能形成两种不同的单质 | 丁的一种单质与KI溶液反应生成丁的另一种单质 |
| A.甲、乙、丙、丁 | B.丁、甲、乙、丙 |
| C.丙、丁、甲、乙 | D.乙、甲、丁、丙 |
您最近半年使用:0次
2020-10-07更新
|
1533次组卷
|
4卷引用:高一必修第一册(苏教2019版)专题5 高考挑战区
高一必修第一册(苏教2019版)专题5 高考挑战区四川省泸州合江县利城高级中学校2021-2022学年高一下学期第三次月考化学试题(已下线)第四章《物质结构 元素周期律》能力提升单元检测-【帮课堂】2022-2023学年高一化学同步精品讲义(人教版2019必修第一册)陕西省西安市蓝田县乡镇学校联考2023-2024学年高一上学期1月期末化学试题
10 . A、B、C、D、E、F、G七种短周期主族元素的原子序数依次增大。A和E最外层电子数相同,短周期主族元素的原子中,E原子的半径最大;B、C和F在周期表中相邻,B、C同周期,C、F同主族,F原子的质子数是C原子质子数的2倍;A和C可形成两种常见的液态化合物X和Y(相对分子质量X<Y);D形成的分子为双原子分子。回答问题:
(1)D元素的名称为_________ ,F形成的离子的结构示意图为__________ 。
(2)元素E、F形成的化合物的电子式为_______ 。
(3)元素C、F氢化物的沸点C______ F(填“>”或“<”)。
(4)写出液态化合物Y的一种用途_________ 。
(5)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式______ 。
(6)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为_____ 。
(1)D元素的名称为
(2)元素E、F形成的化合物的电子式为
(3)元素C、F氢化物的沸点C
(4)写出液态化合物Y的一种用途
(5)用某种金属易拉罐与A、C、E组成的化合物的水溶液反应,产生的气体可充填气球,请写出该反应的离子方程式
(6)A、B、G三种元素两两组合形成的化合物在空气中相遇形成白烟,反应的化学方程式为
您最近半年使用:0次



