1 . 现有X、Y、Z三种属于元素周期表前18种的元素,X的单质可以在Z的单质中燃烧,生成XZ,燃烧时火焰为苍白色;X的单质也可以与Y的单质化合,生成常温下为液体的X2Y;Z的单质溶于X2Y中,生成一种含X、Y、Z三种元素的物质,具有强氧化性,可用于自来水的消毒。根据以上信息,完成下列问题:
(1)画出Z的原子结构示意图为____________ 。
(2)将XZ的水溶液滴入NaHCO3溶液中,有气泡产生,反应的离子方程式为____________ 。
(3)实验室可用X、Y两种元素组成的另外一种化合物来制备Y的单质,试写出该反应的化学方程式______ ;若生成11.2 L(标准状况)的Y的单质,则转移的电子的物质的量为____________ 。
(4)据报道:“84”消毒液(主要成分是NaClO)与“洁厕灵”(主要成分是XZ)混用,释放出一种有毒气体,发生中毒事件。试用离子方程式表示其原因__________ 。
(5)试写出Z的单质溶于X2Y中反应的化学方程式为_____________ 。
(6)由Y与Z组成的化合物ZY2,已成为一种新型自来水消毒剂。从物质的分类角度分析,化合物ZY2属于___________ 。
(1)画出Z的原子结构示意图为
(2)将XZ的水溶液滴入NaHCO3溶液中,有气泡产生,反应的离子方程式为
(3)实验室可用X、Y两种元素组成的另外一种化合物来制备Y的单质,试写出该反应的化学方程式
(4)据报道:“84”消毒液(主要成分是NaClO)与“洁厕灵”(主要成分是XZ)混用,释放出一种有毒气体,发生中毒事件。试用离子方程式表示其原因
(5)试写出Z的单质溶于X2Y中反应的化学方程式为
(6)由Y与Z组成的化合物ZY2,已成为一种新型自来水消毒剂。从物质的分类角度分析,化合物ZY2属于
您最近一年使用:0次
2020-11-16更新
|
612次组卷
|
5卷引用:山西省朔州市怀仁市大地学校2020-2021学年高一上学期第四次月考化学试题
山西省朔州市怀仁市大地学校2020-2021学年高一上学期第四次月考化学试题湖南省三湘名校教育联盟2020-2012学年高一上学期期中考试化学试题(已下线)4.2.2 元素周期表和元素周期律的应用(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.2.2 元素周期表和元素周期律的应用-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)(已下线)专题4.2.2 元素周期表和周期律的应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)
解题方法
2 . 下列每一序号代表一种元素。元素①是常见的过渡元素,其氧化物为黑色且具有磁性。元素②~⑤的性质如表1和元素⑥~⑩在周期表中的位置如表2所示。请回答下列有关问题:
表1

(1)元素⑤的简单离子的结构示意图是_ ;所给元素中,其含氧化合物能用于漂白,该元素可能是_ (填元素符号)。
(2)元素④在元素周期表中的位置是___ ,该元素的氢化物与元素⑤的单质在高温催化剂条件下反应的化学方程式为_____ 。
(3)元素③的单质与元素①的磁性氧化物在高温条件下发生反应的化学方程式为______ 。
(4)元素⑥的单质在元素⑤的单质中燃烧的产物含有的化学键为___ 。
(5)元素⑦ 、⑧、⑨的氢化物的稳定性由弱到强的顺序为__ (填化学式)。设计实验证明单质氧化性顺序为⑩>⑧____ 。
元素序号 | ② | ③ | ④ | ⑤ |
原子半径/pm | 130 | 118 | 75 | 73 |
主要化合价 | +2 | +3 | +5、+3、-3 | -2 |

(1)元素⑤的简单离子的结构示意图是
(2)元素④在元素周期表中的位置是
(3)元素③的单质与元素①的磁性氧化物在高温条件下发生反应的化学方程式为
(4)元素⑥的单质在元素⑤的单质中燃烧的产物含有的化学键为
(5)元素⑦ 、⑧、⑨的氢化物的稳定性由弱到强的顺序为
您最近一年使用:0次
2020-07-23更新
|
27次组卷
|
2卷引用:山西省朔州市怀仁市第一中学云东校区2019-2020学年高一期末考试化学试题
名校
3 . X、Y、Z、W、R、P、Q是短周期主族元素,部分信息如下表所示:
(1)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为___ 。
(2)Z的单质与水反应的化学方程式是___ ;R与Q两元素最高价氧化物水化物反应的离子方程式___ 。
(3)Y与R相比,非金属性较强的是___ (用元素符号表示),下列事实能证明这一结论的是___ (填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)写出工业制取Y的单质的化学方程式___ 。
(5)反应3X2(g)+P2(g) 2PX3(g)过程中的能量变化如图所示回答下列问题:
2PX3(g)过程中的能量变化如图所示回答下列问题:
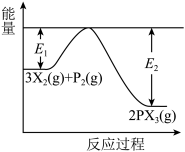
①该反应是___ 反应(填“吸热”“放热”);
②反应体系中加入催化剂对反应热是否有影响?___ ,原因是___ (从能量说明)
| X | Y | Z | W | R | P | Q | |
| 原子半径/nm | 0.154 | 0.074 | 0.099 | 0.075 | 0.143 | ||
| 主要化合价 | -4,+4 | -2 | -1,+7 | -3,+5 | +3 | ||
| 其他 | 阳离子核外无电子 | 无机非金属材料的主角 | 焰色反应呈黄色 |
(1)R在自然界中有质量数为35和37的两种核素,它们之间的关系是互为
(2)Z的单质与水反应的化学方程式是
(3)Y与R相比,非金属性较强的是
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX4
c.Y与R形成的化合物中Y呈正价
(4)写出工业制取Y的单质的化学方程式
(5)反应3X2(g)+P2(g)
 2PX3(g)过程中的能量变化如图所示回答下列问题:
2PX3(g)过程中的能量变化如图所示回答下列问题:
①该反应是
②反应体系中加入催化剂对反应热是否有影响?
您最近一年使用:0次
名校
4 . 部分短周期元素的性质或原子结构等信息如下表:
(1)写出X在元素周期表中的位置_________ 。
(2)写出实验室制取W的气态氢化物的化学方程式_________ 。
(3)Z的一种核素可测定文物年代,其中子数比质子数多2,这种核素的符号是_________ 。
(4)W的气态氢化物与最高价氧化物对应水化物形成的盐中存在的化学键类型为_________ 。
(5)W元素与氢元素按原子数目比1:3和2:4构成分子A和B,A的电子式为_________ ,B的结构式为__________ 。
(6)X与Y相比,非金属性较强的是_______ (填元素符号),下列能证实这一事实的是_________
a.单质X沸点比单质Y的低
b.X的氢化物比Y的氢化物稳定
c.单质X能与水反应,而单质Y不能与水反应
| 元素编号 | 元素性质或原子结构信息 |
| X | 元素最高正价是+7价 |
| Y | M层的电子数是K层的3倍 |
| Z | 最外层电子数是次外层电子数的2倍 |
| W | 单质是双原子分子,其氢化物水溶液呈碱性 |
(2)写出实验室制取W的气态氢化物的化学方程式
(3)Z的一种核素可测定文物年代,其中子数比质子数多2,这种核素的符号是
(4)W的气态氢化物与最高价氧化物对应水化物形成的盐中存在的化学键类型为
(5)W元素与氢元素按原子数目比1:3和2:4构成分子A和B,A的电子式为
(6)X与Y相比,非金属性较强的是
a.单质X沸点比单质Y的低
b.X的氢化物比Y的氢化物稳定
c.单质X能与水反应,而单质Y不能与水反应
您最近一年使用:0次
9-10高二·山东·假期作业
名校
解题方法
5 . A、B、C、D是按原子序数由小到大排列的前20号元素的单质。B、E均为组成空气的成分。F的焰色反应呈黄色。在G中,非金属元素与金属元素的原子个数比为1:2。在一定条件下,各物质之间的相互转化关系如右(部分产物未列出):
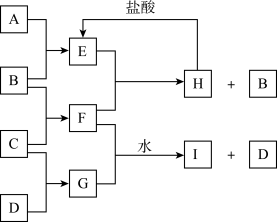
(1)A是_____ ,C是______ (填元素名称)。
(2)H与盐酸反应生成 E 的化学方程式是_________ 。
(3)E与F反应的化学方程式是___________ 。
(4)F与G的水溶液反应生成I和D的离子方程式是_____________ 。

(1)A是
(2)H与盐酸反应生成 E 的化学方程式是
(3)E与F反应的化学方程式是
(4)F与G的水溶液反应生成I和D的离子方程式是
您最近一年使用:0次
2020-06-13更新
|
114次组卷
|
8卷引用:2011-2012学年山西省山大附中高一2月月考化学试卷
(已下线)2011-2012学年山西省山大附中高一2月月考化学试卷(已下线)2010年安丘中学高二暑期练习化学卷(五)(已下线)2011-2012学年黑龙江省庆安三中高一上学期期末考试化学试卷(已下线)2011-2012学年内蒙古包头33中高二下学期期末考试化学试卷(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第5讲 无机框图题的解答策略【押题专练】青海省西宁市海湖中学2019-2020学年高一下学期第一阶段考试化学试题安徽省安庆市怀宁县怀宁中学2019-2020学年高一下学期期中考试化学试题山东省潍坊第一中学2021届高三上学期开学检测化学试题
名校
解题方法
6 . A、B、C、D、E、F的核电荷数依次增大,且均为核电荷数小于18的非稀有气体元素。A的单质是自然界中密度最小的气体,A和C可形成A2C和A2C2两种常见的液态化合物,B、C原子的最外层电子数之和等于11,D+与C的简单离子的核外电子排布相同,C、E原子的最外层电子数相同。请回答下列问题:
(1)写出元素符号:B______ ,D______ 。
(2)A元素具有两个中子的核素的表示符号为_____ ,E的简单离子的结构示意图是______ 。
(3)A2C2的分子式为________ 。
(4)将少量F的单质通入足量氢氧化钠溶液中,发生反应的离子方程式是_________________________________________________ 。
(5)标准状况下,试管中收集满F的简单氢化物后倒立于水中(假设溶质不向试管外扩散),一段时间后,试管内溶液中溶质的物质的量浓度为____________ mol·L-1。
(1)写出元素符号:B
(2)A元素具有两个中子的核素的表示符号为
(3)A2C2的分子式为
(4)将少量F的单质通入足量氢氧化钠溶液中,发生反应的离子方程式是
(5)标准状况下,试管中收集满F的简单氢化物后倒立于水中(假设溶质不向试管外扩散),一段时间后,试管内溶液中溶质的物质的量浓度为
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、M、N是短周期元素,且原子序数依次递增。已知X的最外层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大。Z和N可以形成ZN2型化合物。回答下列问题:
(1)元素N在周期表中的位置____________ ,它的最高价氧化物的化学式为____________________________________ 。
(2)由元素X、Y形成的一种化合物可以作为呼吸面具的供氧剂,该化合物的电子式为__________________ ,其所含化学键的类型为____________ 。
(3)用电子式表示ZN2的形成过程____________________ 。
(4)Z能在氮气中燃烧,Z在氮气中燃烧的产物与水反应可产生一种使湿润红色石蕊试纸变蓝的气体。写出Z在氮气中的燃烧产物与水反应的化学方程式:________________________________________________________
(1)元素N在周期表中的位置
(2)由元素X、Y形成的一种化合物可以作为呼吸面具的供氧剂,该化合物的电子式为
(3)用电子式表示ZN2的形成过程
(4)Z能在氮气中燃烧,Z在氮气中燃烧的产物与水反应可产生一种使湿润红色石蕊试纸变蓝的气体。写出Z在氮气中的燃烧产物与水反应的化学方程式:
您最近一年使用:0次
2020-05-18更新
|
98次组卷
|
3卷引用:山西省运城市高中联合体2019-2020学年高一下学期第一次摸底考试化学试题
名校
8 . A、B、C、D、E、F、G 是短周期元素,周期表中 B 与 C 相邻,C 与 E 同主族; A 中 L 层是 K 层的 2 倍,B 的电子数比 C 的电子数少 1 个;F 元素的原子在周期表中半径最小;常见化合物 D2C2 与水反应生成 C 的气体单质,且完全反应后的溶液能使酚酞溶液变红。G 是第三周期原子半径最小的主族元素。
(1)A 在元素周期表中的位置_________________ 。
(2) D2C2 的电子式为________ , 属于________________ 化合物(填“离子”或“共价”)。
(3)C 与 F 元素可形成 18 电子分子的电子式为 。
(4)A、B、C 的氢化物稳定性顺序为____________________ (用分子式表示); G 的阴离子的还原性比 E 的阴离子的还原性 ___________________________ (填“强”或“弱”)。
(5)F2C 和 F2E 中,沸点较高的是________ (填化学式),其主要原因是 _____________ 。
(6)锡(Sn)与 A 同主族,常温下能和浓硫酸反应,生成 Sn(SO4)2 和刺激性气味气体, 反应的化学方程式为__________________________________ 。
(1)A 在元素周期表中的位置
(2) D2C2 的电子式为
(3)C 与 F 元素可形成 18 电子分子的电子式为 。
(4)A、B、C 的氢化物稳定性顺序为
(5)F2C 和 F2E 中,沸点较高的是
(6)锡(Sn)与 A 同主族,常温下能和浓硫酸反应,生成 Sn(SO4)2 和刺激性气味气体, 反应的化学方程式为
您最近一年使用:0次
2020-05-08更新
|
184次组卷
|
2卷引用:山西省古县第一中学2019-2020学年高一下学期期中考试化学试题
解题方法
9 . A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。其中B的单质在常温下为双原子分子,它与A的单质可形成分子X,X的水溶液呈碱性;D的简单阳离子与X具有相同电子数,且D是同周期中简单离子半径最小的元素;E元素的原子最外层比次外层少两个电子,C、F两种元素的原子最外层共有13个电子。则
(1)A的元素符号______________ ,D的元素名称 ____________ 。
(2)C在周期表中的位置:___________ ,E的离子结构示意图________ ;
(3)B、C、E分别与A形成的化合物中最稳定的是________ (写化学式);E、F的最高价氧化物对应的水化物的酸性较强的是________ (写化学式)
(4)F的单质在反应中常作氧化剂,该单质的水溶液与E的低价氧化物反应的离子方程式为________________ 。
(5)X在纯净的C单质中可以安静的燃烧,生成B的单质。该反应的化学方程式为:__________________ 。
(1)A的元素符号
(2)C在周期表中的位置:
(3)B、C、E分别与A形成的化合物中最稳定的是
(4)F的单质在反应中常作氧化剂,该单质的水溶液与E的低价氧化物反应的离子方程式为
(5)X在纯净的C单质中可以安静的燃烧,生成B的单质。该反应的化学方程式为:
您最近一年使用:0次
名校
10 . 三种短周期元素x、y、z对应的单质X、Y、Z,常温常压下均为无色气体,在适当条件下单质X、Y、Z之间可以发生如图所示的变化。已知B分子组成中z原子个数比C分子中多一个。
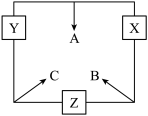
请回答下列问题:
(1)元素x的原子结构示意图___ ;元素y在周期表中的位置是___ ;
(2)写出单质氟与C反应的离子反应方程式:___ 。
(3)Y与X在一定条件下生成化合物A的化学方程式:___ 。
(4)一定条件下,将盛有10mLA的大试管倒置于水槽的水中然后缓缓通入Y至液体刚好充满试管,写出反应的化学方程式___ ;通入相同状况下气体Y的体积为___ 。
(5)用电子式表示B的形成过程___ 。

请回答下列问题:
(1)元素x的原子结构示意图
(2)写出单质氟与C反应的离子反应方程式:
(3)Y与X在一定条件下生成化合物A的化学方程式:
(4)一定条件下,将盛有10mLA的大试管倒置于水槽的水中然后缓缓通入Y至液体刚好充满试管,写出反应的化学方程式
(5)用电子式表示B的形成过程
您最近一年使用:0次



