名校
1 . 有A、B、C、D、E、F6种短周期元素,其元素特征信息如表,回答下列问题:
(1)C元素在周期表中位置___________ 。
(2)写出D、E、F元素符号:D___________ 、E___________ 、F___________ 。
(3)写出A、B、C形成的化合物的电子式___________ ;该化合物含有的化学键类型有___________ 、___________ 。
(4)写出三种含B元素的10e-微粒___________ 、___________ 、___________ 。
(5)F的非金属性强于E,下列表述中能证明这一事实的是___________ (填字母)。
A.F的氢化物比E的氢化物稳定
B.F的单质能将E从其钠盐溶液中置换出来
| 编号 | 元素特征信息 |
| A | 其单质是密度最小的物质 |
| B | 阴离子带两个单位负电荷,单质是空气的主要成分之一 |
| C | 其阳离子与B的阴离子有相同的电子层结构,且与B可以形成两种离子化合物 |
| D | 其氢氧化物和氧化物都有两性,与C同周期 |
| E | 与C同周期,最高正化合价与最低负化合价的代数和为4 |
| F | 其最简单气态氢化物能和其最高价氧化物反应生成一种离子化合物 |
(1)C元素在周期表中位置
(2)写出D、E、F元素符号:D
(3)写出A、B、C形成的化合物的电子式
(4)写出三种含B元素的10e-微粒
(5)F的非金属性强于E,下列表述中能证明这一事实的是
A.F的氢化物比E的氢化物稳定
B.F的单质能将E从其钠盐溶液中置换出来
您最近一年使用:0次
名校
2 . 下表为元素周期表的一部分,请参照元素 在表中的位置,用相应化学用语回答下列问题:
在表中的位置,用相应化学用语回答下列问题:
(1)画出表中形成化合物种类最多元素的原子结构示意图______ ;写出它与原子半径最小的原子形成 电子且为正四面体结构的化合物的电子式
电子且为正四面体结构的化合物的电子式______ ,用电子式表示 和
和 形成化合物的过程
形成化合物的过程______ 。
(2) 形成的简单离子半径由大到小的顺序为
形成的简单离子半径由大到小的顺序为______  填离子符号
填离子符号 ;
; 的最高价氧化物对应水化物的酸性由强到弱的顺序为
的最高价氧化物对应水化物的酸性由强到弱的顺序为______  填化学式
填化学式 。
。
(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是______  填化学式
填化学式 ,写出它与
,写出它与 的最高价氧化物对应水化物发生反应的离子方程式:
的最高价氧化物对应水化物发生反应的离子方程式:______ 。
(4)有两种化合物 和
和 都由
都由 四种元素组成.若
四种元素组成.若 与
与 在水溶液中能发生离子反应,则该反应的离子方程式为
在水溶液中能发生离子反应,则该反应的离子方程式为 ______ 。
 在表中的位置,用相应化学用语回答下列问题:
在表中的位置,用相应化学用语回答下列问题:
(1)画出表中形成化合物种类最多元素的原子结构示意图
 电子且为正四面体结构的化合物的电子式
电子且为正四面体结构的化合物的电子式 和
和 形成化合物的过程
形成化合物的过程(2)
 形成的简单离子半径由大到小的顺序为
形成的简单离子半径由大到小的顺序为 填离子符号
填离子符号 ;
;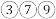 的最高价氧化物对应水化物的酸性由强到弱的顺序为
的最高价氧化物对应水化物的酸性由强到弱的顺序为 填化学式
填化学式 。
。(3)这些元素形成的氧化物中,不溶于水,但既能与强酸又能与强碱反应的是
 填化学式
填化学式 ,写出它与
,写出它与 的最高价氧化物对应水化物发生反应的离子方程式:
的最高价氧化物对应水化物发生反应的离子方程式:(4)有两种化合物
 和
和 都由
都由 四种元素组成.若
四种元素组成.若 与
与 在水溶液中能发生离子反应,则该反应的离子方程式为
在水溶液中能发生离子反应,则该反应的离子方程式为
您最近一年使用:0次
2023-07-30更新
|
204次组卷
|
3卷引用:宁夏回族自治区银川市宁夏育才中学2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
3 . X、Y、Z、W、R五种元素的性质或结构信息如表,根据表中的信息回答下列问题:
(1)写出元素R在元素周期表中的位置:_______ 。
(2)由X、Z、R三种元素形成具有漂白性的化合物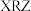 的化学式为
的化学式为_______ 。
(3)W与Z的单质在加热条件反应的化学方程式是_______ 。
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:_______ ,燃烧片刻后取出燃烧管,迅速将集气瓶倒扣在过量的烧碱溶液中,可能产生的现象是_______ ,所得溶液中存在的溶质除了过量的 外,还含有的是
外,还含有的是_______ (填化学式)。
| 元素 | X | Y | Z | W | R |
| 性质或结构信息 | 单质是最轻的气体 | 常见单质为空气中的主要成分之 | 是地壳中含量最多的元素 | 原子核内有11个质子 | 原子核外有3个电子层,常见单质为黄绿色气体 |
(2)由X、Z、R三种元素形成具有漂白性的化合物
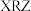 的化学式为
的化学式为(3)W与Z的单质在加热条件反应的化学方程式是
(4)写出少量X的单质在盛满R的单质的集气瓶中燃烧的现象:
 外,还含有的是
外,还含有的是
您最近一年使用:0次
名校
4 . A、B、C、D、E是位于短周期的主族元素。已知:①氢化物的稳定性HmD>HmC;②Cm−、E(m−1)−具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
(1)HmDm的电子式为_______ ,含有_______ (填“离子键”、“极性键”或“非极性键”)。
(2)Cm−、E(m−1)−的还原性强弱顺序为_______ 、离子半径大小顺序为_______ (均用离子符号表示),能证明其还原性强弱的离子方程式为_______ 。
(3)比较两种氢化物的沸点:HmD_______ HmC(填“>”或“<”),C元素在元素周期表中的位置为_______ 。
(4)用于判断C和D非金属性强弱的依据是_______。
(1)HmDm的电子式为
(2)Cm−、E(m−1)−的还原性强弱顺序为
(3)比较两种氢化物的沸点:HmD
(4)用于判断C和D非金属性强弱的依据是_______。
| A.简单气态氢化物的稳定性 | B.与氢气化合的难易程度 |
| C.得电子数目的多少 | D.最高价含氧酸的酸性 |
您最近一年使用:0次
名校
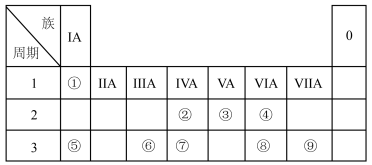
5 . 下图是元素周期表的一部分。按要求填写下列空白:

(1)元素⑦在周期表中的位置为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物中所含的化学键为_______ ;③的氢化物的电子式为_______ 。
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是_______ 。
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱

(1)元素⑦在周期表中的位置为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物中所含的化学键为
(6)为了证明⑤和⑥两种元素的金属性强弱,下列说法或实验能提供证据的是
A.比较两种元素的单质的熔点、沸点高低
B.将两种元素的单质分别与冷水反应,观察反应的剧烈程度
C.比较两种元素的最高价氧化物对应的水化物的碱性强弱
您最近一年使用:0次
2023-01-31更新
|
191次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2022-2023学年高一下学期3月月考化学试题
名校
解题方法
6 . 处于同一短周期A、B、C、D四种元素,在同族元素中,A的气态氢化物的沸点最高,B的最高价氧化物对应的水化物的酸性在同周期中是最强的,C的电负性介于A、B之间,D与B相邻。请填空:
(1)在B的单质分子中存在_______ 个π键,_______ 个σ键;
(2)已知B的气态氢化物很容易与H+结合,此时B原子与H+间形成的键称为_______ ,形成的离子立体构型为_______ ;
(3)在A、B、C、D四种元素形成的电子数相同的四种氢化物中,沸点最低的是_______ (写分子式),其沸点显著低于其他三种氢化物的原因是_______ ;
(4)A的氢化物易溶于水,原因是_______ 。
(1)在B的单质分子中存在
(2)已知B的气态氢化物很容易与H+结合,此时B原子与H+间形成的键称为
(3)在A、B、C、D四种元素形成的电子数相同的四种氢化物中,沸点最低的是
(4)A的氢化物易溶于水,原因是
您最近一年使用:0次
解题方法
7 . A、B、D、E、F、G为短周期主族元素,且原子序数依次递增。A位于第一周期,短周期中,F的氢氧化物碱性最强,E、G同主族。A与其他非金属元素化合时易形成共价键,F与其他非金属元素化合时易形成离子键,且F+与E2-核外电子排布相同。由以上元素组成的物质BE和D2具有相同的电子数。请回答下列问题:
(1)B位于第_____ 周期_____ 族。
(2)G的离子结构示意图为____ 。
(3)BE2的电子式为_____ 。
(4)由A、E、F三种元素形成的化合物的化学式为_____ ,含有的化学键有_____ (填写完整化学键类型),属于_____ 化合物。
(5)写出F2E2与水反应的化学方程式_____ 。
(1)B位于第
(2)G的离子结构示意图为
(3)BE2的电子式为
(4)由A、E、F三种元素形成的化合物的化学式为
(5)写出F2E2与水反应的化学方程式
您最近一年使用:0次
名校
解题方法
8 . 元素 、
、 、
、 、
、 、
、 均为原子序数依次增大的短周期主族元素,
均为原子序数依次增大的短周期主族元素, 在地壳金属元素中的含量仅次于
在地壳金属元素中的含量仅次于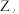 已知
已知 原子最外层电子数与核外电子总数之比为
原子最外层电子数与核外电子总数之比为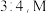 原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物
原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物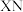 常温下为气体,请回答下列问题:
常温下为气体,请回答下列问题:
(1)写出 、
、 、
、 按原子个数之比
按原子个数之比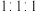 形成的化合物的化学式
形成的化合物的化学式_______ ; 和
和 气态氢化物的稳定性大小比较为
气态氢化物的稳定性大小比较为_______ (用化学式和“ ”“
”“ ”或“
”或“ ”表示)。
”表示)。
(2)X与 可分别形成
可分别形成 电子和
电子和 电子的分子,写出该
电子的分子,写出该 电子分子转化成
电子分子转化成 电子分子的化学方程式
电子分子的化学方程式_______ 。
(3)Z元素的单质能与 和
和 形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为_______ 。
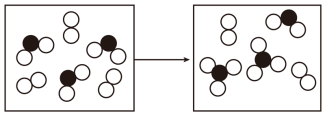
(4)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,示意图中转移电子的数目为_______ 。
(5)由 、
、 、
、 三种元素组成的离子,在水溶液中与
三种元素组成的离子,在水溶液中与 和
和 均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式_______ 。
 、
、 、
、 、
、 、
、 均为原子序数依次增大的短周期主族元素,
均为原子序数依次增大的短周期主族元素, 在地壳金属元素中的含量仅次于
在地壳金属元素中的含量仅次于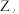 已知
已知 原子最外层电子数与核外电子总数之比为
原子最外层电子数与核外电子总数之比为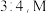 原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物
原子的最外层电子数与次外层电子数之比为3:4、N-、Z3+、X+离子半径逐渐减小;化合物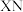 常温下为气体,请回答下列问题:
常温下为气体,请回答下列问题:(1)写出
 、
、 、
、 按原子个数之比
按原子个数之比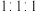 形成的化合物的化学式
形成的化合物的化学式 和
和 气态氢化物的稳定性大小比较为
气态氢化物的稳定性大小比较为 ”“
”“ ”或“
”或“ ”表示)。
”表示)。(2)X与
 可分别形成
可分别形成 电子和
电子和 电子的分子,写出该
电子的分子,写出该 电子分子转化成
电子分子转化成 电子分子的化学方程式
电子分子的化学方程式(3)Z元素的单质能与
 和
和 形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为
形成的化合物在一定条件下发生反应,同时放出大量的热,其反应的化学方程式为(4)如图表示由上述元素中的某两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,示意图中转移电子的数目为

(5)由
 、
、 、
、 三种元素组成的离子,在水溶液中与
三种元素组成的离子,在水溶液中与 和
和 均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
均不能大量共存,还能和氯水反应,写出其与新制氯水反应的离子方程式
您最近一年使用:0次
名校
解题方法
9 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请回答下列问题。
(1)A在元素周期表中的位置为___________ ,画出基态B原子的轨道表示式___________ 。
(2)B的简单气态氢化物的沸点___________ (填“高于”或“低于”)PH3,原因是___________ 。
(3)A、B、C三种元素的电负性由高到低的排列次序为___________ (用元素符号表示)。
(4)已知元素A、B形成的 链状分子中所有的原子都满足8电子稳定结构,则其分子中
链状分子中所有的原子都满足8电子稳定结构,则其分子中 键与
键与 键数目之比为
键数目之比为___________ 。
(5)G元素可形成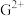 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(6)短周期元素 与元素
与元素 在周期表中的位置呈现对角线关系,已知元素
在周期表中的位置呈现对角线关系,已知元素 、
、 的电负性分别为1.5和3.0,预测它们形成的化合物是
的电负性分别为1.5和3.0,预测它们形成的化合物是___________ (填“离子”或“共价”)化合物。推测 的最高价氧化物对应的水化物
的最高价氧化物对应的水化物___________ (填“能”或“不能”)与 的最高价氧化物对应水化物发生反应。
的最高价氧化物对应水化物发生反应。
| A | 原子核外有6个电子 |
| B | 原子序数比 大1 大1 |
| C | 基态原子中 电子总数与p电子总数相等 电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子价层电子排布式为3s23p1 |
| F | 基态原子的最外层p 轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属,其高价氯化物的盐溶液常用于刻蚀铜制印刷电路板 |
(2)B的简单气态氢化物的沸点
(3)A、B、C三种元素的电负性由高到低的排列次序为
(4)已知元素A、B形成的
 链状分子中所有的原子都满足8电子稳定结构,则其分子中
链状分子中所有的原子都满足8电子稳定结构,则其分子中 键与
键与 键数目之比为
键数目之比为(5)G元素可形成
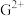 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(6)短周期元素
 与元素
与元素 在周期表中的位置呈现对角线关系,已知元素
在周期表中的位置呈现对角线关系,已知元素 、
、 的电负性分别为1.5和3.0,预测它们形成的化合物是
的电负性分别为1.5和3.0,预测它们形成的化合物是 的最高价氧化物对应的水化物
的最高价氧化物对应的水化物 的最高价氧化物对应水化物发生反应。
的最高价氧化物对应水化物发生反应。
您最近一年使用:0次
2022-07-25更新
|
978次组卷
|
3卷引用:宁夏石嘴山市第三中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
10 . 元素周期表是化学知识的宝库,它的内涵十分丰富。如表是a~m九种元素在周期表中的位置,请回答下列问题:
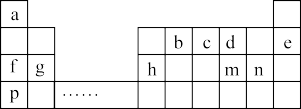
(1)m的阴离子结构示意图为____ 。
(2)d与a元素的原子按1:1结合的化合物的电子式____ 。
(3)b的最高价氧化物的结构式为____ 。
(4)d、g、n形成的简单离子的半径由大到小的顺序为____ (用离子符号填写)。
(5)f、g、p的最高价氧化物的水化物碱性从强到弱的顺序为____ (填化学式)。
(6)p和n两种元素最高价氧化物的水化物相互反应的离子反应方程式为____ 。
(7)c的氢化物和c的最高价氧化物对应水化物之间反应能生成盐M,M中含有的化学键类型有____ 。
(8)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。由镓的性质推知,镓与铝同主族,且位于h的下一周期。镓在周期表中的位置____ 。冶炼金属镓通常采用的方法是____ 。

(1)m的阴离子结构示意图为
(2)d与a元素的原子按1:1结合的化合物的电子式
(3)b的最高价氧化物的结构式为
(4)d、g、n形成的简单离子的半径由大到小的顺序为
(5)f、g、p的最高价氧化物的水化物碱性从强到弱的顺序为
(6)p和n两种元素最高价氧化物的水化物相互反应的离子反应方程式为
(7)c的氢化物和c的最高价氧化物对应水化物之间反应能生成盐M,M中含有的化学键类型有
(8)“类铝”在门捷列夫预言4年后,被布瓦博德朗在一种矿石中发现,命名为镓(Ga)。由镓的性质推知,镓与铝同主族,且位于h的下一周期。镓在周期表中的位置
您最近一年使用:0次



