解题方法
1 . 已知六种短周期元素A、B、C、D、E、F的原子序数依次增大,A的原子核内没有中子,A、D同主族,C、F同主族,A和B可形成5核10电子的阳离子,C与D形成的离子化合物D2C中所有离子的电子数相同,E的最高价氧化物的水化物可与D、F的最高价氧化物的水化物反应。试回答下列问题:
(1)E在元素周期表中的位置是___________ 。
(2)写出A和B形成4核10电子分子的电子式和结构式___________ 、___________ 。
(3)C、D、F的简单离子半径由大到小的顺序为(用离子符号表示)___________ 。
(4)根据“对角线规则”,铍(Be)的性质与上述六种元素中的___________ (填名称)相似,能溶于氢氧化钠溶液,生成Na2BeO2与H2。请写出氢氧化铍与氢氧化钠溶液反应的化学方程式___________ 。
(5)A、C、D可形成多种二元化合物。下列说法不正确的是___________(填字母)。
(6)能说明氯的非金属性比F强的事实是___________(填字母)。
①F的最高价氧化物水化物比次氯酸稳定
②高氯酸的酸性比F的最高价氧化物的水化物的酸性强
③F的简单阴离子比Cl—易被氧化
④HCl比F的氢化物稳定
⑤铜与盐酸不反应,但能与F的最高价氧化物的水化物的浓溶液反应
⑥铁与氯气在加热条件下反应生成氯化铁,铁与F单质在加热条件下反应生成某化亚铁
(1)E在元素周期表中的位置是
(2)写出A和B形成4核10电子分子的电子式和结构式
(3)C、D、F的简单离子半径由大到小的顺序为(用离子符号表示)
(4)根据“对角线规则”,铍(Be)的性质与上述六种元素中的
(5)A、C、D可形成多种二元化合物。下列说法不正确的是___________(填字母)。
| A.A2C2和D2C2中都含共价键 |
| B.A、D可形成离子化合物 |
C.D2C、D2C2中阴阳离子个数比均为 |
| D.D2C和D2C2均能溶于A2C,并发生化合反应 |
①F的最高价氧化物水化物比次氯酸稳定
②高氯酸的酸性比F的最高价氧化物的水化物的酸性强
③F的简单阴离子比Cl—易被氧化
④HCl比F的氢化物稳定
⑤铜与盐酸不反应,但能与F的最高价氧化物的水化物的浓溶液反应
⑥铁与氯气在加热条件下反应生成氯化铁,铁与F单质在加热条件下反应生成某化亚铁
| A.全部 | B.②③④⑥ | C.①②④⑤⑥ | D.②③④⑤⑥ |
您最近一年使用:0次
名校
2 . 有X、Y、Z、M、R、Q六种短周期的主族元素,部分信息如下表所示:
请回答下列问题:
(1)R在元素周期表中的位置是___________
(2)根据表中数据推测,Y的原子半径的最小范围是___________
(3)Z、M、Q的简单离子的半径由大到小的顺序为___________ (用离子符号表示)
(4)由元素X、M、Q组成的化合物属于___________ 化合物。写出Z2M2的电子式___________
(5)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是___________ (选填字母序号)
A.常温下Y的单质呈固态,R的单质呈气态
B.稳定性:XR>YX4
C.Y与R形成的化合物中Y呈正价
D.酸性HR>H2XO3
(6)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式___________
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.160 | ||
| 主要化合价 | -4、+ 4 | -2 | -1、+ 7 | |||
| 其它信息 | 某种核素无中子 | 常用的半导体材料 | 短周期主族元素中原子半径最大 | 次外层电子数是最外层电子数的4倍 |
(1)R在元素周期表中的位置是
(2)根据表中数据推测,Y的原子半径的最小范围是
(3)Z、M、Q的简单离子的半径由大到小的顺序为
(4)由元素X、M、Q组成的化合物属于
(5)下列事实能作为比较元素Y与R的非金属性相对强弱依据的是
A.常温下Y的单质呈固态,R的单质呈气态
B.稳定性:XR>YX4
C.Y与R形成的化合物中Y呈正价
D.酸性HR>H2XO3
(6)写出R的单质与Z的最高价氧化物对应水化物的水溶液反应的离子方程式
您最近一年使用:0次
2021-06-01更新
|
1270次组卷
|
6卷引用:山西省运城市盐湖区第五高级中学2023-2024学年高一上学期化学期末练兵卷(二)
解题方法
3 . A、B、C、D四种元素处于同一短周期,在同族元素中,A的气态氢化物的沸点最高,B的最高价氧化物对应的水化物的酸性在同周期中是最强的,C的电负性介于A、B之间,D与B相邻。
(1)C的原子的价电子排布式为___________ 。
(2)在B的单质分子中存在___________ 个π键,___________ 个σ键。
(3)已知B的气态氢化物很容易与H+结合,B的气态氢化物分子与 H+形成的离子立体构型为___________ 。
(4)在A、B、C、D四种元素形成的电子数相同的四种氢化物中沸点最低的是___________ (写分子式),其沸点显著低于其他三种氢化物的原因是: ___________ 。
(1)C的原子的价电子排布式为
(2)在B的单质分子中存在
(3)已知B的气态氢化物很容易与H+结合,B的气态氢化物分子与 H+形成的离子立体构型为
(4)在A、B、C、D四种元素形成的电子数相同的四种氢化物中沸点最低的是
您最近一年使用:0次
4 . 根据下列叙述完成要求
(1)A元素原子核外M层电子数是L层电子数的一半___________ (写出元素名称);
(2)B元素原子的最外层电子数是次外层电子数的1.5倍___________ (画出原子结构示意图);
(3)C元素的单质在常温下可与水剧烈反应,产生的气体能使带火星的木条复燃:___________ (写出核外电子排布式);
(4)D元素的次外层电子数是最外层电子数的 :
: ___________ (写出价电子排布式);
(5)1~36号元素原子核外电子排布中未成对电子数最多的原子___________ (价电子排布图)。
(1)A元素原子核外M层电子数是L层电子数的一半
(2)B元素原子的最外层电子数是次外层电子数的1.5倍
(3)C元素的单质在常温下可与水剧烈反应,产生的气体能使带火星的木条复燃:
(4)D元素的次外层电子数是最外层电子数的
 :
: (5)1~36号元素原子核外电子排布中未成对电子数最多的原子
您最近一年使用:0次
解题方法
5 . I.实验室需要0.5 mol∙L−1CuSO4溶液450mL和0.5 mol∙L−1硫酸溶液500mL,根据这两种溶液的配制情况回答下列问题:
(1)配制CuSO4溶液时,如果用CuSO4固体,应该称量固体的质量为___________ ;配制硫酸溶液时,需要取质量分数为98%、密度为1.84 g∙cm−3的浓硫酸的体积为___________ 。
(2)下列操作对溶液的浓度有何影响?(填“偏大”、“偏小”、“无影响”)
①配制的过程中有少量的液体迸溅出来___________
②定容时俯视刻度线___________ 。
Ⅱ.A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,C原子最外层电子数是电子层数的3倍,E和C同主族,A、B组成的气态化合物的水溶液呈碱性,D与C能按原子个数比为1:1或2:1形成离子化合物。
(1)A与C形成的化合物中,原子个数比为2:1的化合物的结构式为___________ ,此化合物中含有的化学键为___________ 。
(2)D与C按原子个数比为1:1形成化合物的电子式是___________ 。
(1)配制CuSO4溶液时,如果用CuSO4固体,应该称量固体的质量为
(2)下列操作对溶液的浓度有何影响?(填“偏大”、“偏小”、“无影响”)
①配制的过程中有少量的液体迸溅出来
②定容时俯视刻度线
Ⅱ.A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,C原子最外层电子数是电子层数的3倍,E和C同主族,A、B组成的气态化合物的水溶液呈碱性,D与C能按原子个数比为1:1或2:1形成离子化合物。
(1)A与C形成的化合物中,原子个数比为2:1的化合物的结构式为
(2)D与C按原子个数比为1:1形成化合物的电子式是
您最近一年使用:0次
6 . 短周期元素A、B、C、D、E的原子序数依次增大,A元素阳离子的原子核外没有电子,B是空气中含量最多的元素,C元素原子最外层电子数是其电子层数的三倍,C与D可形成两种常见的离子化合物,C与E形成的化合物具有两性。
(1)画出D元素的原子结构示意图_____ 。C、D、E的简单离子半径由小到大的顺序______ (用离子符号表示)。
(2)写出元素E在周期表中的位置____ 。
(3)工业上常用A和B的单质合成一种常见气体,检验该气体的常用方法______ 。
(4)D2C2与H2O反应的化学方程式是_______ ,D2C2与CuSO4溶液反应的现象是______ 。
(5)由元素A、B、C按原子个数比4∶2∶3形成的化合物 F 中含有的化学键类型是______ ,写出其电离方程式:_______ 。
(1)画出D元素的原子结构示意图
(2)写出元素E在周期表中的位置
(3)工业上常用A和B的单质合成一种常见气体,检验该气体的常用方法
(4)D2C2与H2O反应的化学方程式是
(5)由元素A、B、C按原子个数比4∶2∶3形成的化合物 F 中含有的化学键类型是
您最近一年使用:0次
7 . 短周期主族元素 、
、 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 与
与 同主族,
同主族, 的原子内层电子数是其最外层电子数的2倍,
的原子内层电子数是其最外层电子数的2倍, 是地壳中含量最多的元素,
是地壳中含量最多的元素, 的最高正化合价与负化合价的绝对值相差2,
的最高正化合价与负化合价的绝对值相差2, 的原子最外层电子数等于
的原子最外层电子数等于 、
、 、
、 的原子最外层电子数之和。请回答下列问题:
的原子最外层电子数之和。请回答下列问题:
(1)写出下列元素的名称:
_______ ,
_______ ,
_______ 。
(2) 与氢组成的化合物,其分子的空间结构是
与氢组成的化合物,其分子的空间结构是_______ 形。
(3) 与
与 相比,金属性较强的是
相比,金属性较强的是_______ (填元素符号),能证明该结论的一个事实_______ 。
 、
、 、
、 、
、 、
、 的原子序数依次增大,
的原子序数依次增大, 与
与 同主族,
同主族, 的原子内层电子数是其最外层电子数的2倍,
的原子内层电子数是其最外层电子数的2倍, 是地壳中含量最多的元素,
是地壳中含量最多的元素, 的最高正化合价与负化合价的绝对值相差2,
的最高正化合价与负化合价的绝对值相差2, 的原子最外层电子数等于
的原子最外层电子数等于 、
、 、
、 的原子最外层电子数之和。请回答下列问题:
的原子最外层电子数之和。请回答下列问题:(1)写出下列元素的名称:



(2)
 与氢组成的化合物,其分子的空间结构是
与氢组成的化合物,其分子的空间结构是(3)
 与
与 相比,金属性较强的是
相比,金属性较强的是
您最近一年使用:0次
名校
解题方法
8 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4。请回答下列问题:
(1)Y的元素名称是______ 。
(2)W在周期表中的位置是______ 。
(3)写出化合物Z2R的电子式______ 。
(4)写出化合物X2Y2的结构式______ 。
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是______ (用元素的离子符号表示)。
(6)下列说法能证明非金属性Q强于R的是______ (填序号)。
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是______ 。
(1)Y的元素名称是
(2)W在周期表中的位置是
(3)写出化合物Z2R的电子式
(4)写出化合物X2Y2的结构式
(5)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(6)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:Q>R
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性: Q>R
(7)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
您最近一年使用:0次
2021-01-19更新
|
592次组卷
|
5卷引用:山西省大同市第一中学校2022-2023学年高一上学期1月期末考试化学试题
名校
解题方法
9 . x、y、z、w、u为前20号元素中的五种,在一定条件下组成的单质及其化合物有如图所示转化关系。其中H、I、G为固体,F为液体,其他为气体。G由w- 和u2+ 两种具有相同电子构型的离子构成,是实验室常用的干燥剂。 回答下列问题:
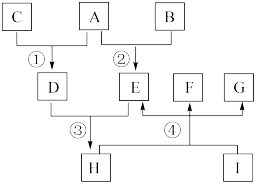
(1)G的电子式是___________
(2)在实验室中检验气体E的的简单方法是___________
(3)写出实验室中加热混合物的方法制备C的反应的离子方程式:___________
(4)写出反应④的化学方程式___________
(5)一定量E、C混合恰好完全反应且产生白烟,则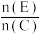 的范围为
的范围为___________

(1)G的电子式是
(2)在实验室中检验气体E的的简单方法是
(3)写出实验室中加热混合物的方法制备C的反应的离子方程式:
(4)写出反应④的化学方程式
(5)一定量E、C混合恰好完全反应且产生白烟,则
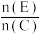 的范围为
的范围为
您最近一年使用:0次
解题方法
10 . X、Y、Z、W、Q五种元素的原子序数依次增大,X原子的半径最小;Y的单质在空气中含量最大;元素Z的焰色在浓雾中最具穿透性;含元素W的化合物很多具有漂白性;Q是最常见金属,位于周期表过渡区。回答问题:
(1)X与Z的化合物 与水反应转移的电子数为
与水反应转移的电子数为____________ 。
(2)用Y的某化合物可检查输送液态W单质的管道是否泄漏,其化学方程式为____________ 。
(3)检查某常见固体物质为 的操作为
的操作为_______________ 。
(4)Q位于周期表的第_________ 周期第________ 族,其单质 溶于
溶于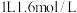 稀硝酸中(只被还原为
稀硝酸中(只被还原为 )的化学方程式为
)的化学方程式为______________ 。
(1)X与Z的化合物
 与水反应转移的电子数为
与水反应转移的电子数为(2)用Y的某化合物可检查输送液态W单质的管道是否泄漏,其化学方程式为
(3)检查某常见固体物质为
 的操作为
的操作为(4)Q位于周期表的第
 溶于
溶于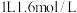 稀硝酸中(只被还原为
稀硝酸中(只被还原为 )的化学方程式为
)的化学方程式为
您最近一年使用:0次



