名校
解题方法
1 . 已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
| A.W与X元素的单质在常温下不反应 |
| B.X、Y、Z、W的原子半径依次减小 |
| C.W的气态氢化物的沸点一定低于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
您最近一年使用:0次
2020-03-26更新
|
63次组卷
|
2卷引用:山西省长治市2019-2020学年高一下学期第一次在线月考化学试题
名校
解题方法
2 . 现有七种短周期主族元素,其原子序数按A、B、C、D、E、F、G的顺序递增。A元素的最高正化合价和最低负化合价的代数和等于0,且A的氧化物能够造成温室效应;A、B、C三种元素都能形成10电子分子,且C与F位于同一主族;D与C可形成离子化合物DC;E的简单阳离子是同周期元素所形成的简单离子中半径最小的。回答下列问题:
(1)B位于周期表第______ 周期第______ 族。
(2)请写出B的氢化物可能的电子式_________ 、_________ 。
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为__________ (用化学式表示)。
(4)A的单质与F的最高价氧化物的水化物浓溶液反应的化学方程式为:_________ 。
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为__________ (用化学式表示)。
(6)下列实验方法能证明D与E的金属性强弱关系的是____ (填字母序号)。
A.比较D和E的单质分别与等浓度的稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物的价态
D.比较D和E最高价氧化物的水化物的碱性强弱
(7)4 mol D 单质与含有10 mol B的最价氧化物的水化物溶液恰好完全,则含有B元素的还原产物可能是_______ 、_________ (写出化学式)。
(1)B位于周期表第
(2)请写出B的氢化物可能的电子式
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为
(4)A的单质与F的最高价氧化物的水化物浓溶液反应的化学方程式为:
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为
(6)下列实验方法能证明D与E的金属性强弱关系的是
A.比较D和E的单质分别与等浓度的稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物的价态
D.比较D和E最高价氧化物的水化物的碱性强弱
(7)4 mol D 单质与含有10 mol B的最价氧化物的水化物溶液恰好完全,则含有B元素的还原产物可能是
您最近一年使用:0次
3 . 表为元素周期表的一部分,表中a~f代表六种短周期主族元素。完成下列填空:
(1)六种元素中,原子半径最大的是_________ (填元素编号) 。d、e、f三种元素的原子结构上的相同点是________________________________ 。
(2)若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是___________ ;六种元素中,最高价氧化物对应水化物的酸性最强的是_________ (填元素符号)。
(3)若f元素的原子L层电子数比M层电子数多1个,则e元素的非金属性比f元素的非金属性_________ (选填“强”、“弱’’),能说明这一事实的化学方程式是____________________ (任写一个)。
(4)若b为非金属元素,则以下推断正确的是_________ (选填编号)。
①a一定是金属元素 ②d一定是金属元素 ③f一定是非金属元素
| a | b | c |
| d | e | f |
(1)六种元素中,原子半径最大的是
(2)若a的气态氢化物的水溶液呈碱性,则a的气态氢化物的电子式是
(3)若f元素的原子L层电子数比M层电子数多1个,则e元素的非金属性比f元素的非金属性
(4)若b为非金属元素,则以下推断正确的是
①a一定是金属元素 ②d一定是金属元素 ③f一定是非金属元素
您最近一年使用:0次
名校
4 . X、Y、Z、W、R属于短周期主族元素。X的最高价氧化物的水化物的碱性是短周期主族元素中最强的,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W元素与Z元素同主族,R元素原子与Y元素原子的核外电子数之比为2:1。下列叙述错误的是( )
| A.X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 |
| B.Z、W、R最高价氧化物对应水化物的酸性强弱:R>W>Z |
| C.Y简单的氢化物比R简单的氢化物稳定,熔沸点高 |
| D.RY2、WY2通入Ba(NO3)2溶液中均无白色沉淀生成 |
您最近一年使用:0次
名校
解题方法
5 . 已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性。下列说法正确的是( )
| A.X、Y、Z、W的原子半径依次减小 |
| B.W与X元素的单质在常温下不反应 |
| C.W的气态氢化物的沸点一定低于Z的气态氢化物的沸点 |
| D.若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 |
您最近一年使用:0次
2020-03-05更新
|
370次组卷
|
2卷引用:河南省安阳市林州市第一中学2019-2020学年高一下学期2月月考化学试题
解题方法
6 . 短周期主族元素A、B、C、D、E的原子序数依次增大,其中A、D同主族,B、C、E分处三个连续的主族,且最外层电子数依次增加。C是地壳中含量最多的元素,C和D可形成两种化合物(阳离子与阴离子个数比均为2:1),A和D也可以形成离子化合物。下列说法错误的是
| A.原子半径:D>E>B>C |
| B.A与其他四种元素形成的二元化合物中其化合价均为+1 |
| C.最高价含氧酸的酸性:E>B |
| D.化合物DCA、DEC的水溶液均显碱性 |
您最近一年使用:0次
解题方法
7 . W、X、Y、Z、R是原子序数依次增大的短周期元素。a、b、c、d、e、f是由这些元素组成的化合物,气体a的水溶液呈碱性,c为红棕色气体,f是由W、Z、R元素形成的化合物。m为元素Z形成的单质,W与X能形成化合物XW4。上述物质的转化关系如图所示,下列说法正确的是( )
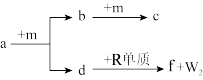
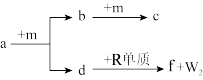
| A.简单离子半径: R>Z |
| B.最高价氧化物对应水化物的酸性:X>Y |
C. 为离子化合物,含有离子键和共价键 为离子化合物,含有离子键和共价键 |
| D.符合通式XnWn的化合物均能使溴的CCl4溶液因发生反应而褪色 |
您最近一年使用:0次
名校
8 . X、Y、Z、W是原子序数依次增大的短周期主族元素,其原子半径依X、Z、Y、W的顺序增大。已知Y的气态氢化物水溶液显碱性、Z是地壳中含量最高的元素,W的原子半径在同周期中最小(稀有气体除外)。下列说法正确的是( )
A.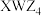 的酸性强于 的酸性强于 ,所以W的非金属性比Y强 ,所以W的非金属性比Y强 |
| B.X、Y分别与Z按原子个数比2∶1形成的化合物都是弱电解质 |
| C.由Y和Z元素形成的氧化物最多可有5种 |
| D.由X、Y、Z元素组成的化合物均为共价化合物 |
您最近一年使用:0次
解题方法
9 . 短周期A、B、C、D 4种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上电子数之和。
(1)元素:A为___________ B为___________ C为___________ D为___________
(2)D在周期表中的位置第______ 周期,第________ 族;它的最高价氧化物对应的水化物:___________
(3)C与水反应的化学方程式是_________________________________ ,所得溶液显___________ (“酸性”或“碱性”)
(1)元素:A为
(2)D在周期表中的位置第
(3)C与水反应的化学方程式是
您最近一年使用:0次
名校
解题方法
10 . 现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
回答下列问题:
(1)①在元素周期表中的位置是____ 。写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是____ ;碱性最强的化合物属于化合物____ (填“离子”或“共价”)。
(3)比较④和⑦的氢化物的稳定性____ (用化学式表示)。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)①在元素周期表中的位置是
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)比较④和⑦的氢化物的稳定性
您最近一年使用:0次



