2019·山东青岛·二模
名校
解题方法
1 . 前20号元素X、Y、Z、W、R原子序数依次增大。其中X、Z、R最外层电子数相等,且X与Z、R均可形成离子化合物;Y、W同主族,Y最外层电子数是内层电子数的3倍。下列说法正确的是( )
| A.元素原子半径大小顺序为:r(W)> r(Z)> r(Y) |
| B.X分别与Y、Z、W形成的常见化合物都属于电解质 |
| C.Y分别与Z、R形成的化合物中均只含有离子键 |
| D.Y分别与Z、W均可形成具有漂白性的化合物,且漂白原理相同 |
您最近一年使用:0次
2019-12-16更新
|
156次组卷
|
6卷引用:【南昌新东方】2019 新建一中 高三期中 015
(已下线)【南昌新东方】2019 新建一中 高三期中 015【市级联考】山东省青岛市2019届高三下学期5月第二次模考理科综合化学试题(已下线)专题06 物质结构 元素周期律——2019年高考真题和模拟题化学分项汇编辽宁省抚顺市第一中学2020届高三上学期期中考试化学试题陕西省西安中学2020届高三上学期第三次月考化学试题安徽省太和第一中学2019-2020学年高二下学期教学衔接调研考试(飞越班)化学试题
名校
解题方法
2 . A、B、C、D是四种短周期元素,它们的原子序数依次增大,其中,A、C及B、D分别是同主族元素;A元素的原子半径是所有主族元素中原子半径最小的;B、D两元素的原子核中质子数之和是A、C两元素原子核中质子数之和的2倍;四种元素所形成的单质中A、B单质是气体,C、D单质是固体。
(1)写出以下元素的名称:B________________ ;C______________ 。
(2)写出D元素在周期表中的位置___________________________
(3)用电子式表示C2D的形成过程:_______________________________
(4)写出由B、C两元素所形成的原子个数比为1:1的化合物的的电子式_______ ;属于_______ (填“离子”或“共价”)化合物,存在的化学键的种类有______________________ ;写出它与水反应的离子方程式_______________________________
(1)写出以下元素的名称:B
(2)写出D元素在周期表中的位置
(3)用电子式表示C2D的形成过程:
(4)写出由B、C两元素所形成的原子个数比为1:1的化合物的的电子式
您最近一年使用:0次
解题方法
3 . W、X、Y、Z是原子序数依次最大的短周期元素,W的原子半径最小,W、Y同主族,X、Z同主族,X、Z的原子序数之和是W、Y原子序数之和的2倍,下列说法中不正确的是
| A.由X、Y、Z三种元素形成的化合物只能为Y2ZX3或Y2ZX4 |
| B.由W和X两种元素形成的化合物可能含有非极性共价键 |
| C.由W、X、Y、Z四种元素形成的化合物水溶液可能呈强酸性 |
| D.W、X、Y、Z四种元素两两之间形成二元化合物 |
您最近一年使用:0次
名校
4 . 下表为元素周期表中短周期的一部分,其中Y元素的原子序数为M与N元素原子序数之和。下列说法正确的是
| M | N | ||
| X | Y | Z |
| A.氢化物的稳定性:N >Z,是因为其氢化物分子间可形成氢键 |
| B.元素的非金属性:M > Y,是因为元素M形成的化合物种类比元素Y更多 |
| C.熔沸点:YN2>MN2,是因为YN2的分子间作用力更强 |
| D.简单离子的半径:N >X,是因为它们具有相同的电子层结构且X的核电荷数更大 |
您最近一年使用:0次
2018-05-29更新
|
201次组卷
|
2卷引用:【全国百强校】江西省南昌市第二中学2017-2018学年高一下学期第二次月考化学试题
名校
5 . X、Y和Z是短周期的三种元素,已知X元素原子的最外层只有一个电子,Y元素原子M层上的电子数是K层和L层电子总数的一半,Z元素原子L层上的电子数比Y元素原子L层上电子数少2个,则这三种元素所组成的化合物的化学式不可能是 ( )。
| A.X2YZ4 | B.X3YZ3 | C.X3YZ4 | D.XYZ3 |
您最近一年使用:0次
2011·江西·二模
6 . 已知X、Y和Z三种元素的原子序数之和等于48。X的一种1∶1型氢化物分子中既有σ键又有π键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单元为正方体(如图),边长为4.03×10-10 m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
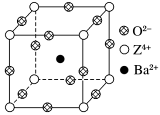
(1) Y在周期表中位于______________ ;Z4+的核外电子排布式为___________________ 。
(2)X的该种氢化物分子构型为________ ,X在该氢化物中以_______ 方式杂化。X和Y形成的化合物的熔点应该_______ (填“高于”或“低于”)X的氢化物的熔点。
(3)①制备M的化学方程式是_____________ 。
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的________ 。
③在M晶体中,Z4+的氧配位数为________ 。
④已知O2-半径为1.40×10-10 m,则Z4+半径为____ m。

(1) Y在周期表中位于
(2)X的该种氢化物分子构型为
(3)①制备M的化学方程式是
②在M晶体中,若将Z4+置于正方体的体心,Ba2+置于正方体的顶点,则O2-处于正方体的
③在M晶体中,Z4+的氧配位数为
④已知O2-半径为1.40×10-10 m,则Z4+半径为
您最近一年使用:0次
2016-12-09更新
|
1125次组卷
|
5卷引用:2011届江西省重点中学协作体高三第二次联考(理综)化学部分
(已下线)2011届江西省重点中学协作体高三第二次联考(理综)化学部分苏教版2017届高三单元精练检测十一化学试题黑龙江省齐齐哈尔市第八中学2017-2018学年高二6月月考化学试题山东省章丘市第四中学2019届高三上学期第二次质量检测理综化学试题新疆奎屯市第一高级中学2018-2019学年高二下学期第一次月考化学试题
解题方法
7 . 短周期元素X、Y、Z、W、M的原子序数依次增大,元素X与W位于同一主族,Z元素的单质既能与盐酸反应又能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半, M的最高正价与最低负价的绝对值之差为4,五种元素原子的最外层电子数之和为19, 下列说法正确的是( )
| A.简单气态氢化物的稳定性:W>X |
| B.简单离子半径由大到小的顺序:Y>Z>M |
| C.M的气态氢化物是弱电解质 |
| D.Y、Z元素的单质作电极,在NaOH溶液环境下构成原电池,Z电极上产生大量气泡 |
您最近一年使用:0次
名校
8 . 短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。Y原子的质子数为Z原子的质子数的一半,W原子的最外层电子数比Y原子的最外层电子数多2个。下列叙述正确的是( )
| A.Y的最高价氧化物对应的水化物可与其简单气态氢化物发生反应 |
| B.原子半径:Z>W>Y>X |
| C.简单气态氢化物的稳定性:Z>W |
| D.X的简单气态氢化物与足量W的单质在光照条件下反应的生成物均为气体 |
您最近一年使用:0次
2017-07-12更新
|
419次组卷
|
4卷引用:江西省上饶县中学2016-2017学年高一下学期期末考试化学试题
名校
解题方法
9 . 如图是元素周期表的一部分,A、B、C均为短周期元素,A、C两种元素的原子核外电子数之和等于B的质子数,B的原子核内质子数和中子数相等。回答:
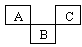
(1)写出元素符号:A____ ;C_____ 。
(2)B的最高价氧化物对应水化物的化学式为____ 。
(3)A的单质的电子式为___ ;A的氢化物的水溶液与其最高价氧化物的水化物反应的化学方程式____ 。

(1)写出元素符号:A
(2)B的最高价氧化物对应水化物的化学式为
(3)A的单质的电子式为
您最近一年使用:0次
2017-07-13更新
|
278次组卷
|
3卷引用:江西省鄱阳县第二中学2018-2019学年高一下学期期中考试化学试题
名校
10 . 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外最外层共有24个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同
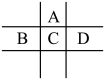
回答下列问题:
(1) A与E形成的化合物的化学式是__________ .B的最高价氧化物化学式为_____________ ,
(2)D的单质与水反应的方程式为__________________________________________________ .
(3) 向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是___________________ :有关反应的离子方程式为:_____________________________________ .
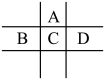
回答下列问题:
(1) A与E形成的化合物的化学式是
(2)D的单质与水反应的方程式为
(3) 向D与E形成的化合物的水溶液中滴入烧碱溶液直至过量,观察到的现象是
您最近一年使用:0次
2019-04-22更新
|
111次组卷
|
2卷引用:江西省新余市分宜中学2018-2019学年高一下学期第二次段考化学试题



