名校
解题方法
1 . 2008年北京奥运会的“水立方”,在2022年冬奥会上华丽转身为“冰立方”,实现了奥运场馆的再利用,其美丽的透光气囊材料由乙烯 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。
(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
(2)第三周期元素的原子中,未成对电子不可能有_______。
(3)基态F原子的轨道表示式为_______ ,四氟乙烯的电子式为_______ 。
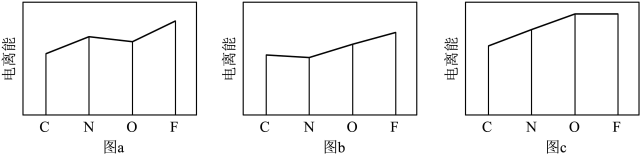
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是_______ (填字母),第三电离能的变化图是_______ (填字母)。
(5) 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为_______ 和_______ ;聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因_______ 。
(6)比较甲醚和乙醇的沸点高低,并说明理由_______ 。
 与四氟乙烯
与四氟乙烯 的共聚物
的共聚物 制成。
制成。(1)2015年2月,科学家首次观测到化学键的形成。化学键不存在于_______。
| A.原子与原子之间 | B.分子与分子之间 | C.离子与离子之间 | D.离子与电子之间 |
(2)第三周期元素的原子中,未成对电子不可能有_______。
| A.4个 | B.3个 | C.2个 | D.1个 |
(3)基态F原子的轨道表示式为
(4)图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是

(5)
 和
和 分子中C的杂化轨道类型分别为
分子中C的杂化轨道类型分别为(6)比较甲醚和乙醇的沸点高低,并说明理由
您最近一年使用:0次
名校
解题方法
2 . 随着原子序数的递增,7种短周期元素A~G的最高正价或最低负价与原子序数的关系如图。
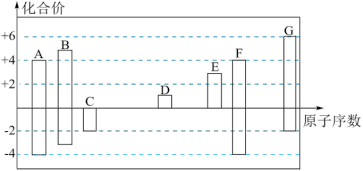
回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号_______ 。
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为_______ 。
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为_______ 。
(4)元素A与G形成的电子总数为38的分子的结构式为_______ 。
(5)元素C与D按原子个数比1:1形成的化合物的电子式为_______ ,所含有化学键类型有_______ 。
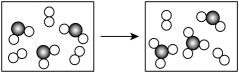
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:_______ 。

回答下列问题:
(1)写出中子数为8的A元素的一种核素的化学符号
(2)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(3)E元素最高价氧化物对应水化物与氢氧化钠溶液反应的离子方程式为
(4)元素A与G形成的电子总数为38的分子的结构式为
(5)元素C与D按原子个数比1:1形成的化合物的电子式为
(6)如图表示由C、G元素组成的两种气体分子在一定条件下的密闭容器中充分反应的转化关系,请写出该转化过程的化学方程式:

您最近一年使用:0次
20-21高二·全国·课时练习
解题方法
3 . 有A、B、C、D、E 5种元素,它们的核电荷数依次增大,且都小于20。其中C、E是金属元素;A和E属于同一族,它们原子的最外层电子排布为ns1。B和D也属于同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。A、B、C、D、E五种元素的电负性分别为2.5、3.5、0.8、2.1、1.5中的一种,请回答下列问题:
(1)A是___________ (用元素符号填空,下同),B是___________ ,C是___________ ,D是___________ ,E是___________ 。
(2)A、B、C、D、E的电负性分别为:A___________ ,B___________ ,C___________ ,D___________ ,E___________ 。
(3)由电负性判断,以上五种元素中金属性最强的是___________ ,非金属性最强的是___________ (填元素符号)。
(4)当B与A、C、D分别形成化合物时,B显___________ 价,其他元素显___________ 价(填“正”或“负”)。
(5)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是___________ ,有共价键的是___________ 。
(1)A是
(2)A、B、C、D、E的电负性分别为:A
(3)由电负性判断,以上五种元素中金属性最强的是
(4)当B与A、C、D分别形成化合物时,B显
(5)当B与A、C、D、E(与E形成E2B)分别形成化合物时,化合物中有离子键的是
您最近一年使用:0次
名校
解题方法
4 . A、B、C、D四种元素的核电荷数依次增大,且均不超过18。A元素的原子核外只有一个电子,B元素原子K层电子数是L层电子数的一半,C元素的原子最外层电子数是次外层电子数的3倍,D元素原子的M层只有一个电子。
(1)B元素的名称是_______ ,C元素的名称是_______ 。
(2)A、C两元素组成化合物的电子式为_______ 。
(3)A、C、D三种元素组成化合物的电子式是_______ 。该化合物含有化学键类型为_______ 。
(1)B元素的名称是
(2)A、C两元素组成化合物的电子式为
(3)A、C、D三种元素组成化合物的电子式是
您最近一年使用:0次
5 . 黄铜矿是主要的炼铜原料, 是其中铜的主要存在形式。回答下列问题:
是其中铜的主要存在形式。回答下列问题:
(1) 中存在的化学键类型是
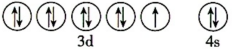
中存在的化学键类型是___________ 。下列基态原子或离子的价层电子轨道表示式正确的是___________ (填标号)。
A. :
:
B. :
:
C. :
:
D. :
:
(2)在较低温度下 与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
①X分子的空间结构是___________ ,中心原子杂化类型为___________ ,属于___________ (填“非极性”或“极性”)分子。
②X的沸点比水低的主要原因是___________ 。
(3) 与氧气反应生成
与氧气反应生成 。
。 中心原子的价层电子对数为
中心原子的价层电子对数为___________ ,共价键的类型有___________ 。
(4)四方晶系 的晶胞结构如图所示。
的晶胞结构如图所示。
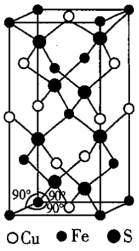
已知: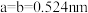 ,
, ,
, 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 晶体的密度是
晶体的密度是___________  (列出计算式)。
(列出计算式)。
 是其中铜的主要存在形式。回答下列问题:
是其中铜的主要存在形式。回答下列问题:(1)
 中存在的化学键类型是
中存在的化学键类型是A.
 :
:
B.
 :
:
C.
 :
:
D.
 :
:
(2)在较低温度下
 与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。
与浓硫酸作用时,有少量臭鸡蛋气味的气体X产生。①X分子的空间结构是
②X的沸点比水低的主要原因是
(3)
 与氧气反应生成
与氧气反应生成 。
。 中心原子的价层电子对数为
中心原子的价层电子对数为(4)四方晶系
 的晶胞结构如图所示。
的晶胞结构如图所示。
已知:
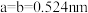 ,
, ,
, 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 晶体的密度是
晶体的密度是 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解题方法
6 . 有三种物质 、
、 、
、 在常温下三者分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,且火焰呈黄色,并生成淡黄色固体
在常温下三者分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,且火焰呈黄色,并生成淡黄色固体 ;元素D的负一价阴离子的电子层结构与氩原子相同。则:
;元素D的负一价阴离子的电子层结构与氩原子相同。则:
(1)元素A、B、C、D的名称分别为_______ 、_______ 、_______ 、_______ 。
(2) 分子中含有的化学键类型为
分子中含有的化学键类型为_______ (填“极性键”或“非极性键”)。
(3)D的负一价阴离子的核外电子排布式为____ , 属于
属于___ (填“离子”或“共价”)化合物。
 、
、 、
、 在常温下三者分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,且火焰呈黄色,并生成淡黄色固体
在常温下三者分别为气体、固体和液体。元素A的最高正价和最低负价的绝对值相等;元素B的单质能在C的气态单质中剧烈燃烧,且火焰呈黄色,并生成淡黄色固体 ;元素D的负一价阴离子的电子层结构与氩原子相同。则:
;元素D的负一价阴离子的电子层结构与氩原子相同。则:(1)元素A、B、C、D的名称分别为
(2)
 分子中含有的化学键类型为
分子中含有的化学键类型为(3)D的负一价阴离子的核外电子排布式为
 属于
属于
您最近一年使用:0次
解题方法
7 . 向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。
(1)写出H2O分子的电子式:___ 。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是________ 。
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)写出铜原子价电子层的电子排布式:___ ,与铜同一周期副族元素的基态原子中最外层电子数与铜原子相同的元素有___ (填元素符号)。
(4)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有___ 。
(5)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4•H2O晶体。实验中所加C2H5OH的作用是___ 。
(1)写出H2O分子的电子式:
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是
A.氧原子的杂化类型发生了改变
B.微粒的形状发生了改变
C.微粒的化学性质发生了改变
D.微粒中的键角发生了改变
(3)写出铜原子价电子层的电子排布式:
(4)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有
(5)实验过程中加入C2H5OH后可观察到析出深蓝色Cu(NH3)4SO4•H2O晶体。实验中所加C2H5OH的作用是
您最近一年使用:0次
20-21高一上·全国·课时练习
8 . 某融雪剂的主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1 mol XY2 含有54 mol电子。
(1)该融雪剂的化学式是_____ ,该物质中化学键类型是______ ,电子式是_______ 。
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是_______ ;D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8e-稳定结构,该分子的结构式为_______ ,电子式为______ ,化学键类型为______ (填“离子键”“非极性共价键”或“极性共价键”)。
(1)该融雪剂的化学式是
(2)元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图是
您最近一年使用:0次
解题方法
9 . 已知 A、B、C、D、E 是五种短周期的主族元素,它们的原子序数依次增大, A 是所有元素中原子半径最小的元素,B、C 组成的某一种化合物能引起温室效应;常温下, 金属 D 单质投入水中能与水剧烈反应;E 的单质在常温下是一种有色的气体。请按要求回答下列几个问题:
(1)B、D 的元素名称分别为:_____ 、_____ ;
(2)E 的最高价氧化物对应的水化物的化学式为:_____ ;
(3)C 离子的结构示意图为:_____ ;
(4)B、C、D 三种元素的原子半径从大到小的顺序为_____ (用元素符号表示);
(5)B、E 的最高价氧化物对应水化物的酸性从强到弱的顺序为:_____ (用对应的化学式表示)
(6) 写出 C、D 两种元素组成的阴、阳离子个数比为 1:2 且既含离子键又含有非极性共价键的化合物的电子式:_____ 。
(1)B、D 的元素名称分别为:
(2)E 的最高价氧化物对应的水化物的化学式为:
(3)C 离子的结构示意图为:
(4)B、C、D 三种元素的原子半径从大到小的顺序为
(5)B、E 的最高价氧化物对应水化物的酸性从强到弱的顺序为:
(6) 写出 C、D 两种元素组成的阴、阳离子个数比为 1:2 且既含离子键又含有非极性共价键的化合物的电子式:
您最近一年使用:0次
名校
解题方法
10 . 在遭遇冰雪灾害时,常使用一种融雪剂其主要成分的化学式为XY2,X、Y均为周期表前20号元素,其阳离子和阴离子的电子层结构相同,且1molXY2含有54mol电子。
(1)该融雪剂的化学式是___ ,电子式是___ ,该物质中化学键类型是__ 。
(2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图___ ;是D与E能形成一种结构类似于CO2的三原子分子,且每个原子均达到了8电子稳定结构,该分子的电子式为___ ,化学键类型为___ (填“离子键”或“共价键”)。
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成___ ,其化学键类型为___ ;加热时生成___ ,其化学键类型为____ ,电子式为___ 。
(1)该融雪剂的化学式是
(2)主族元素D、E原子的最外层电子数是其电子层数的2倍,D与Y相邻,则D的离子结构示意图
(3)W是与D同主族的短周期元素,Z是第三周期金属性最强的元素,Z的单质在W的常见单质中反应时有两种产物:不加热时生成
您最近一年使用:0次
2020-10-10更新
|
431次组卷
|
9卷引用:人教版2017-2018学年高一化学必修二同步训练:第一章 物质结构 元素周期律
人教版2017-2018学年高一化学必修二同步训练:第一章 物质结构 元素周期律北京市人大附中2017-2018学年下学期高一第一次月考 化学试卷山西省祁县中学2017-2018学年高一下学期第一次月考化学试题人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第三节 化学键高一必修第一册(苏教2019)专题5 第二单元 微粒之间的相互作用力2(已下线)4.3.1 离子键(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)黑龙江省讷河市拉哈一中2020-2021学年高一下学期3月月考化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020-2021学年高一上学期期末化学试题(已下线)易错专题29 化学键-【突破易错·冲刺满分】2021-2022学年高一上学期化学期中期末易错专题(人教版2019)



