名校
解题方法
1 . 下列叙述中正确的是
| A.含离子键的化合物一定是离子化合物 |
| B.含共价键的化合物一定是共价化合物 |
| C.全部由非金属元䋈组成的化合物一定是共价化合物 |
| D.在离子化合物中不可能有共价键 |
您最近一年使用:0次
2024-02-02更新
|
0次组卷
|
2卷引用:上海市建平中学2023-2024学年高一上学期期末教学质量检测化学试卷
名校
2 . 元素周期律
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
(2) 的电子式正确的是________
的电子式正确的是________
(3)有关N、O两种元素,下列排序错误的是________
(4)甲~戊均为短周期元素,在元素周期表中的相对位置如图所示。戊的最高价氧化物对应的水化物为强酸。下列说法不正确的是________
基于元素之间具有内在联系的思想,通过对元素性质及其关系的探寻,元素周期律已成为将物质组成元素性质以及原子结构建立联系的连接点。
(1)下列不属于主族元素的是________
A. | B. | C. | D. |
 的电子式正确的是________
的电子式正确的是________A.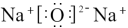 | B. |
C.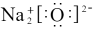 | D. |
| A.元素的最高化合价:O>N | B.简单氢化物的稳定性: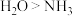 |
| C.元素的电负性:O>N | D.离子半径: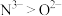 |
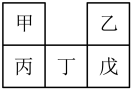
| A.原子半径:丁>戊>乙 |
| B.非金属性:戊>丁>丙 |
| C.甲的氢化物遇氯化氢一定有白烟产生 |
| D.丙的最高价氧化物对应的水化物一定能与强碱反应 |
您最近一年使用:0次
名校
3 . 元素周期表的表达形式有多种,但都能表示出元素的周期性变化规律,请回答下列问题:
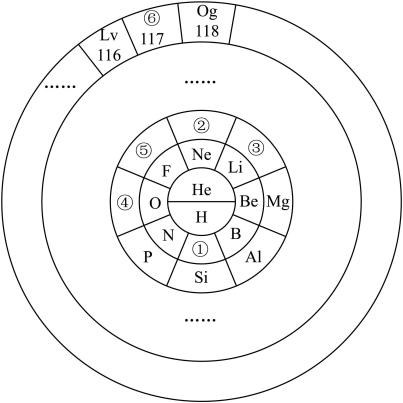
(1)①与④元素形成的化合物属于___________ 晶体。
(2)写出③的最高价氧化物对应水化物和Al的最高价氧化物的水化物相互反应的离子方程式:__________ 。
(3)②号元素为___________ (填元素符号)。请写出1个与②核外电子数相同的简单离子组成的化合物的化学式:___________ 。其中存在的化学键属于___________ 键,该物质在熔融状态下___________ 导电(填“能”或“不能”)。
(4)⑤的单质具有较强的氧化性,能与大多数金属发生反应,请写出⑤的单质与过量的铁粉反应的化学方程式:___________ ,将反应所得混合物溶于水,得到浅绿色的溶液,请写出相关的离子方程式:___________ 。
(5)其中非金属性④___________ ⑤(填“>”或“<”),请用一个化学方程式证明___________ 。
(6)⑥(原子序数117)的单质是一种具有放射性的卤族元素,它在元素周期表中的位置为___________ ,根据元素的周期性规律,以下推测正确的是________
A.单质在常温下为气体 B.气态氢化物的稳定性较好
C.离子具有强还原性 D.半径大于⑤

(1)①与④元素形成的化合物属于
(2)写出③的最高价氧化物对应水化物和Al的最高价氧化物的水化物相互反应的离子方程式:
(3)②号元素为
(4)⑤的单质具有较强的氧化性,能与大多数金属发生反应,请写出⑤的单质与过量的铁粉反应的化学方程式:
(5)其中非金属性④
(6)⑥(原子序数117)的单质是一种具有放射性的卤族元素,它在元素周期表中的位置为
A.单质在常温下为气体 B.气态氢化物的稳定性较好
C.离子具有强还原性 D.半径大于⑤
您最近一年使用:0次
名校
4 . 已知X、Y、Z、M四种主族元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成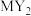 、
、 两种分子,其中
两种分子,其中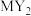 可以使红色的品红溶液褪色。
可以使红色的品红溶液褪色。
(1)画出Y的原子结构示意图___________ ,写出离子化合物ZX的电子式___________ ;
(2)由X、Y、Z、M四种元素组成的一种固体化合物,属于强电解质,溶于水的过程中破坏了______。
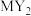 、
、 两种分子,其中
两种分子,其中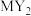 可以使红色的品红溶液褪色。
可以使红色的品红溶液褪色。(1)画出Y的原子结构示意图
(2)由X、Y、Z、M四种元素组成的一种固体化合物,属于强电解质,溶于水的过程中破坏了______。
| A.离子键 | B.金属键 |
| C.共价键 | D.分子间作用力 |
您最近一年使用:0次
名校
解题方法
5 . 氮的循环对人类的生产和生活具有重要意义,如图所示的氮循环是生态系统物质循环的重要组成部分。
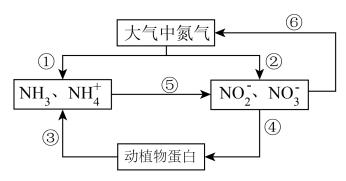
(1)下列说法中错误的是________。
(2)以氨气为原料制备两种常见氮肥的反应如下:
a.NH3+H2O+CO2=NH4HCO3 b.2NH3+CO2 H2O+CO(NH2)2
H2O+CO(NH2)2
上述两个反应所涉及的化合物中,属于离子化合物的是____ 。
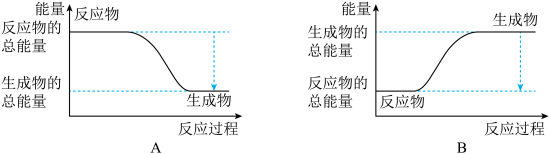
(3)工业合成氨的反应如下:N2+3H2 2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN-H键放出的能量为391kJ,则由N2和H2生成2molNH3的能量变化为
2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN-H键放出的能量为391kJ,则由N2和H2生成2molNH3的能量变化为________ kJ。如图能正确表示该反应中能量变化的是______ (填“A”或“B”)。

(1)下列说法中错误的是________。
| A.图中①和②的转化过程属于氮的固定 |
| B.③和④的转化说明含氮有机物和含氮无机物可以相互转化 |
| C.发生⑤转化的过程中,氮元素被氧化 |
| D.⑥是在反硝化细菌作用下的反硝化过程,该过程无助于弥补人工固氮对氮循环造成的影响 |
a.NH3+H2O+CO2=NH4HCO3 b.2NH3+CO2
 H2O+CO(NH2)2
H2O+CO(NH2)2上述两个反应所涉及的化合物中,属于离子化合物的是
(3)工业合成氨的反应如下:N2+3H2
 2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN-H键放出的能量为391kJ,则由N2和H2生成2molNH3的能量变化为
2NH3。已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molN-H键放出的能量为391kJ,则由N2和H2生成2molNH3的能量变化为
您最近一年使用:0次
名校
6 . 下列化学用语描述不正确的是
A.可用于考古断代的一种核素的符号: |
B. 的电子式: 的电子式: |
C.钠离子的结构示意图: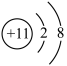 |
D.用电子式表示 的形成过程为: 的形成过程为: |
您最近一年使用:0次
2023-03-07更新
|
506次组卷
|
6卷引用:上海外国语大学附属大境中学2022-2023学年高一下学期期末考试化学试题
解题方法
7 . 化学键类型、晶体类型都相同的是
| A.CO2和NH4Cl | B.NaBr和CaCl2 | C.KOH和NaCl | D.SiO2和H2O |
您最近一年使用:0次
名校
解题方法
8 . 下列固体熔化时破坏共价键的是
| A.冰 | B.铝 | C.二氧化硅 | D.烧碱 |
您最近一年使用:0次
名校
9 . 下列物质发生所述变化时,所克服的微粒间作用力,属于同类型的是
| A.干冰和碘的升华 | B.NaBr和HI分别在水中电离 |
C. 和CaO的熔化 和CaO的熔化 | D.将氯化氢和乙醇分别加入水中 |
您最近一年使用:0次
名校
10 . 下列叙述中,正确的是
| A.由共价键构成的物质一定是共价化合物 |
| B.只有金属元素和非金属元素化合时才能形成离子键 |
| C.晶体中不一定存在化学键 |
| D.共价化合物可能含离子键,离子化合物可能含共价键 |
您最近一年使用:0次



