名校
1 . 电负性用来描述不同元素的原子对键合电子吸引力的大小,是元素的一种基本性质。下表为一些元素的电负性(已知两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键):
下列说法不正确的是
| 元素 | Li | Be | B | C | N | F | Na | Mg | Al | Si | Cl | Ca |
| 电负性 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 | 4.0 | 0.9 | a | 1.5 | 1.8 | 3.0 | 1.0 |
| A.根据电负性变化规律,确定a的最小范围为1.0<a<1.5 |
| B.NF3中N-F键的极性比NCl3中N-Cl键的极性强 |
| C.AlCl3是一种可溶性盐,属于离子化合物 |
| D.可以通过测定化合物在熔融状态下是否导电鉴别Li3N与SiC |
您最近一年使用:0次
2024-02-22更新
|
201次组卷
|
4卷引用:安徽省皖中联盟考试2023-2024学年高二上学期1月期末化学试题
解题方法
2 . 下表是元素周期表的一部分,表中所列的 分别代表一种元素.
分别代表一种元素.
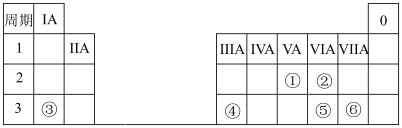
回答下列问题:
(1)①的原子结构示意图为____________ 。
(2)②和⑤中原子半径较大的是____________ (填元素符号);③和④的最高价氧化物对应的水化物中碱性较强的是____________ (填化学式)。
(3)④的单质在强碱溶液中反应的离子方程式为____________ 。
(4)用电子式表示③和⑥形成化合物的过程____________ ;实验室用该化合物配制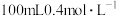 的溶液,下列实验仪器需要用到的是
的溶液,下列实验仪器需要用到的是____________ (填标号),若在配制时仰视容量瓶上的刻度线,则所配溶液物质的量浓度会____________ (填“偏大”、“偏小”或“不变”)。
A. B.
B.  C.
C.  D.
D.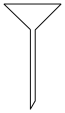
 分别代表一种元素.
分别代表一种元素.
回答下列问题:
(1)①的原子结构示意图为
(2)②和⑤中原子半径较大的是
(3)④的单质在强碱溶液中反应的离子方程式为
(4)用电子式表示③和⑥形成化合物的过程
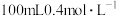 的溶液,下列实验仪器需要用到的是
的溶液,下列实验仪器需要用到的是A.
 B.
B.  C.
C.  D.
D.
您最近一年使用:0次
解题方法
3 . ①~⑪11种元素在元素周期表中的位置如下表所示:
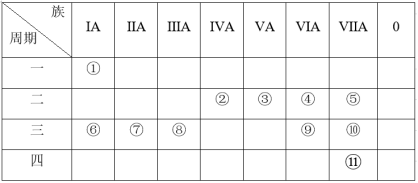
回答下列问题:
(1)元素②最高价氧化物的电子式为________ ,元素③的单质分子结构式为_____ 。
(2)在盛有水的小烧杯中加入少量元素⑥的单质,发生反应的化学方程式为________ 。
(3)元素⑥⑧最高价氧化物对应水化物反应的离子方程式为___________ 。
(4)在第三周期元素形成的简单离子中,半径最小的是______ (填离子符号);②③④⑤四种元素的简单氢化物沸点最高的是_______ (填化学式)。
(5)下列事实不能说明⑩的非金属性比⑨的非金属性强的是______(填字母)。
(6)①④⑥三种元素形成的化合物中含有的化学键类型为_______ ;⑪的最高价氧化物对应的水化物为________ (填化学式)。
(7)用电子式表示元素⑥与⑨形成化合物的过程:___________ 。

回答下列问题:
(1)元素②最高价氧化物的电子式为
(2)在盛有水的小烧杯中加入少量元素⑥的单质,发生反应的化学方程式为
(3)元素⑥⑧最高价氧化物对应水化物反应的离子方程式为
(4)在第三周期元素形成的简单离子中,半径最小的是
(5)下列事实不能说明⑩的非金属性比⑨的非金属性强的是______(填字母)。
| A.将⑩的单质通入⑨的气态氢化物的溶液中,有淡黄色沉淀产生 |
| B.⑨的单质不能与水反应,⑩的单质可以与水反应 |
| C.⑨的单质与Fe化合时产物中Fe为+2价,⑩的单质与Fe化合时产物中Fe为+3价 |
| D.⑩的气态氢化物的沸点高于⑨的 |
(7)用电子式表示元素⑥与⑨形成化合物的过程:
您最近一年使用:0次
2024-01-30更新
|
108次组卷
|
2卷引用:安徽省阜阳市2023-2024学年高一上学期期末联考化学试卷
解题方法
4 . 下列物质中既含有离子键又含有共价键的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
5 . 解答下列问题:
(1)2017年中科院某研究团队通过设计一种新型Na—Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+ O2(g)=H2O(l) ΔH1=-akJ·mol-1
O2(g)=H2O(l) ΔH1=-akJ·mol-1
C8H18(l)+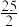 O2(g)=8CO2(g)+9H2O(l) ΔH2=-bkJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH2=-bkJ·mol-1
试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式:___________ 。
(2)直接排放含SO2的烟气会形成酸雨,危害环境。工业上常用催化还原法和碱吸收法处理SO2气体。1molCH4完全燃烧生成气态水和1molS(g)燃烧的能量变化如下图所示:

在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:___________ 。
(3)合成氨在工业生产中具有重要意义。在合成氨工业中I2O5常用于定量测定CO的含量。
已知2I2(s)+5O2(g)=2I2O5(s) ΔH=-76kJ·mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1。
则该测定反应的热化学方程式为___________ 。
(4)化学反应原理研究物质转化过程中的规律并在生产生活中有广泛的应用。汽车排气管内的催化转化器可实现尾气无毒处理。
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
CO2(g)=C(s)+O2(g) ΔH=+393.5kJ·mol-1
则反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的ΔH=___________ kJ·mol-1。
(5)氮及其化合物与人类生产、生活密切相关。氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用CO还原NO2至N2,当消耗标准状况下3.36LCO时,放出的热量为___________ kJ(用含有a和b的代数式表示)。
(6)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析, 晶体中所含化学键的类型有
晶体中所含化学键的类型有___________ ,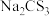 水溶液显
水溶液显___________ (填“酸性”、“碱性”或“中性”)。
(1)2017年中科院某研究团队通过设计一种新型Na—Fe3O4/HZSM-5多功能复合催化剂,成功实现了CO2直接加氢制取辛烷值汽油,该研究成果被评价为“CO2催化转化领域的突破性进展”。
已知:H2(g)+
 O2(g)=H2O(l) ΔH1=-akJ·mol-1
O2(g)=H2O(l) ΔH1=-akJ·mol-1C8H18(l)+
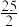 O2(g)=8CO2(g)+9H2O(l) ΔH2=-bkJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH2=-bkJ·mol-1试写出25℃、101kPa条件下,CO2与H2反应生成汽油(以C8H18表示)的热化学方程式:
(2)直接排放含SO2的烟气会形成酸雨,危害环境。工业上常用催化还原法和碱吸收法处理SO2气体。1molCH4完全燃烧生成气态水和1molS(g)燃烧的能量变化如下图所示:

在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式:
(3)合成氨在工业生产中具有重要意义。在合成氨工业中I2O5常用于定量测定CO的含量。
已知2I2(s)+5O2(g)=2I2O5(s) ΔH=-76kJ·mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1。
则该测定反应的热化学方程式为
(4)化学反应原理研究物质转化过程中的规律并在生产生活中有广泛的应用。汽车排气管内的催化转化器可实现尾气无毒处理。
已知:N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221.0kJ·mol-1
CO2(g)=C(s)+O2(g) ΔH=+393.5kJ·mol-1
则反应2NO(g)+2CO(g)=N2(g)+2CO2(g)的ΔH=
(5)氮及其化合物与人类生产、生活密切相关。氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
已知:CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用CO还原NO2至N2,当消耗标准状况下3.36LCO时,放出的热量为
(6)氮元素、硫元素还能形成多种化合物。如汽车安全气囊中的填充物叠氮酸钠(NaN3),能用于处理废水中的重金属离子的硫代碳酸钠(Na2CS3)。根据所学化学知识分析,
 晶体中所含化学键的类型有
晶体中所含化学键的类型有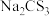 水溶液显
水溶液显
您最近一年使用:0次
6 . 汽车受到猛烈碰撞时,安全气囊内的 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法正确的是
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法正确的是

 固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法正确的是
固体迅速分解,产生氮气和金属钠,该过程中的能量变化如图所示。下列说法正确的是
A. 属于共价化合物 属于共价化合物 |
B. 的分解反应属于吸热反应 的分解反应属于吸热反应 |
C. 表示 表示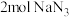 固体的能量 固体的能量 |
D. 作为气体发生剂,具有产气快、产气量大等优点 作为气体发生剂,具有产气快、产气量大等优点 |
您最近一年使用:0次
名校
解题方法
7 . 下列物质中化学键类型完全相同的是
A. , , | B.NaBr, |
C.NaCl, | D. ,KI ,KI |
您最近一年使用:0次
2023-03-09更新
|
395次组卷
|
2卷引用:安徽省芜湖市2022-2023学年高一上学期期末教学质量统测化学试题
名校
8 . 下列化学用语描述不正确的是
A.可用于考古断代的一种核素的符号: |
B. 的电子式: 的电子式: |
C.钠离子的结构示意图: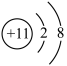 |
D.用电子式表示 的形成过程为: 的形成过程为: |
您最近一年使用:0次
2023-03-07更新
|
506次组卷
|
6卷引用:安徽省蚌埠市2022-2023学年高一下学期期末考试化学试题
名校
9 . 下列有关化学用语的表示方法正确的是
A.水的电子式: |
B.用电子式表示 的形成过程为: 的形成过程为: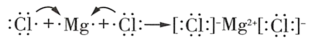 |
C. 核外有a个电子,核内有b个中子,M的原子符号为: 核外有a个电子,核内有b个中子,M的原子符号为: |
D.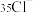 的结构示意图: 的结构示意图: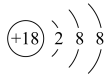 |
您最近一年使用:0次
2023-07-15更新
|
294次组卷
|
4卷引用:安徽省黄山市2022-2023学年高一上学期期末质量检测化学试题
安徽省黄山市2022-2023学年高一上学期期末质量检测化学试题(已下线)专项03 化学用语的正误判断与书写-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)(已下线)寒假作业11 化学键-【寒假分层作业】2024年高一化学寒假培优练(人教版2019必修第一册)天津市武清区杨村第一中学2023-2024学年高三上学期第三次质量检测化学试题
10 . 饱和氯化钠溶液中存在如图所示过程,下列说法正确的是


| A.NaCl固体溶于水,破坏了离子键 | B.此过程中溶解速率小于结晶速率 |
| C.再加入NaCl固体,溶质的物质的量浓度变大 | D.此过程说明NaCl只有在水溶液中才能电离 |
您最近一年使用:0次
2023-02-19更新
|
123次组卷
|
2卷引用:安徽省宣城市2022-2023学年高一上学期期末调研考试化学试题



