1 . 下列晶体中,与 的晶体类型和化学键类型完全相同的是
的晶体类型和化学键类型完全相同的是
 的晶体类型和化学键类型完全相同的是
的晶体类型和化学键类型完全相同的是| A.KCl | B.Cu | C. | D. |
您最近一年使用:0次
名校
2 . 下列说法正确的是
A.常温下, 微溶于水, 微溶于水, 也微溶于水 也微溶于水 |
B.常温下, 难溶于水, 难溶于水, 也难溶于水 也难溶于水 |
| C.常温下,非金属单质均为气态,金属单质均为固态 |
| D.共价化合物中一定不含离子键,离子化合物中一定不含共价键 |
您最近一年使用:0次
名校
解题方法
3 . X、Y、Z、P、Q是原子序数依次增大的短周期主族元素,其中X的一种核素没有中子,Y的单质是空气的主要成分,Z和Q同主族且Q的原子序数是Z的二倍,在短周期元素中P的金属性最强。回答下列问题:
(1)X、Y、Z三种元素的原子半径从大到小的顺序为_______ (用元素符号表示)。
(2)Y、Z的简单氢化物中较不稳定的是_______ (填化学式),P和Q的最高价氧化物对应水化物的化学方程式为_______ 。
(3)M是由X、Z两种元素组成的含有10个电子的分子,M的电子式为_______ ,M分解反应过程中,反应物中化学键断裂吸收的总能量_______ 生成物中化学键形成放出的能量(填“大于”、“小于”或“等于”)。
(4)已知化合物PX与水反应生成氢气,因此可将其用作野外生存的生氢剂。
①该反应的化学方程式为_______ 。
②该反应中的氧化剂是_______ 还原剂是_______ 。
③反应中涉及到化学键的断裂和形成,其中包括_______ 填序号)。
a.离子键 b.极性共价键 c.非极性共价键 d.氢键
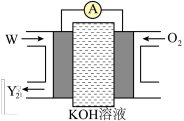
(5)化合物W是由X、Y两种元素组成的含有18个电子的分子,是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料,一种W燃料电池的工作原理如下图所示。放电一段时间,电解质溶液中OH﹣的物质的量浓度_______ (填“增大”“减小”或“不变”),负极反应式为_______ 。
(1)X、Y、Z三种元素的原子半径从大到小的顺序为
(2)Y、Z的简单氢化物中较不稳定的是
(3)M是由X、Z两种元素组成的含有10个电子的分子,M的电子式为
(4)已知化合物PX与水反应生成氢气,因此可将其用作野外生存的生氢剂。
①该反应的化学方程式为
②该反应中的氧化剂是
③反应中涉及到化学键的断裂和形成,其中包括
a.离子键 b.极性共价键 c.非极性共价键 d.氢键
(5)化合物W是由X、Y两种元素组成的含有18个电子的分子,是一种应用广泛的化工原料,常用作火箭和燃料电池的燃料,一种W燃料电池的工作原理如下图所示。放电一段时间,电解质溶液中OH﹣的物质的量浓度
您最近一年使用:0次
4 . 一种以太阳能聚热驱动制备CO和 的过程如图,
的过程如图, 是总反应的催化剂,下列说法正确的是
是总反应的催化剂,下列说法正确的是
 的过程如图,
的过程如图, 是总反应的催化剂,下列说法正确的是
是总反应的催化剂,下列说法正确的是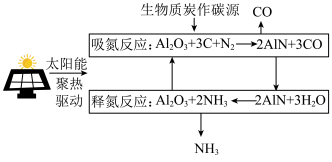
A.CO和 互为同素异形体 互为同素异形体 |
| B.吸氮反应中有非极性共价键的断裂和极性共价键的形成 |
C.释氮反应时,每生成22.4 L ,转移6 mol电子 ,转移6 mol电子 |
| D.CO属于酸性氧化物 |
您最近一年使用:0次
解题方法
5 . NaOH是一种重要的化工原料,工业生产中可利用直流电电解饱和食盐水法来制取:
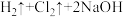 。下列说法正确的是
。下列说法正确的是

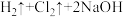 。下列说法正确的是
。下列说法正确的是A.NaCl的电子式为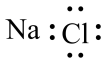 | B.NaOH中含有共价键 |
| C.熔融的NaOH不能导电 | D.该反应的氧化产物为 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法中正确的是
| A.所有铵盐受热均可以分解,产物均有NH3 |
| B.所有铵盐都易溶于水,所有铵盐中的N均呈-3价 |
| C.NH4Cl含有离子键和共价键 |
| D.NH4Cl和NaCl的固体混合物可用升华法分离 |
您最近一年使用:0次
7 . 下列物质中,既含离子键,又含非极性共价键的离子化合物是
| A.NaOH | B.Na2O2 | C.NH4Cl | D.HNO3 |
您最近一年使用:0次
名校
8 . X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,周期表的全部元素中X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半,U的最高化合价和最低化合价的代数和为6;R和Q可形成原子数之比为 和
和 的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。
的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。
请回答下列问题:
(1)Z元素在元素周期表中的位置是_____ ;由上述元素中的四种元素形成的既含有离子键又含有共价键的化合物为_____ (写出其中一种物质的名称)。
(2)Q、R、T三种元素的简单离子半径由小到大顺序为_____ (用离子符号表示)。
(3)T与R二者的最高价氧化物对应的水化物反应的化学方程式为_____ 。T与U二者的最高价氧化物对应的水化物反应的离子方程式为_____ 。
(4)下列可以判断R和T金属性强弱的是_____(填序号)。
(5)Q、R两元素可形成离子化合物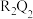 ,
,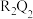 的电子式为
的电子式为_____ ;用电子式表示化合物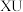 的形成过程
的形成过程_____ 。
 和
和 的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。
的两种化合物:R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应。请回答下列问题:
(1)Z元素在元素周期表中的位置是
(2)Q、R、T三种元素的简单离子半径由小到大顺序为
(3)T与R二者的最高价氧化物对应的水化物反应的化学方程式为
(4)下列可以判断R和T金属性强弱的是_____(填序号)。
| A.单质的熔点R比T低 |
| B.单质与酸反应时,失电子数R比T少 |
| C.单质与水反应R比T剧烈 |
| D.最高价氧化物的水化物的碱性R比T强 |
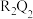 ,
,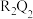 的电子式为
的电子式为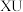 的形成过程
的形成过程
您最近一年使用:0次
名校
解题方法
9 . 下列物质中,只含共价键的是
A. | B. | C. | D. |
您最近一年使用:0次
名校
解题方法
10 . 下面所列的是一组你熟悉的物质:
A.HCl B. C.
C. D.CaO E.NaOH F.
D.CaO E.NaOH F. G.
G.
(1)上述物质中只存在离子键的有___________ (填“序号”,下同);只存在共价键的有___________ 。既存在离子键又存在共价键的有___________ 。
(2)上述物质中属于离子化合物的有___________ ;属于共价化合物的有___________ ,属于非电解质的是___________ 。
A.HCl B.
 C.
C. D.CaO E.NaOH F.
D.CaO E.NaOH F. G.
G.
(1)上述物质中只存在离子键的有
(2)上述物质中属于离子化合物的有
您最近一年使用:0次



