解题方法
1 . 能证明HCl是共价化合物的是
| A.水溶液呈酸性 | B.受热不易分解 |
| C.液态下不能导电 | D.仅由非金属元素组成 |
您最近一年使用:0次
解题方法
2 . 几种主族元素在周期表中的位置如下:
(1)⑤元素的最简单氢化物是________ (填化学式),①和⑦形成的化合物中存在的化学键类型为_______ ,④和⑧形成的化合物中存在的化学键类型为________ 。
(2)①③⑥三种元素原子半径由大到小的顺序是________ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的离子结构示意图为_______ ,该元素在周期表中的位置是________ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的物质的电子式是________ ,③的单质与其反应的离子方程式为________ 。
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是________ (填字母,下同)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑧的气态氢化物溶于水形成的酸酸性比⑦的气态氢化物溶于水形成的酸酸性强
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
(6)用电子式表示①的单质与⑨的单质形成化合物的过程:_______ 。
族 周期 | IA | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑨ | ⑦ | ||||
| 4 | ② | ⑧ | ||||||
(2)①③⑥三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的离子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的物质的电子式是
(5)⑦的非金属性强于⑧,下列表述中能证明这一事实的是
a.⑦的氢化物比⑧的氢化物稳定
b.⑧的气态氢化物溶于水形成的酸酸性比⑦的气态氢化物溶于水形成的酸酸性强
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦氧化物对应的水化物的酸性强于⑧氧化物对应的水化物的酸性
(6)用电子式表示①的单质与⑨的单质形成化合物的过程:
您最近一年使用:0次
名校
解题方法
3 . 下列事实可以证明氯化钠中一定存在离子键的是
| A.水溶液能导电 | B.熔融状态下能导电 |
| C.具有较高的熔点 | D.常温下易溶于水 |
您最近一年使用:0次
2022-04-21更新
|
134次组卷
|
2卷引用:上海市上海外国语大学附属大境中学2021-2022学年高一下学期4月份线上测试化学试题
4 . 根据元素周期表和元素周期律,判断下列叙述不正确的是


A.如图所示实验(左侧锥形瓶内有二氧化碳气体冒出,右侧试管中有硅酸产生)可证明元素的非金属性: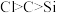 |
| B.氢元素与其他元素既可形成共价化合物也可形成离子化合物 |
C.用中文“ ”(ào)命名的第118号元素在周期表中位于第七周期0族 ”(ào)命名的第118号元素在周期表中位于第七周期0族 |
| D.在元素周期表中金属和非金属的分界处可以找到半导体材料 |
您最近一年使用:0次
名校
解题方法
5 . 现有部分短周期元素的性质或原子结构如表:
(1)元素X在元素周期表中的位置为________ 。
(2)元素Y与氢元素形成离子YH 的电子式为
的电子式为______ 。
(3)下列表述中能证明元素X、元素Y非金属性强弱的是_____ 。
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(4)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是_______ 。
(5)写出实验室制取Y的最简单氢化物的化学方程式:________ 。
(6)在100mL 18 mol∙L−1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式_______ 。
| 元素编号 | 元素性质或原子结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 第三周期元素的简单离子中半径最小 |
(2)元素Y与氢元素形成离子YH
 的电子式为
的电子式为(3)下列表述中能证明元素X、元素Y非金属性强弱的是
a.常温下X的单质和Y的单质状态不同
b.Y的最高价氧化物对应水化物的酸性比X的最高价氧化物对应水化物的酸性强
c.X与Y形成的化合物中X元素呈正价状态
(4)Y的最高价氧化物的水化物与气态氢化物合成的化合物含的化学键类型是
(5)写出实验室制取Y的最简单氢化物的化学方程式:
(6)在100mL 18 mol∙L−1的浓硫酸中加入过量的铜片,加热使之充分反应,若使剩余的铜片继续溶解,可向其中加入硝酸钠,写出反应的离子方程式
您最近一年使用:0次
名校
6 . 下表为元素周期表的一部分,请回答下列有关问题
(1)已知元素⑩的一种核素,其中子数为45,用原子符号表示该核素为_______ 。
(2)由元素①和④形成的四核分子的结构式为_______ 。
(3)由上述元素构成的淡黄色固体化合物的电子式为_______ ,该化合物所含的化学键类型为_______ (填“离子键”、“极性键”或“非极性键”),若将少量该固体投入到含有 、
、 、
、 、
、 的溶液中,反应完全后,上述离子数目增大的有
的溶液中,反应完全后,上述离子数目增大的有_______ (用离子符号表示)。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是_______ (用离子符号表示),元素⑨的最高价氧化物对应水化物与元素⑥的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)元素的非金属性⑧_______ ⑩(填“>”或“<”);下列事实不能证明上述结论的是_______ 。
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
(2)由元素①和④形成的四核分子的结构式为
(3)由上述元素构成的淡黄色固体化合物的电子式为
 、
、 、
、 、
、 的溶液中,反应完全后,上述离子数目增大的有
的溶液中,反应完全后,上述离子数目增大的有(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素的非金属性⑧
A.元素⑧的单质与⑩的氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的最高价氧化物对应水化物的酸性比元素⑩的强
C.元素⑧和⑩的氢化物受热分解,前者的分解温度高
D.元素⑧的氢化物的水溶液的酸性比元素⑩的弱
E.元素⑧的氢化物的还原性比元素⑩的弱
您最近一年使用:0次
2022-01-08更新
|
547次组卷
|
3卷引用:黑龙江省哈尔滨市第三中学校2021-2022学年高一上学期期末考试化学试题
7 . 下表列出了9种元素在元素周期表中的位置。

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是_______
(2)画出元素⑧形成的简单离子的结构示意图_______
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为_______
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是_______
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是_______ (填化学式)
(6)写出元素⑥的单质与水反应的离子反应方程式_______
(7)写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式_______

请回答下列问题:
(1)考古工作者利用元素②的一种核素测定一些文物的年代,这种核素的符号是
(2)画出元素⑧形成的简单离子的结构示意图
(3)写出元素④和⑥的单质在加热条件下反应,所得产物的电子式为
(4)⑥元素的最高价氧化物对应的水化物含有的化学键是
(5)②、③、④、⑤四种元素的简单气态氢化物中,稳定性最强的是
(6)写出元素⑥的单质与水反应的离子反应方程式
(7)写出一个能证明元素⑧比元素⑨非金属性强的反应事实的离子方程式
您最近一年使用:0次
2021-03-24更新
|
133次组卷
|
2卷引用:江苏省高邮临泽中学2020-2021学年高一下学期3月质量测试化学试题
名校
解题方法
8 . 表为元素周期表的一部分,表中所列的字母分别代表某一化学元素,回答下列问题:

(1)元素B在元素周期表中的位置是_______ ,B、C、D三种元素原子半径从大到小的顺序是_______ (填元素符号)。
(2) A与C按原子个数比1:1组成的物质其电子式为_______ 。
(3) C的氢化物比同族下一周期元素的氢化物沸点_______ (填“高”或“低”)。
(4)元素D的单质在元素C的单质中点燃生成X,X中的化学键除了离子键,还有_______ (填“极性”或“非极性”)共价键,若将其投入硫酸亚铁溶液中,预测主要的反应现象是_______ 。
(5)上述中X常用作呼吸面具和潜水艇中的供氧剂,可选用合适化学试剂和图中所示实验装置证明。

①装置A使用石灰石与浓盐酸反应制取CO2,装置B中所加入的试剂为_______ 。
②装置C中X与CO2反应的化学方程式是_______ 。
③装置D的作用为_______ 。

(1)元素B在元素周期表中的位置是
(2) A与C按原子个数比1:1组成的物质其电子式为
(3) C的氢化物比同族下一周期元素的氢化物沸点
(4)元素D的单质在元素C的单质中点燃生成X,X中的化学键除了离子键,还有
(5)上述中X常用作呼吸面具和潜水艇中的供氧剂,可选用合适化学试剂和图中所示实验装置证明。

①装置A使用石灰石与浓盐酸反应制取CO2,装置B中所加入的试剂为
②装置C中X与CO2反应的化学方程式是
③装置D的作用为
您最近一年使用:0次
解题方法
9 . 下列说法正确的是( )
| A.CaO与水反应过程中,有共价键的断裂和形成 |
| B.H2O的热稳定性比H2S强,是由于H2O的分子间作用力较大 |
| C.KCl、HCl、KOH的水溶液都能导电,所以它们都属于离子化合物 |
| D.将盐酸加入Na2CO3溶液中,产生的气体能使Na2SiO3溶液变浑浊,可证明非金属性:Cl>C>Si |
您最近一年使用:0次
名校
10 . 类推是化学学习中的常用方法,但类推的结论最终要经过实践的检验才能证明其正确与否。下列类推结论中正确的是
| A.第二周期元素氢化物稳定性顺序是HF﹥H2O﹥NH3,则第二周期元素氢化物沸点顺序是HF﹥H2O﹥NH3 |
| B.可电解熔融氯化镁来制取金属镁,则也能用电解熔融氯化钠来制取金属钠 |
| C.Fe3O4可写成FeO·Fe2O3,则Pb3O4也可写成PbO·Pb2O3 |
| D.常见的氢化物是分子晶体,则所有的氢化物都是分子晶体 |
您最近一年使用:0次



