名校
1 . 下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)从元素原子得失电子的角度看,元素⑤具有___________ (填“氧化性”或“还原性”)。
(2)元素②形成的单质气体含有___________ (填“极性”或“非极性”)共价键。
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为___________ 。
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是___________ (填化学式,下同),最高价氧化物对应的水化物具有两性的物质是___________ ,这两种物质反应的离子方程式为___________ 。
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是___________ (填离子符号)。
| 族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)从元素原子得失电子的角度看,元素⑤具有
(2)元素②形成的单质气体含有
(3)元素③、⑨与H原子以原子个数比为1∶1∶1形成的化合物的电子式为
(4)第三周期中元素的最高价氧化物对应水化物中碱性最强的是
(5)元素③、⑤、⑨形成简单离子的半径由大到小的顺序是
您最近一年使用:0次
名校
2 . 我国科学家研究了活性炭催化条件下煤气中H2S和Hg的协同脱除,部分反应机理如图所示(吸附在催化剂表面的物种用*标注)。下列说法正确的是
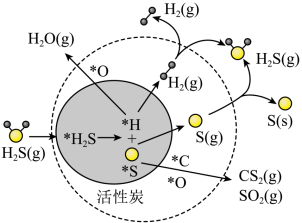
| A.图示反应过程中有极性共价键的断裂,没有非极性共价键的生成 |
| B.H2S活性炭分解生成H2(g)和S(s)的过程释放能量 |
| C.整个脱硫过程中硫元素既表现出氧化性又表现出还原性 |
| D.该机理由于活性炭的参与降低了H2S分解的热效应,使反应更易进行 |
您最近一年使用:0次
2023-04-29更新
|
233次组卷
|
5卷引用:山东省菏泽市2022-2023学年高一下学期期中考试化学(A)试题
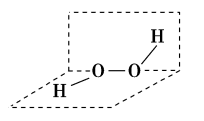
3 . 过氧化氢( )被称为绿色氧化剂,其分子结构如图所示。两个氢原子位于不重合的两个平面上,两个氧原子位于两平面的交线上。下列有关说法不正确的是
)被称为绿色氧化剂,其分子结构如图所示。两个氢原子位于不重合的两个平面上,两个氧原子位于两平面的交线上。下列有关说法不正确的是
 )被称为绿色氧化剂,其分子结构如图所示。两个氢原子位于不重合的两个平面上,两个氧原子位于两平面的交线上。下列有关说法不正确的是
)被称为绿色氧化剂,其分子结构如图所示。两个氢原子位于不重合的两个平面上,两个氧原子位于两平面的交线上。下列有关说法不正确的是
A. 既有氧化性又有还原性 既有氧化性又有还原性 |
| B.过氧化氢分子中含有H—H键、O—O键 |
C.过氧化氢分子的电子式为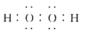 |
| D.过氧化氢分子中存在极性共价键和非极性共价键 |
您最近一年使用:0次
名校
解题方法
4 . A、B、C、D、E、F、G的原子序数依次增大的元素,A、D元素的原子最外层电子数相同,A元素的一种原子没有中子;B的一种同位素可用于考古断代;C是地壳中含量最多的一种元素;D元素的阳离子电子层结构与氖原子相同;E的最外层电子数是电子层数的2倍;F的单质具有强氧化性。G是用途最广泛的金属元素,它的单质能被磁铁所吸引;试回答以下问题:
(1)E的原子结构示意图:____ 。
(2)D单质与C单质在加热条件下反应产物的电子式____ ,该物质与A的氧化物反应产生氧气,离子方程式为_____ 。
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为____ 。
(4)G单质在一定条件下可以和A2C反应,方程式为_______ 。
(5)用电子式写出A2C的形成过程_______ 。
(1)E的原子结构示意图:
(2)D单质与C单质在加热条件下反应产物的电子式
(3)化合物甲、乙由A、B、C、D中的三种或四种组成的常见物质,且甲、乙的水溶液均呈碱性。则甲、乙反应的化学方程式为
(4)G单质在一定条件下可以和A2C反应,方程式为
(5)用电子式写出A2C的形成过程
您最近一年使用:0次
名校
解题方法
5 . 下表列出了①~⑨九种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素④的名称是________ ,元素④在周期表中所处位置________ ,从元素原子得失电子的角度看,元素④形成的单质具有________ 性(填“氧化性”或“还原性”)。
(2)元素⑦的原子结构示意图是________ 。
(3)按气态氢化物的稳定性由弱到强的顺序排列,④⑦⑨的氢化物稳定性:_____________________ (写氢化物的化学式)。
(4)写出元素⑤形成的单质与水反应的化学方程式_____________________ 。
(5)①与⑨能形成一种化合物,用电子式表示该化合物的形成过程_____________________ 。
(6)工业制取⑥的单质的反应的化学方程式为_____________________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ⑧ |
(1)元素④的名称是
(2)元素⑦的原子结构示意图是
(3)按气态氢化物的稳定性由弱到强的顺序排列,④⑦⑨的氢化物稳定性:
(4)写出元素⑤形成的单质与水反应的化学方程式
(5)①与⑨能形成一种化合物,用电子式表示该化合物的形成过程
(6)工业制取⑥的单质的反应的化学方程式为
您最近一年使用:0次
10-11高一下·浙江杭州·期中
6 . 2004年某一期的《美国化学杂志》报道,中国科学家以二氧化碳为碳源,金属钠为还原剂,在470℃、80MPa下合成金刚石,具有深远意义。下列说法不正确的是
| A.由二氧化碳合成金刚石是化学变化 | B.在该反应中金属钠体现了强还原性 |
| C.在该反应中二氧化碳体现了强氧化性 | D.金刚石中只含有非极性共价键 |
您最近一年使用:0次
名校
解题方法
7 . W、X、Y、Z为原子序数依次增大的短周期主族元素,W、X、Y三种元素原子的最外层电子数之和为11;W、X同周期且相邻,W的最外层电子数为4, 的M层有8个电子。下列结论正确的是
的M层有8个电子。下列结论正确的是
 的M层有8个电子。下列结论正确的是
的M层有8个电子。下列结论正确的是| A.X、Y、Z离子半径的大小顺序为Z>Y>X |
| B.Y与Z形成的化合物为共价化合物 |
| C.最高价氧化物对应的水化物的酸性:Z<W |
| D.单质氧化性:Z>X |
您最近一年使用:0次
2023-01-20更新
|
288次组卷
|
5卷引用:河南省叶县高级中学2022-2023学年高一上学期1月期末考试化学试题
8 . 将“84”消毒液和洁厕灵同时使用会发生反应: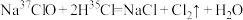 。下列有关说法中正确的是
。下列有关说法中正确的是
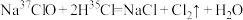 。下列有关说法中正确的是
。下列有关说法中正确的是A.该反应生成 的摩尔质量为 的摩尔质量为 |
B. 和 和 所含中子数之比为35∶37 所含中子数之比为35∶37 |
C.该反应中,体现了 的酸性和氧化性 的酸性和氧化性 |
| D.该反应涉及的物质中有4种物质含共价键 |
您最近一年使用:0次
名校
9 . 下列对氯及其化合物的说法正确的是
| A.氯化铝溶液能导电,所以氯化铝是离子化合物 |
| B.用pH试纸测得氯水的pH=4 |
| C.次氯酸不如次氯酸盐稳定,故用次氯酸盐作为漂白剂的主要成分 |
| D.随着化合价的升高,氯的含氧酸酸性和氧化性均逐渐增强 |
您最近一年使用:0次
解题方法
10 . 下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最不活泼的是: (填具体元素符号或化学式,下同),非金属性最强的元素是: 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是:_________;写出它的最高价氧化物与氢氧化钠反应的离子方程式:____________________________________。
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是: (填“共价键”或“离子键”)。
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是:_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是:_________;写出它的最高价氧化物与氢氧化钠反应的离子方程式:____________________________________。
(4)④与⑧形成的化合物的电子式是: ,该化合物所含化学键类型是: (填“共价键”或“离子键”)。
(5)试设计实验方案比较④与⑤的化学性质(金属性),有关实验步骤、现象和结论填入下表
| 实验步骤 | 实验现象与结论 |
您最近一年使用:0次



